消除肝炎不容等待,Biacore始终陪伴左右
近年来,中国科学家在抗多种肝炎病毒(HAV、HBV、HCV、HDV、HEV)药物的设计与发现中硕果累累,为全人类的健康贡献非凡。Biacore作为分子互作的“金标准”,已助力近五万篇文章的发表与上百款药物的上市,在肝炎药物的研究中,Biacore同样表现出色!接下来,小编带大家赏析几篇Biacore与肝炎药物设计和发现的故事。

甲型肝炎HAV:保守抗原表位的发现与高效抑制剂的合理设计
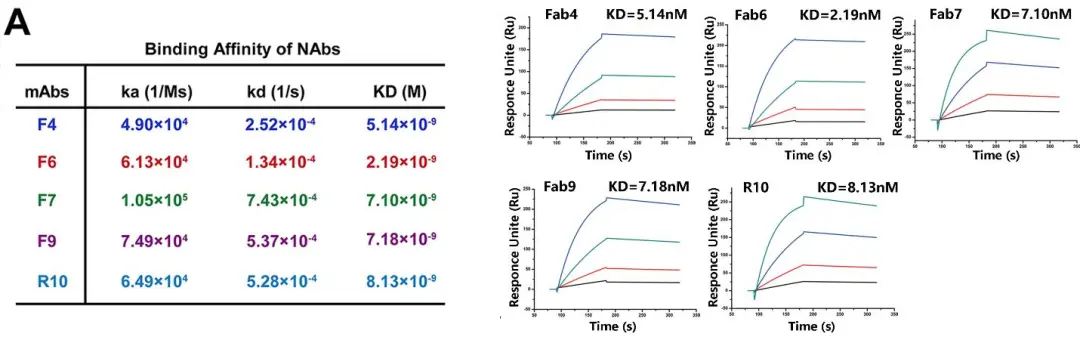
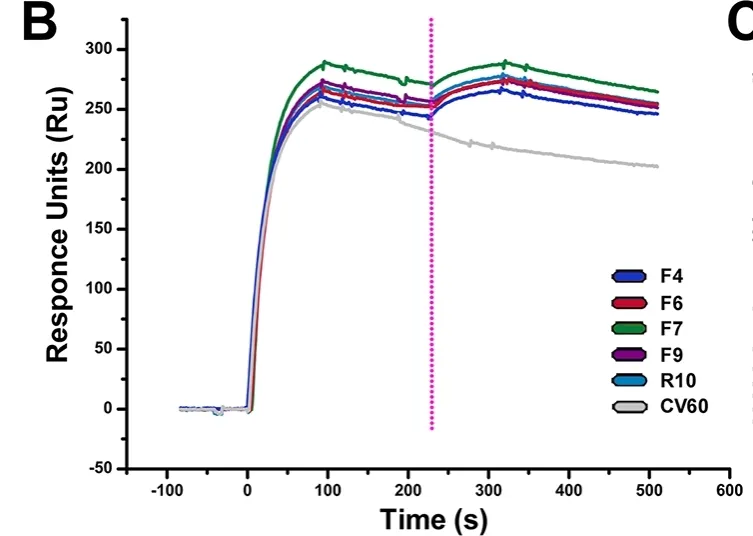
科研人员筛选分离得到了4个HAV中和性抗体(F4, F6, F7和F9),加上先前实验获得的中和性抗体R10,至此获得了5个中和性抗体。然后使用Biacore,检测HAV全颗粒与5个中和抗体的亲和力KD和动力学(Ka和kd)(图2)。结果显示,5个中和性抗体(F4, F6, F7, F9和R10)与HAV均能结合,并且亲和力均高达nM级别,分别为5.14 nM, 2.19 nM, 7.10 nM, 7.18 nM和8.13 nM。
乙型肝炎HBV:基于疫苗诱导的治疗性抗体药发现
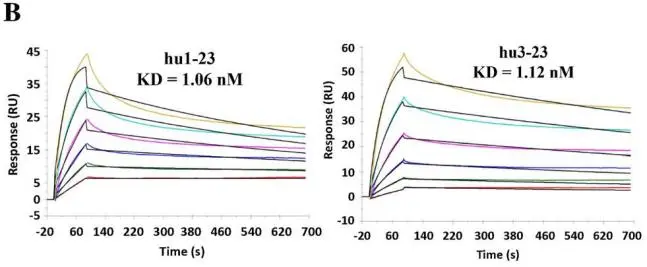
科研人员从接种CR-T3-SEQ13 (HBsAg aa 113-135) 疫苗的食蟹猴中分离出多个anti-HBsAg的单克隆抗体,其中C1-23和C3-23显示出最好的HBsAg 清除率和病毒抑制功效。进一步对C1-23和C3-23进行人源化改造,分别命名为hu1-23和hu3-23。使用Biacore,对二者与HBsAg的亲和力KD检测,结果显示亲和力均在nM级别,分别为1.06 nM和1.12 nM(图4)。
乙型肝炎HBV:基于phage display的治疗性抗体药发现
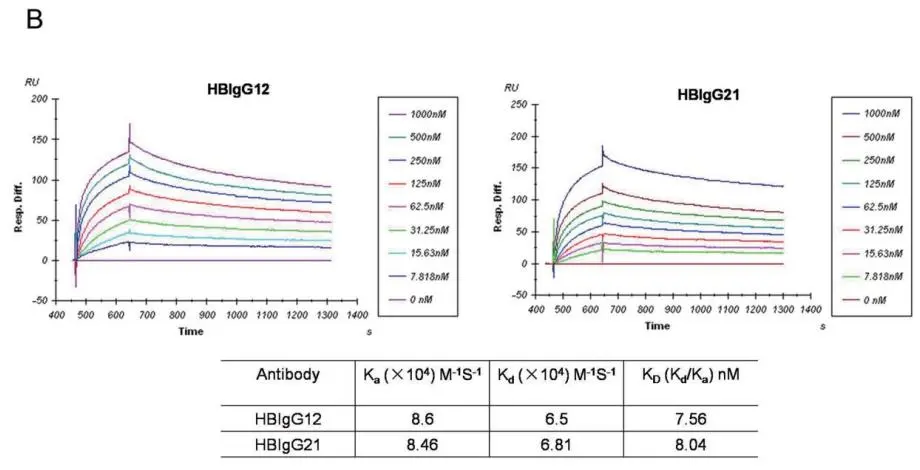
科研人员通过phage display筛选到了HBFab12和HBFab21,据此构建为IgG1单克隆抗体,分别命名为G12和G21。为进一步验证两个单克隆抗体与HBV小包膜蛋白(S)的结合情况,科研人员使用Biacore,对其亲和力KD和动力学(Ka和kd)进行检测,结果显示G12和G21与抗原的亲和力均在nM级别,分别为7.56 nM和8.04 nM(图5)。在 HBV 持续存在的转基因小鼠模型中,单次腹腔注射 G12 显着降低了所有 7 只小鼠的血清 HBsAg 滴度,表明G12是治疗乙型肝炎的潜在候选药物。
丙型肝炎HCV:新型强效NS5B 聚合酶抑制剂的发现
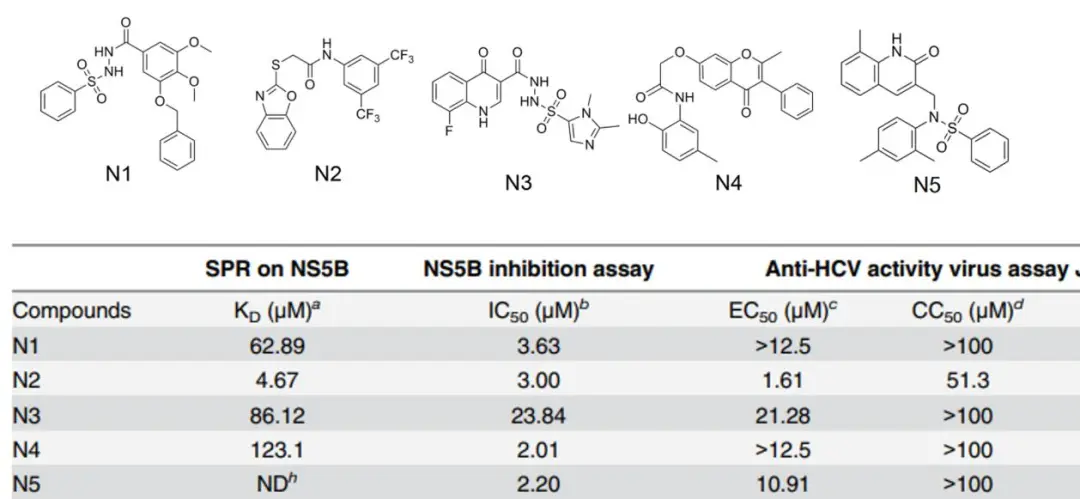
科研人员采用基于随机森林 (RB-VS)、电子药效团 (PB-VS) 和对接 (DB-VS) 的虚拟筛选方法,筛选 InterBioScreen 数据库,最终获得了5个潜在的靶向HCV NS5B 聚合酶的化合物。为验证虚拟筛选得到的化合物是否与NS5B结合以及亲和力KD数据,研究人员使用Biacore进一步验证,结果显示,各化合物与NS5B的结合均在μM 级别(KD = 4.67–123.1 μM),其中N2与NS5B的结合最强(图6),与抗病毒活性的结果一致(EC50)。另外,所有化合物均能抑制 HCV NS5B 聚合酶的活性(IC50),并且除了N2显示出较弱的细胞毒性,其他均无细胞毒性(CC50 > 100 μM)。至此,找到了5 个潜在的HCV NS5B 聚合酶抑制剂供进一步优化和开发,作为治疗HCV感染药物开发的先导化合物。
丁型肝炎HDV和乙型肝炎HBV:
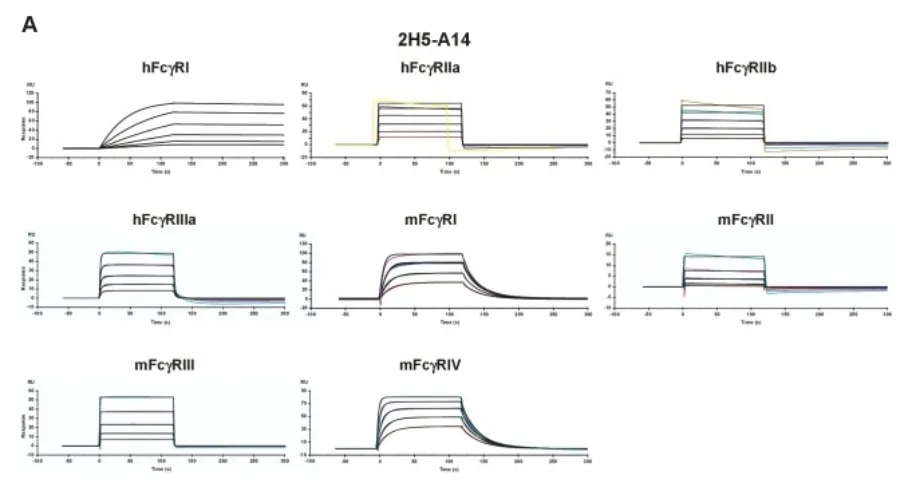
科研人员从噬菌体文库中鉴定了六个抗 preS1抗体,进一步实验表明,其中抗体2H5-A14 通过结合preS1 ,抑制其与 NTCP 的结合,从而阻止乙型肝炎HBV和丁型肝炎HDV的感染。为了进一步验证 2H5-A14 的 ADCC 活性,科研人员使用Biacore,检测了抗体2H5-A14与FcγRs受体的结合情况,结果显示2H5-A14与FcγRs受体均能结合(图7),表明中和性抗体2H5-A14 可以通过Fc-FcγR互作依赖的效应功能(如ADCC)杀死靶细胞。
自 1990 年上市至今,Biacore作为唯一被中美日药典收录的分子互作检测“金标准”,已广泛应用到基础科研与药物开发的多个领域。截至目前,借助 Biacore 累计发表的文章已近50000 篇,超过百种的已上市药物的研发、申报、生产过程中也均有 Biacore 的身影。相信有了Biacore助力“产学研”,未来一定会有越来越多的药物从研发走向上市。

 收藏
收藏 询价
询价