新型双特异性抗体Zanidatamab结构设计及活性验证思路
自拉罗替尼与恩曲替尼问世以来,广谱抗癌呈现千帆竞发的趋势。Zanidatamab作为大分子类药物的明星代表,先后获得FDA给予的孤儿药认定,快速审批认定,突破性疗法认定,成为双抗药物领域“最亮的崽”。
近期,Zymeworks公司发表文章《An anti-HER2 biparatopic antibody that induces unique HER2 clustering and complement-dependent cytotoxicity》(图1),详细阐述了Zanidatamab的研发思路。其中,Zanidatamab结构设计及活性验证思路之灵巧,值得我们借鉴,接下来我们一睹为快。

01
Zanidatamab结构设计
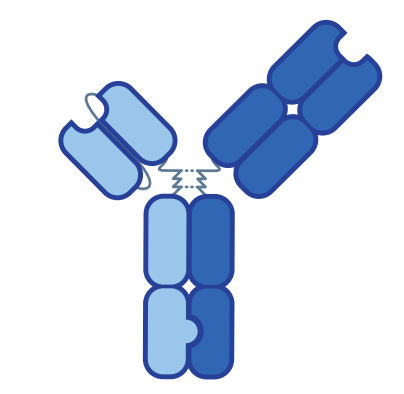
02
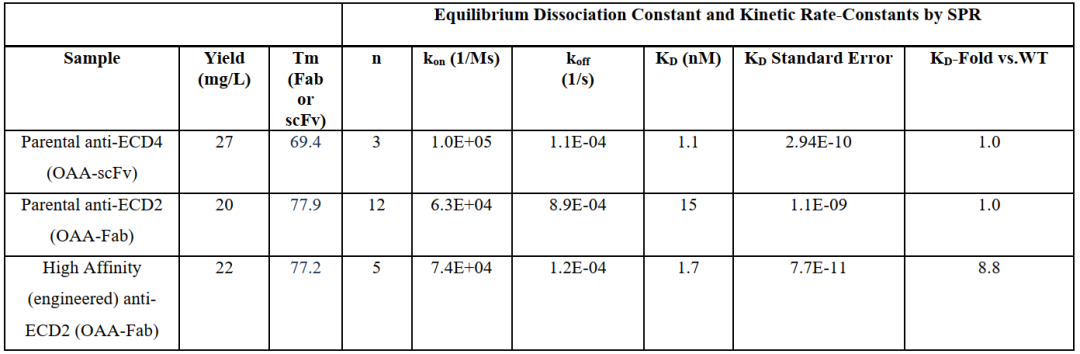
结构改造,提升亲和力,增强靶点交联
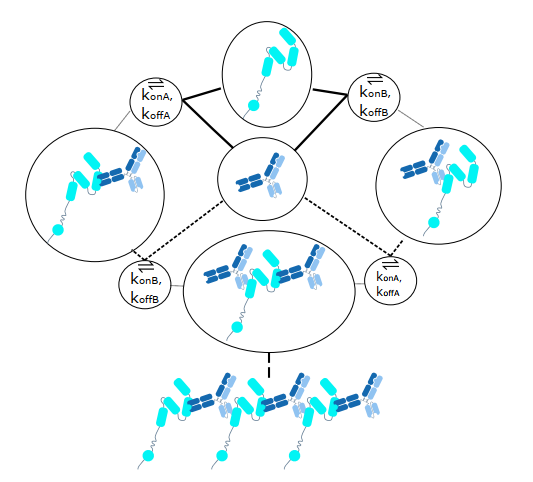
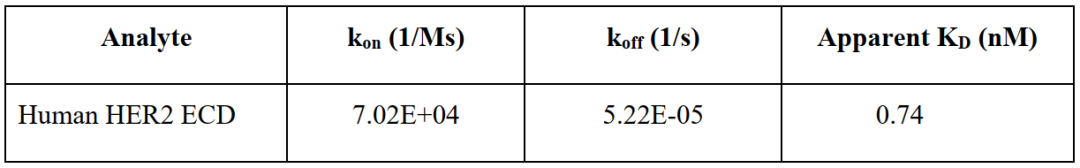
双抗诱导靶点交联可以增强受体驱动型内吞及受体下调,研究人员构建计算动力学模型(图3),并计算出提升靶向HER2-ECD2 Fab亲和力将最大程度增强靶点交联。研发人员随即设计出一系列突变,并以OAA形式使用Biacore进行筛选,最终获得亲和力增强8倍的Fab(表1),使得Zanidatamab与人HER2亲和力达到0.74 nM(表2)。
03
验证结合机制,确认cis/trans结合模式
为了验证Zanidatamab与HER2-ECD的结合机制并获得关于cis/trans受体结合能力信息,研发人员首先归纳出单/双抗与HER2结合的类型(图4)。接下来,研发人员借助Biacore,在芯片表面偶联不同密度抗体,以koff值进行验证(图5)。
Trastuzumab不会因抗体偶联密度而改变koff值;
前体Zanidatamab及Zanidatamab若以cis形式结合,则koff值也不会改变;
前体Zanidatamab及Zanidatamab若以trans形式结合,则koff值变小。
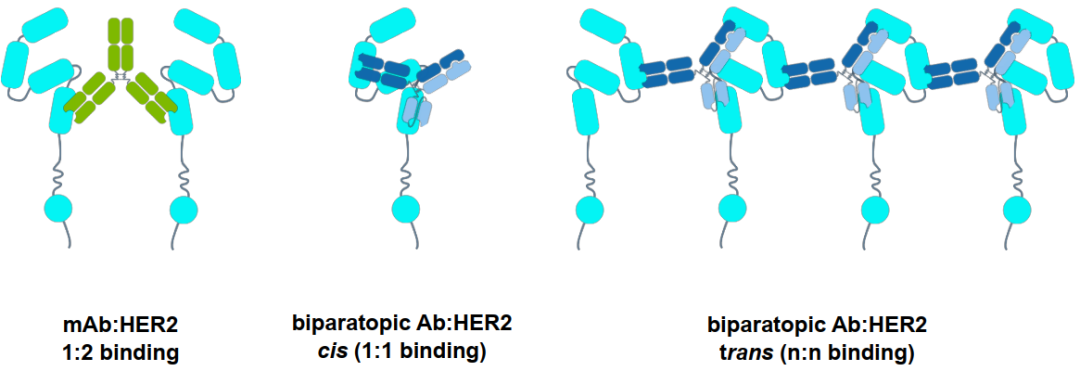
图4:单/双抗与HER2结合模式
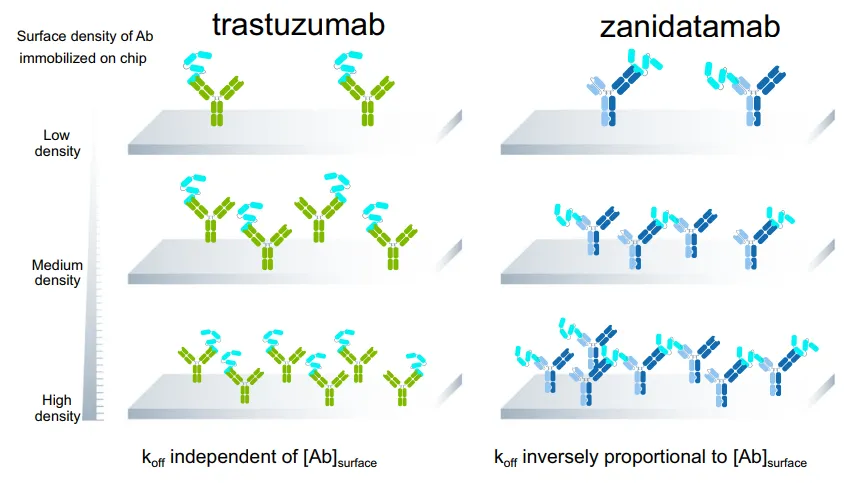
图5:Biacore实验设计思路
最终,Biacore实验结果显示,Trastuzumab koff值不变,前体Zanidatamab及Zanidatamab的koff值变小,确认受体trans结合模式(图6),该结果与超速离心、电镜实验结果相互印证。
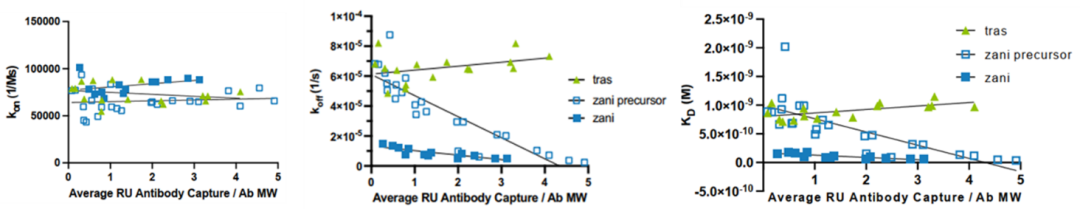
图6:Biacore实验动力学数据
Zanidatamab在细胞模型、动物模型、临床试验上的优异表现得益研发人员精巧的结构设计及后期活性验证。而Biacore凭借数据精准可靠,平台灵活易用,成为研发人员最重要的技术手段。相信在广谱抗癌的潮流中,Biacore将助力更多明星药物,普惠亿万受众。

 收藏
收藏 询价
询价