2024开箱盘点:过去一年Biacore和CNS的那些事儿
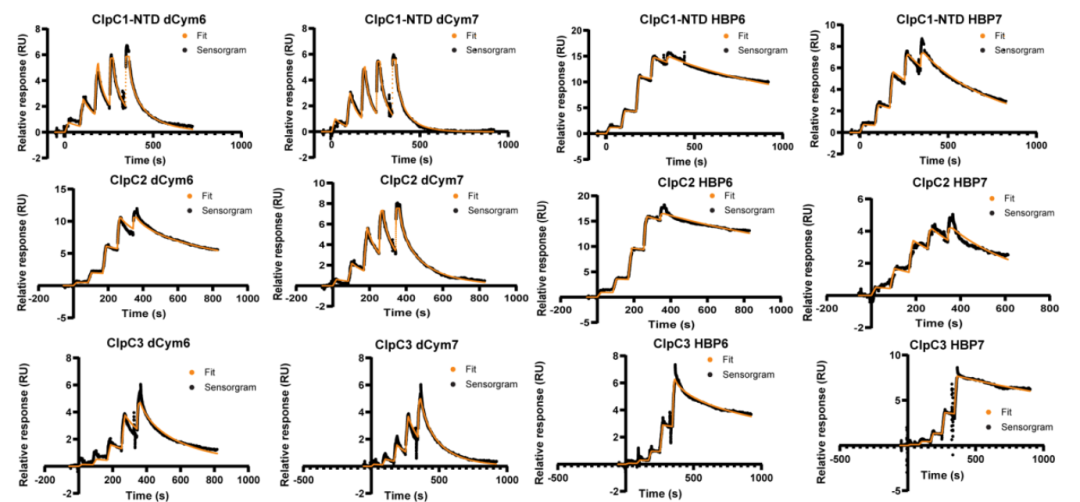
图1:NTA芯片Capture & Coupling后,检测ClpC3与药物的亲和力
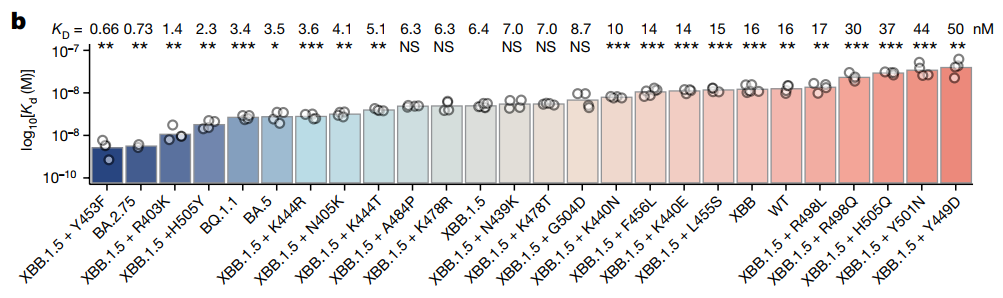
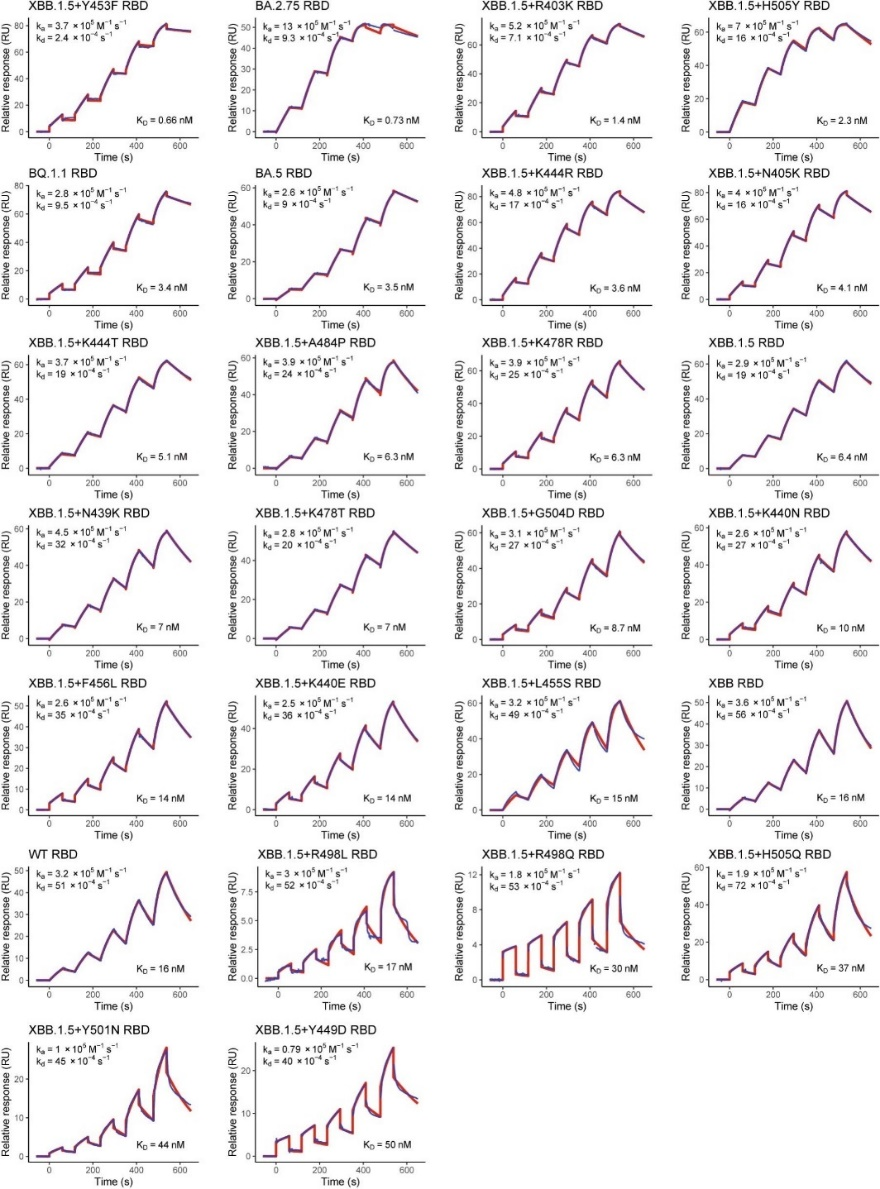
图2:Biacore检测SARS-CoV-2突变体RBD与hACE2的亲和力KD
2023年Science主刊发表了来自美国诺华热带病研究所和格拉斯哥大学一篇题为“Cyanotriazoles are selective topoisomerase II poisons that rapidly cure trypanosome infections”的文章,报道了一类具有强效的锥虫杀伤活性的氰三唑 (CTs) 新型药物。CT化合物通过稳定双链DNA的拓扑异构酶II:酶切割复合物发挥作用。Biacore直接证实在CT1存在下Topo II与dsDNA的亲和力从1.33 μM提升至1 nM,从Biacore独特的单循环动力学分析功能得到的动力学数据可以看出解离速率降低130倍是提高酶切割复合物稳定性的直接原因。
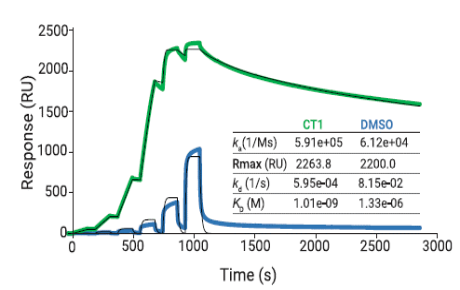
图3:Biacore检测在CT1存在下Topo II与dsDNA的亲和力和动力学
自制捕获芯片:轻松搞定核酸样品
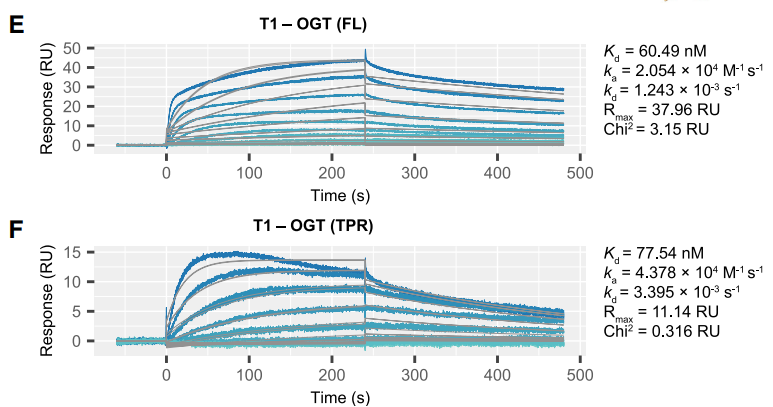
图4:Biacore检测靶点与适配体亲和力
Buffer selector:快速实现不同pH条件的互作检测
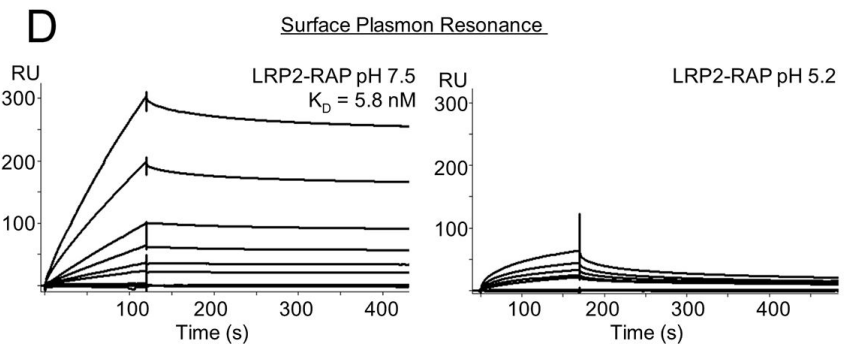
图5:Biacore检测不同pH下LRP2与受体相关蛋白RAP的结合能力
Biotin CAPture芯片:Biotin标签配体也能实现可逆捕获
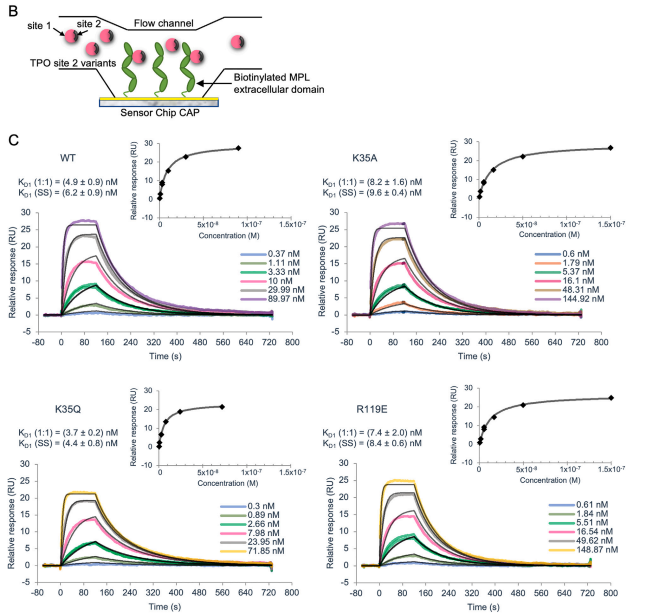
图6:Biotin CAPture芯片检测TPO与受体的结合能力
互作实验的多项选择:单循环动力学和多循环动力学
2023年3月,中科院生物物理研究所和北京生命科学研究所在Nature上发表了题为“Structural mechanisms for regulation of GSDMB pore-forming activity”的研究论文,揭示了IpaH7.8特异性识别GSDMB和GSDMD两种焦亡蛋白的结构基础,破解了GSDMB可变剪接调控细胞焦亡活性的精确分子机理。该研究通过Biacore发现,全长GSDMB与IpaH7.8亲和力为432 nM,比全长GSDMD与IpaH7.8的亲和力和强了约77倍,并且GSDMB的C端与IpaH7.8不结合。
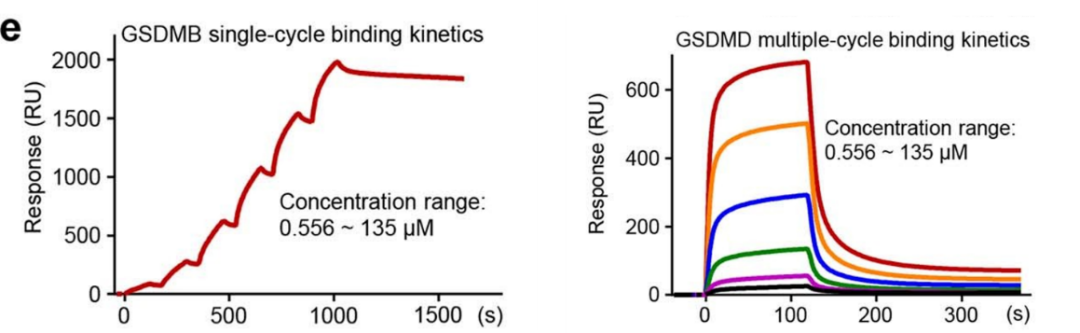

图7:Biacore检测全长GSDMB及其C端、全长GSDMD及其C端与IpaH7.8亲和力
大小通吃:人体最大抗体IgM研究新突破
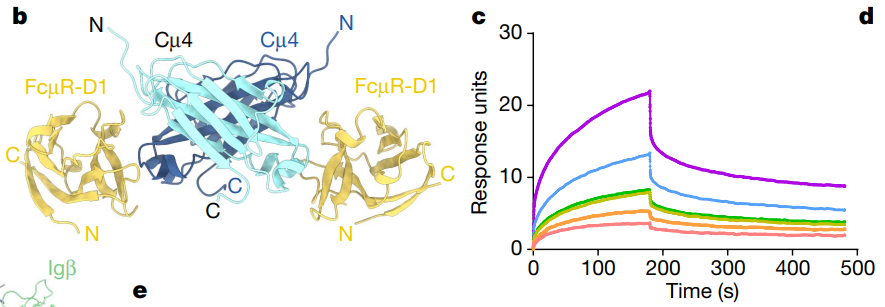
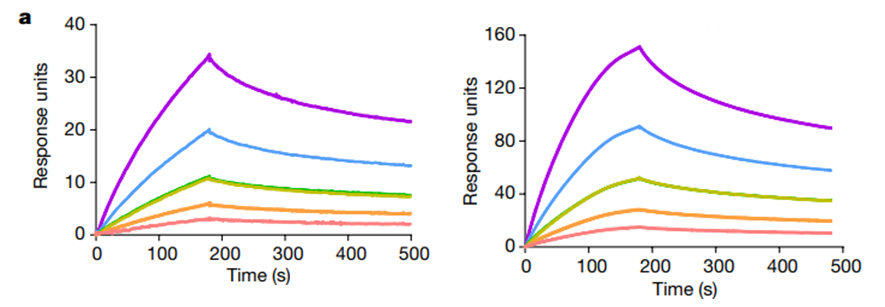
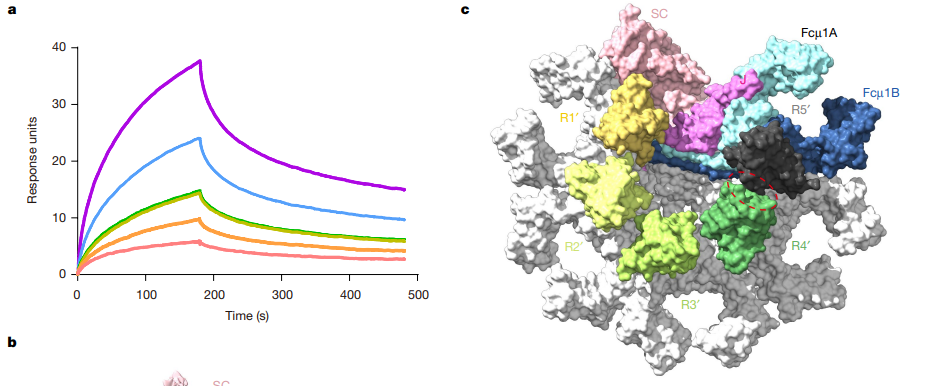
图8:Biacore检测多种类型的IgM(mIgM、pIgM和sIgM)与FcμR的亲和力
参考文献:

 收藏
收藏 询价
询价