超越单靶点!Biacore验证TMEM175双位点协同,开启神经退行治疗新范式
跨膜蛋白175(TMEM175)的上调通过促进α-突触核蛋白聚集体的清除,具有改善帕金森病(PD)的潜力。理解TMEM175激动剂的结构基础对于揭示其PD治疗潜力至关重要。
近日,中山药物创新研究院、中国科学院上海药物研究所、南京中医药大学药学院及中南大学湘雅医院等13家单位联合在《Neuron》发表最新研究,首次解析人源TMEM175离子通道与三种激动剂的冷冻电镜结构,为基于结构的药物设计奠定了基础,并验证了TMEM175激动剂可有效降低病理性α-synuclein水平,为开发治疗PD的新型DMT提供了重要思路。
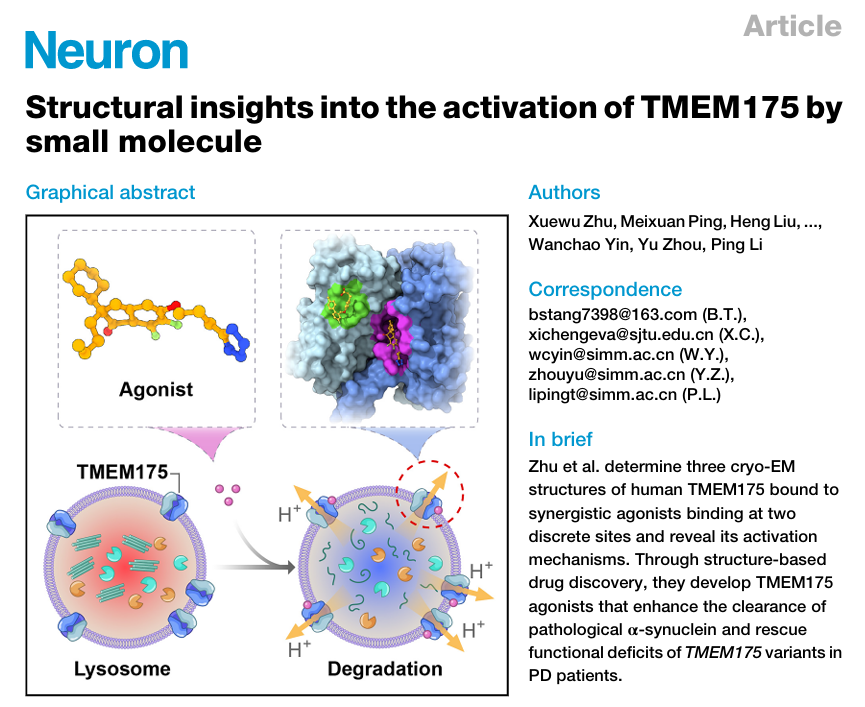
在帕金森病靶点TMEM175激动剂的研发中,精确测定小分子与靶蛋白的结合亲和力是优化先导化合物的关键一步。研究团队如何运用Biacore 8K系统,为DCY1020、DCY1040等候选分子提供关键的动力学数据支撑?
研究人员使用Biacore 8K SPR系统,对候选分子与TMEM175的结合进行了精准量化:
- 芯片固定化:氨基偶联法,将经过peptidisc稳定化处理的TMEM175蛋白共价固定于CM5传感器芯片上,确保了靶蛋白在天然状态下的活性。
- 图片
样品检测:将候选化合物DCY1020、DCY1040和TUG-891进行梯度稀释,以30 μL/min的流速进样,实时监测分子结合与解离过程。 - 图片
数据分析:通过Biacore Insight专业软件进行动力学分析,获得结合亲和力(KD值)等关键参数,为结构优化提供明确方向。
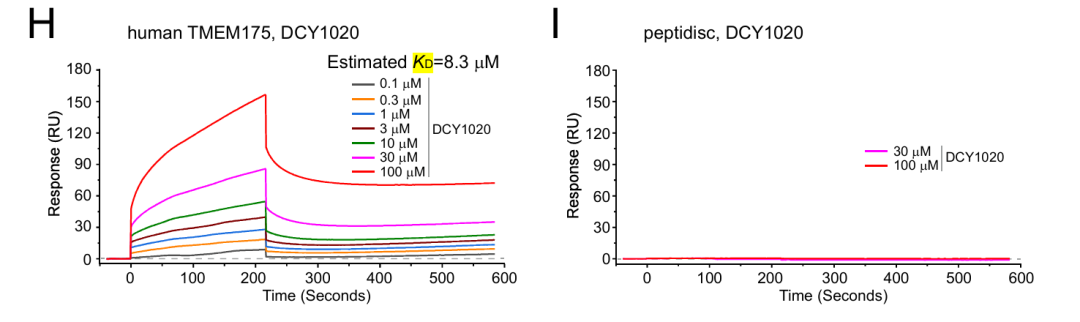
图2:DCY1020与人类TMEM175结合
DCY1020未显示与peptidisc的结合
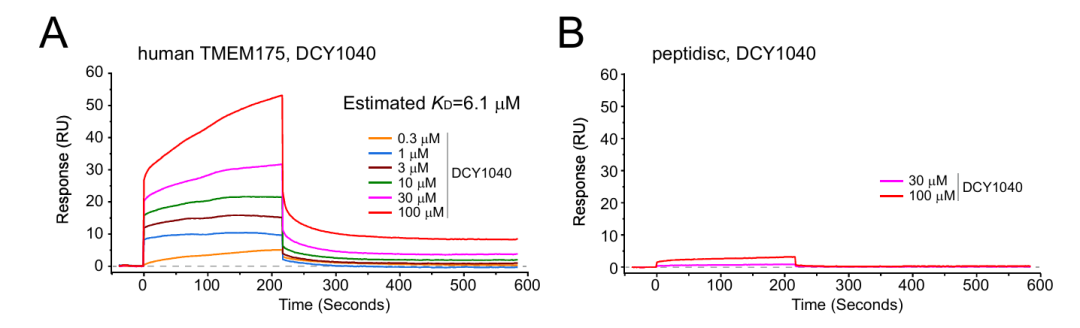
DCY1040未显示与peptidisc的结合
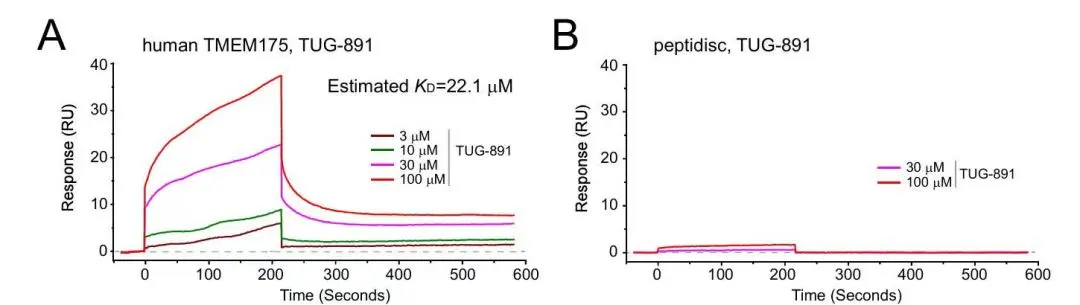
TUG-891未显示与peptidisc的结合
由此可见,此项研究成功地将精准的动力学数据(Biacore)、清晰的原子结构(Cryo-EM)与可靠的功能验证相结合,完整地诠释了TMEM175的激活机制。这不仅为帕金森病的药物开发指明了新方向,也再次证明,多技术平台的紧密协同,是攻克复杂靶点、推动源头创新的有效路径。
无论是破解病理谜题,还是推动药物的临床转化,Biacore都如科研路上的“精准导航仪”,助力科学家突破技术瓶颈。以技术创新赋能基础研究,以全流程支撑加速药物落地,最终让更多像帕金森病这样的难治性疾病患者看到希望,持续为生命科学进步与人类健康保驾护航。

 收藏
收藏 询价
询价