关爱女性,呵护健康–Biacore在乳腺癌药物开发与疾病机理研究中的应用
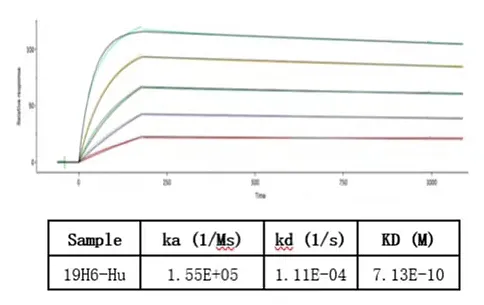
2020 年 6 月 19 日,三生国健药业 (上海) 股份有限公司自主研发的注射用伊尼妥单抗(商品名:赛普汀®)正式获得国家药品监督管理局批准(如图 1 所示),获批的首个适应症为和化疗联合用于治疗 HER2 阳性的转移性乳腺癌。作为我国首个获批的自主研发、Fc 段修饰和生产工艺优化的抗 HER2 单抗,伊尼妥单抗具有更强的 ADCC 效应,为中国 HER2 阳性转移性乳腺癌患者带来更多选择。而在伊尼妥单抗的研发与申报过程中,同样离不开 Biacore,其药物与靶点的结合亲和力正是通过 Biacore 8K 来完成的(如图 2 所示)。

图 1:伊尼妥单抗(商品名:赛普汀®)
正式获得国家药品监督管理局批准

与此同时,广大科研工作者也在针对乳腺癌发生机制研究的过程中贡献着自己的力量。继 2018 年在 Nucleic Acids Research 发表 PHF1 蛋白作用于组蛋白促进肿瘤发生后,今年四月,天津医科大学王艳教授课题组在 Science Advances 上再次发表文章,阐述了 PHF20L1 蛋白作为一个潜在的癌症治疗的靶点,能够通过作用于甲基化组蛋白 H3K27me2,促进乳房肿瘤发生。
此外,他们还发现 PHF20L1 是一种潜在的 MYC 和缺氧驱动癌基因,通过直接抑制 HIC1、KISS1 和 BRCA1 等肿瘤抑制因子,促进乳腺癌细胞的糖酵解、增殖和转移。并且 PHF20L1 的表达也与乳腺癌的高组织学分级密切相关,并在一些癌症中显著上调。同时,Phf20l1 基因缺失不仅诱导乳腺导管生长迟缓,而且抑制体内肿瘤的发生。以上数据表明,PHF20L1 能促进肿瘤的发生,可以作为一个潜在的癌症治疗的靶点。
作者首先使用组蛋白多肽微阵列(Histone peptide array)技术进行筛选。作者发现 GST 融合的 TUDOR 结构域与 H3K27me2 多肽结合很强,而 MBT 和 PHD 结构域没有结合位点。并且 TUDOR 结构域可以识别 H3K27me2 多肽,而不识别 H3K27me2S28p,H3R26me2sK27me2S28p,H3R26me2aK27me2S28p 多肽。GST-TUDOR 不能结合含有 H3S28p 的 H3K27me2,说明结合被丝氨酸磷酸化(S28p)所抑制。生物素化组蛋白多肽与 GST 或 FLAG 融合的 PHF20L1 全长或截短版突变的 pull-down assay,进一步证实了多肽微阵列的筛选结果。
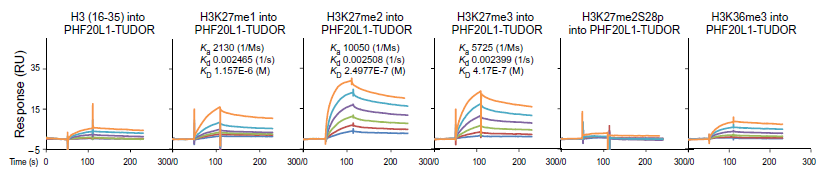
为了进一步研究 TUDOR 结构域与 H3K27me2 的结合,作者使用 Biacore 实验进行亲和力的精确定量研究(图 3 所示)。最终, Biacore 检测结果表明 PHF20L1 TUDOR 结构域与 H3K27me2 多肽亲和力为 0.25 μM,明显高于其它修饰多肽的亲和力。而 S28p 不结合 TUDOR 也证实了之前丝氨酸磷酸化抑制结合的猜想。而高灵敏、高分辨率的 Biacore 系统,能够精确区分不同样品间亲和力的细微差异,从而精确的阐释不同蛋白修饰对功能的影响。
而具体到定量表征分子间互作的亲和力的差异(蛋白识别不同的甲基化/磷酸化修饰)还是需要高灵敏度与高分辨率的 Biacore 来完成。
另外,由于 Biacore 8K Serie 的超高检测通量,相信很多筛选的工作(Histone peptide array,pull-down assay)都可以通过 Biacore 来轻松实现,这不仅能克服传统实验方法通量低、需要标记的缺点,更能节约大量人力物力,实现筛选-表征一站式互作分析。


 收藏
收藏 询价
询价