FDA:基于SPR建立流感中和抗体筛选的方法

图1:FDA发表文章截图
01
结合特异性与芯片表面的稳定性
研究人员在SA芯片的Fc1上固定α2,8唾液酸受体类似物作为阴性对照,Fc2上固定Glycan 3′SLN-PAA-biotin (α2,3唾液酸受体类似物,特异性结合H1凝集素),Fc3上固定Glycan 3′SLN-PAA-biotin (α2,6唾液酸受体类似物,特异性结合H5凝集素)。
Biacore实验结果验证了这种结合的特异性,如图2a所示,NR-44074(H1亚型凝集素)特异性结合于Fc2的α2,6唾液酸受体类似物,与其他通道固定的唾液酸受体类似物没有结合 (α2,3/α2,8) ,并且结合的响应值与NR-44074的浓度呈线性相关(图2b)。
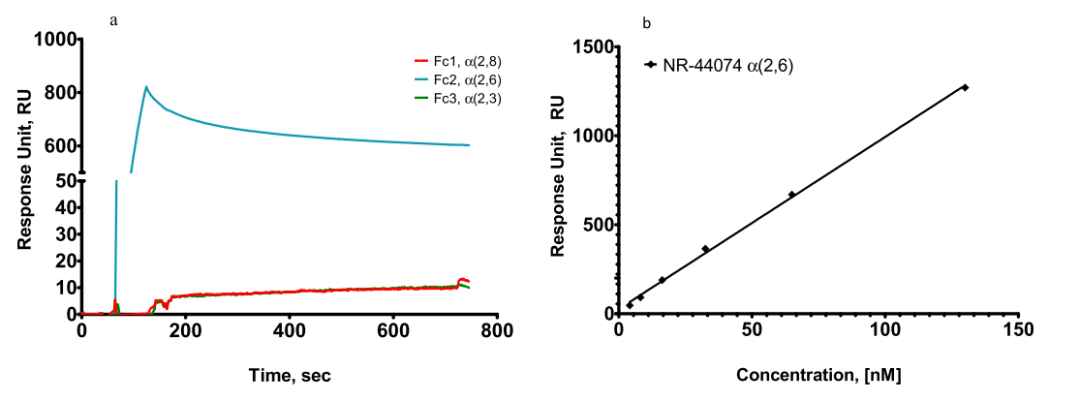
图2:NR-44074特异性结合α2,6唾液酸受体
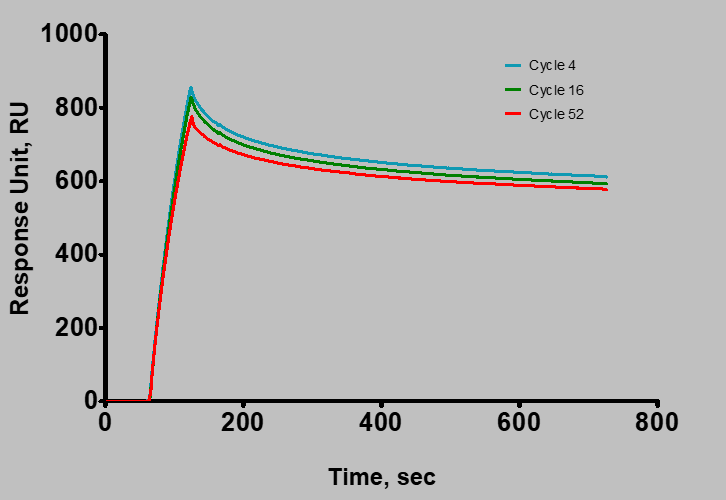
图3:评估芯片表面稳定性
02
单克隆抗体和免疫血清抑制能力
如图4a所示,纯化的小鼠腹水来源针对H1的单克隆抗体NR-28666按照1:8000稀释之后完全抑制了H1凝集素与α2,6唾液酸受体的结合(图4a,红色传感线)。使用感染H1N1的动物抗血清也得到了相似的结果(图4a,绿色传感线),只是抑制效率不如单克隆抗体。作为阴性对照的Anti-H5单克隆抗体2728未展现出这一抑制作用(图4a,黑色传感线)
实验中还测试了WHO作为参照的针对每年流行的流感亚型的兔抗血清,结果显示只有anti-H1-like A/California/07/2009的抗血清(图4b,红色传感线)表现出对A/California/07/2009 or A/California/04/2009 rHA结合的抑制,其他亚型的抗血清与H1凝集素预混后并未影响rHA的结合(图4b)。
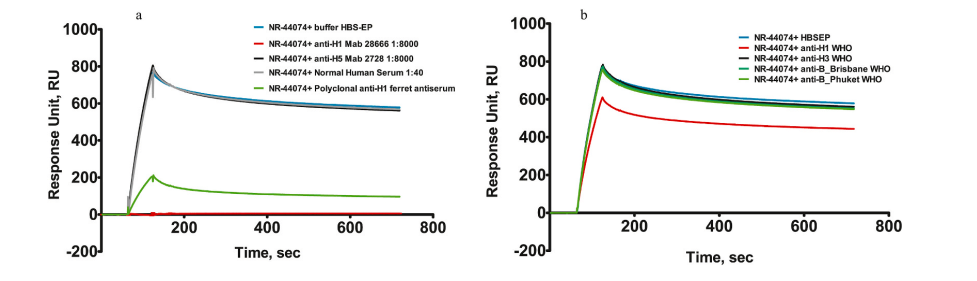
图4:单克隆抗体和免疫血清抑制能力实验
03
人血浆样品的抑制能力
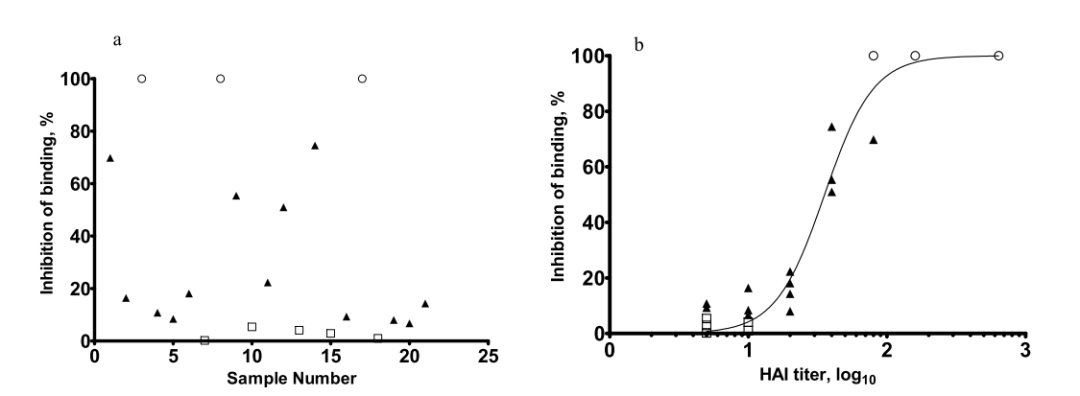
图5:血浆样品的Biacore抑制实验
04
抗体定量
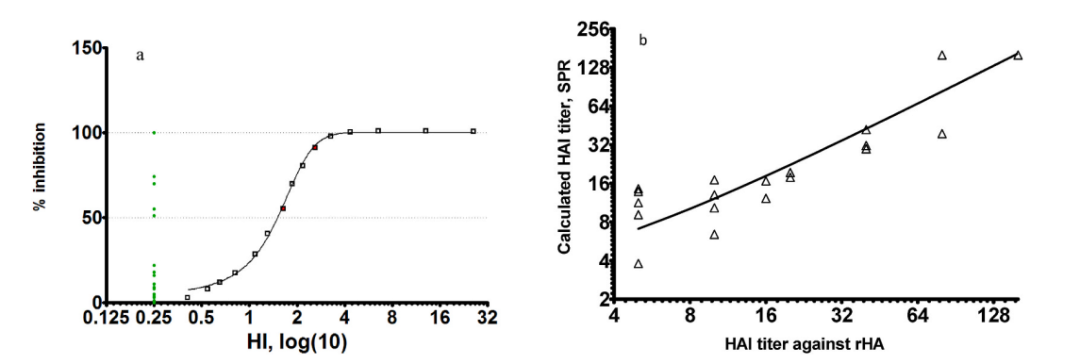
图6:Biacore竞争法检测抗体含量
05
不同IGIV产品中抗流感特异性抗体含量
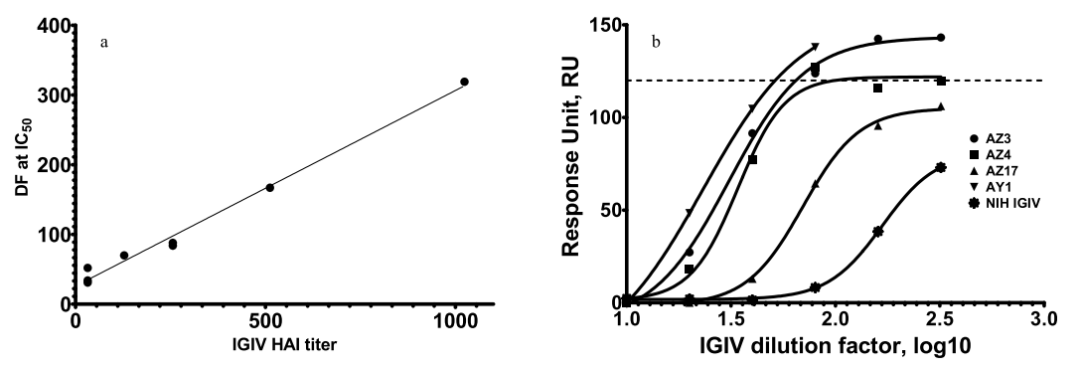
图7:SPR方法评估不同IGIV产品中流感抗体的含量
06
全病毒实验
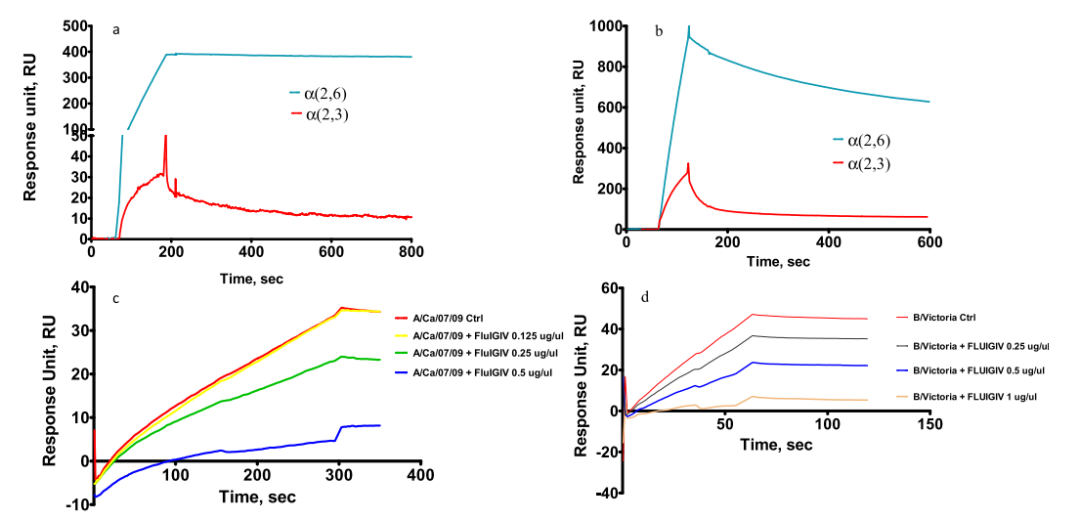
图8:流感病毒粒子的结合特异性及抑制实验
Biacore作为一种高通量,全自动的互作分析设备,与传统的HAI血凝抑制试验相比,能够快速从大量血浆/血清捐献者样品或者IGIV产品中筛选出含有高中和活性抗体的样本。在流行病环境下,采集高免疫血浆用于治疗或预防重症是非常重要的应对策略。
FDA生物制品评价与研究中心基于Biacore所建立的这一评估流感病毒中和抗体效力的方法,与传统HAI的结果显著相关,Biacore的高数据质量和实验的稳定性保证了最终结果的可靠性。这也显示了收录于中美日三国药典的SPR技术在治疗性抗体药物研发中的巨大潜力。

 收藏
收藏 询价
询价