双抗ADC破局免疫逃逸,临床前数据引爆期待
然而,在临床实践中,ADC药物仍面临两大核心挑战:耐药性和治疗窗口窄。前者让初始有效的药物最终失效,后者则限制了给药剂量,使得疗效难以进一步提升。
2025年8月,映恩生物的研发人员就基于以上背景开发出了名为DB-1419的新型双抗ADC。并在国际期刊Clinical Cancer Research上发表题为“Preclinical evaluation of DB-1419, a novel bifunctional and bispecific anti-B7-H3/PD-L1 antibody-drug conjugate”的研究论文,详细阐述了DB-1419的设计以及临床前研究数据,为ADC疗法的未来发展提供了重要参考。
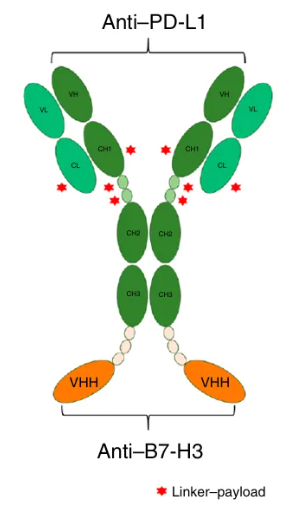
首先研究人员就对DB-1419进行了全方位的质量评估,包括结合特异性、亲和力、血浆稳定性,以及药代动力学特征等。在这其中,就用到了Biacore从分子水平上直接验证双抗ADC是否可以精准的识别并准确结合在靶点上以及结合的强度如何。
作者选择了使用Human Antibody Capture Kit与CM5芯片搭配使用,制作了一张捕获芯片,将DB-1419捕获到传感芯片上,然后以人和食蟹猴的B7-H3和PD-L1作为分析物依次流过芯片表面进行特异性及亲和力动力学的检测。
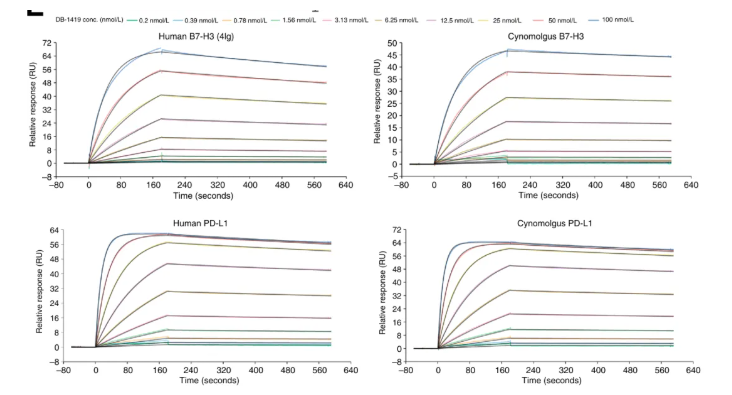
Biacore的检测结果表明,DB-1419对食蟹猴和人B7-H3和PD-L1具有强结合,亲和力分别为1.51×10-9;7.31×10-10;3.07×10-10;2.36×10-10(如图2所示)。
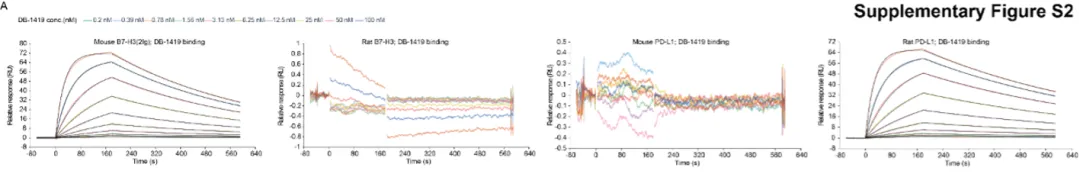
食蟹猴的B7-H3和PD-L1的物种交叉反应性
综上所述,DB-1419凭借其“化疗+免疫”双管齐下的创新设计,在临床前研究中展现了卓越的抗肿瘤活性、良好的药代动力学特性和可控的安全性。它不仅是一款药物,更代表了新一代ADC药物的发展方向。

 收藏
收藏 询价
询价