“多”用途,“肽”给力——Biacore 在多肽药物开发中的应用
多肽通常指不超过 100 个氨基酸构成的肽链。多肽药物集合了化学药物和蛋白类药物的优点,如分子量小、免疫原性低、生物活性高等,成为 21 世纪极具发展前途的药物。
目前,已有多款多肽药物获批上市,如胰岛素、生长激素、依特卡肽等。Biacore 作为中美日药典收录的分子互作技术,已广泛应用于多肽药物的筛选、机理研究、长效化、免疫原性和质控放行等环节,为诸多多肽药物开发提供了关键数据。
01. 多肽药物筛选
Biacore 进行多肽药物筛选的原理主要基于动力学数据,其中 ka 反映药物与蛋白的结合快慢,kd 反映药物结合靶标的稳定性,KD 反映药物与蛋白的亲和强弱。Biacore 可以快速精准的对多肽分子进行筛选和排序,从中筛选出亲和力高、解离慢的进行进一步开发。
例如:
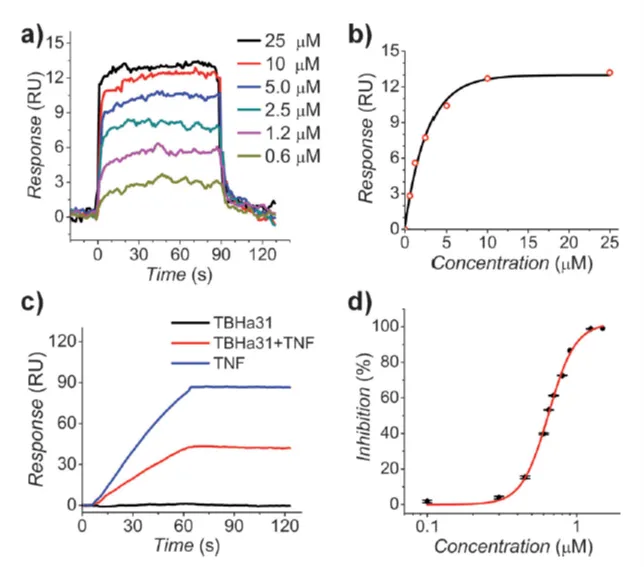
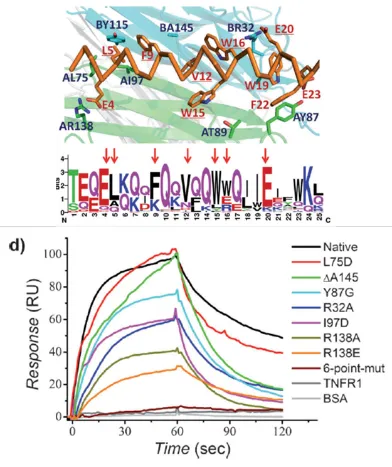
北京大学来鲁华教授课题组针对肿瘤坏死因子 TNF-α 进行了多肽设计计算,然后将 TNF-α 固定在传感芯片表面,基于 Biacore 完成了多肽的结合活性测定,最终筛选到了 TBHa31 这一高亲和多肽。
研究人员还基于 Biacore 设计完成了多肽的竞争实验,证实了 TBHa31 可以阻断 TNF-α 和 TNFR 的结合。作者还对 TNF-α 进行了部分位点突变,发现突变后亲和力有明显降低甚至消失,进一步证实 TBHa31 的结合靶点就是 TNF-α。
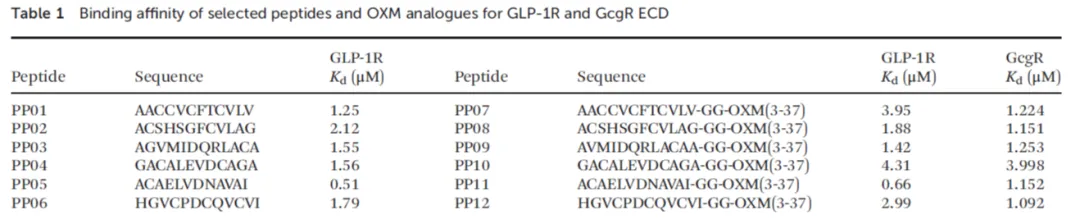
2019 年,华北理工大学附属医院利用 Biacore 技术完成了降糖多肽的筛选。前期研究发现胃泌酸调节素 OXM 是一个有降糖作用的 37 肽,但其半衰期太短。于是作者设计了一系列的 12 肽 GLP-1 激动剂接到 OXM 上,最终基于 Biacore 结果筛选到了 PP11 作为基础进行脂肪酸链修饰以延长半衰期,并取得了不错的临床效果。
02. 多肽药物机理研究
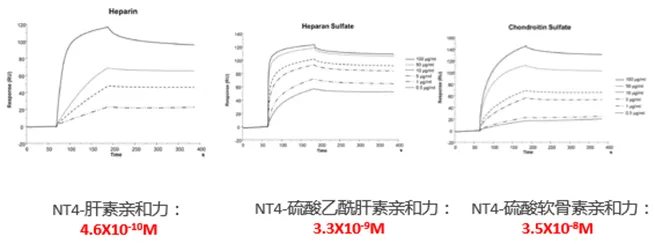
为了阐明 NT4 的作用机制,研究人员将 NT4 多肽固定到芯片表面,不同类型的 GAG 聚糖(肝素、硫酸乙酰肝素、硫酸软骨素)依次流过芯片表面进行亲和力测定。
Biacore 结果表明肝素、硫酸乙酰肝素、硫酸软骨素均能与 NT4 直接相互作用,并且亲和力达到 nM 级别,提示 NT4 多肽具有很好的药物开发潜力。同时 NT4 与不同 GAG 之间结合的亲和力相差 1-2 个数量级,具有显著的选择性,这可能是 NT4 针对不同肿瘤治疗效果差异的分子基础。
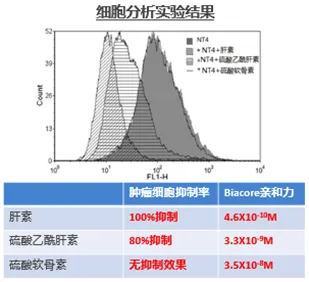
结合细胞实验数据,研究人员比较了 NT4 对肿瘤细胞的抑制效果。NT4 与 GAG 的亲和力越高,抑制效果越好,当亲和力低至 10-8M 后,无抑制效果。
这篇文章中,Biacore 提供了直接的、定量的分子水平相互作用数据,帮助科研人员确证相互作用的发生机制和对象,与细胞实验结果具有很好的一致性。所以 Biacore 可以作为细胞实验前的高通量药物筛选工具,无需细胞培养,节省大量的时间人力成本。
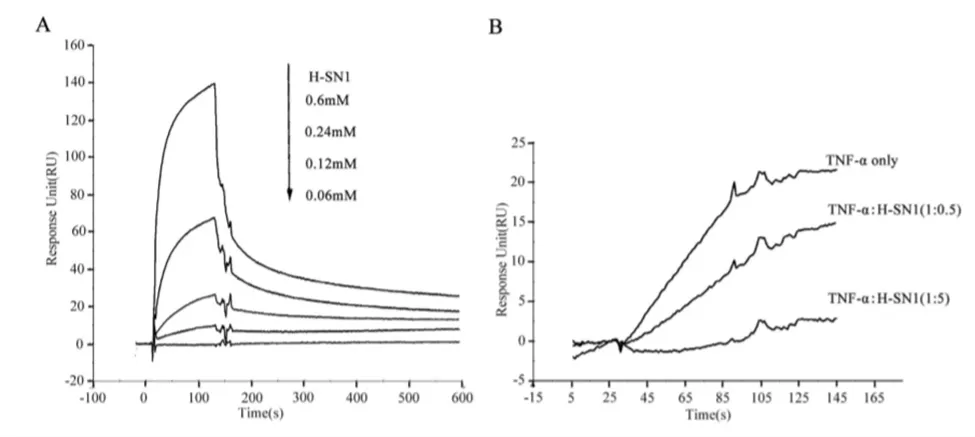
蛇毒含有丰富的活性肽, 具有抗炎和免疫调节作用,但其抗炎活性成分及作用机理尚未明确。第二军医大学通过噬菌体展示技术从蛇毒中筛选得到了 Hydrostatin-SN1 这一天然多肽,采用 Biacore 阐明了该多肽能够特异性地结合 TNFR1(KD = 32μM),且 Hydrostatin-SN1 能够剂量依赖性阻断 TNF-α 与该受体的结合,从而发挥抗炎作用。
03. 多肽药物长效化
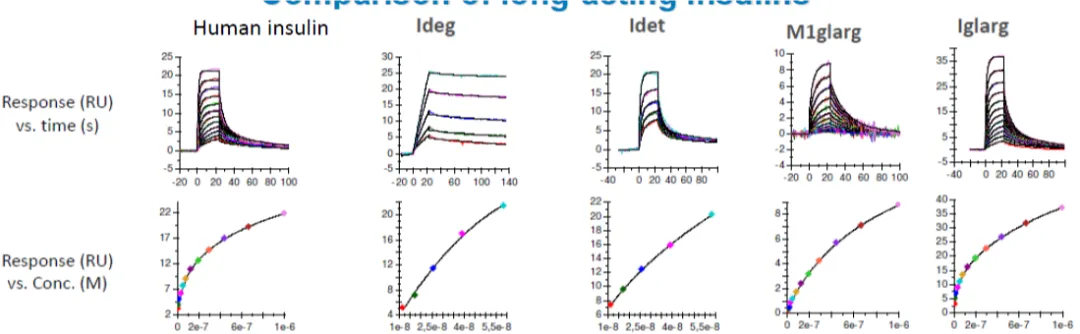
目前,赛诺菲、诺和诺德、甘李、通化东宝等国内外胰岛素生产企业巨头纷纷采用 Biacore 进行胰岛素类似物的开发和质控,涵盖了胰岛素、德谷胰岛素、地特胰岛素、甘精胰岛素等从第一代到第四代全部的胰岛素产品。
半衰期短是多肽药物面临的一大痛点。同济大学开发了一种治疗糖尿病的新型多肽,这种经过改造的 GLP-1 类似物能高亲和地结合白蛋白,免受肾脏滤过和蛋白酶降解,从而有效延长了药物在体内的半衰期。
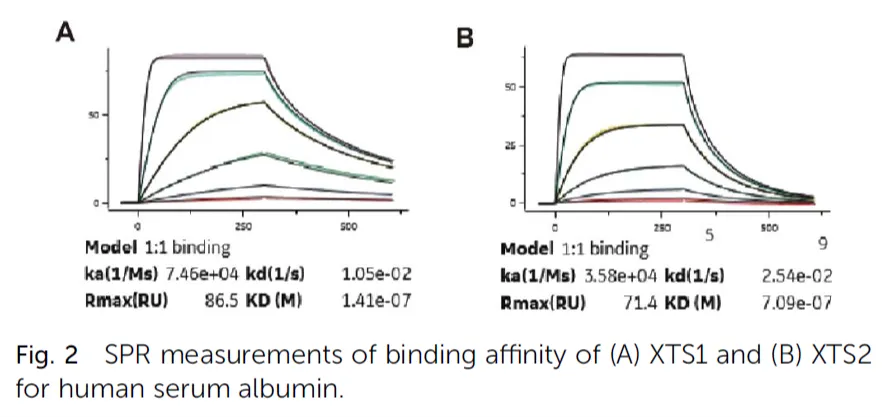
该设计是在 GLP-1 上通过一个可被凝血酶切割的 linker 连接了由 39 个氨基酸组成的白蛋白结合域,而延长半衰期的关键就是提高多肽与白蛋白之间的亲和力。在此过程中,研究人员用 Biacore 验证了其构建的 XTS1/2 与不同种属的白蛋白之间的亲和力。
结果显示 XTS1 与白蛋白的亲和力高于 XTS2,预测 XTS1 在体内也有更长的存留时间。后续的动物实验也表明,XTS1 比利拉鲁肽有更好的结果。
除了利用与白蛋白的结合延长半衰期外,PEG 化也是一种经典的延长多肽半衰期的方法。但 PEG 的分子量比较高,多肽在 PEG 化后有可能影响其与相应受体的结合。因此,准确检测多肽 PEG 化前后与受体结合活性的变化对于其药效的发挥至关重要。
目前,辉瑞和金赛药业在长效生长激素的开发中,也都使用了 Biacore 去检测 PEG 化前后对生长激素与受体结合的影响。并且该方法已经成为行业内的放行标准,用于不同 PEG 化多肽产品的批次放行。
04. 免疫原性
药物在体内会引起免疫应答,轻则中和药效,重则引起不良反应。免疫原性涉及药物的安全性和有效性,因此 FDA、EMA 等法规均将药物免疫原性列为强制性要求的检测项目。免疫原性包括抗药抗体 (ADA) 的筛选、验证、分型与中和活性检测。
- 在 2020 中国药典中,已将 Biacore 基于的 SPR 技术列为了免疫原性检测技术。
- 在 FDA 免疫原性指导原则中,将 SPR 技术与 ELISA、RIPA 一同列为了推荐的三种筛选方法。
- 在 EMA 对免疫原性检测的指导原则中,详细阐释了 SPR 技术进行免疫原性检测的优势:SPR 是一种实时检测技术,能够检测快速解离的抗药抗体,这些 ADA 可能无法被其他方法检测到,因为 ELISA 基于的桥联法可能会在检测过程中丢失信号,并且 Biacore 也比 ELISA 方法更耐受药物分子干扰。
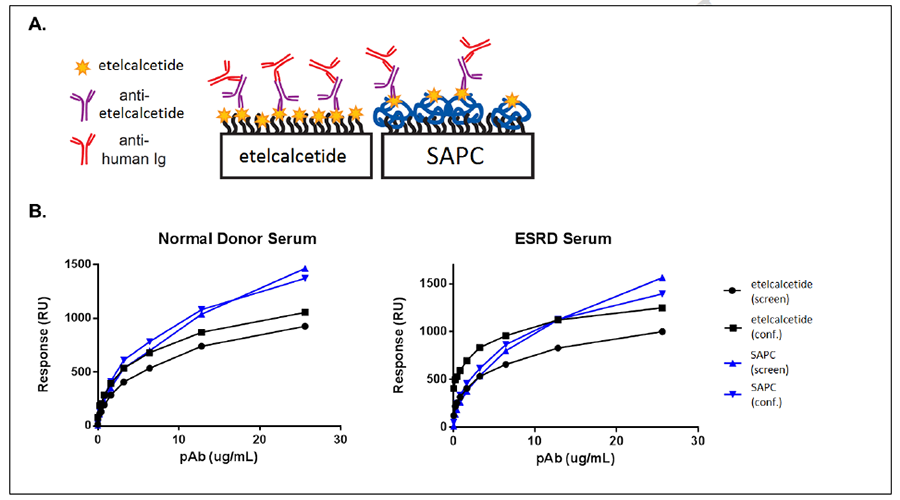
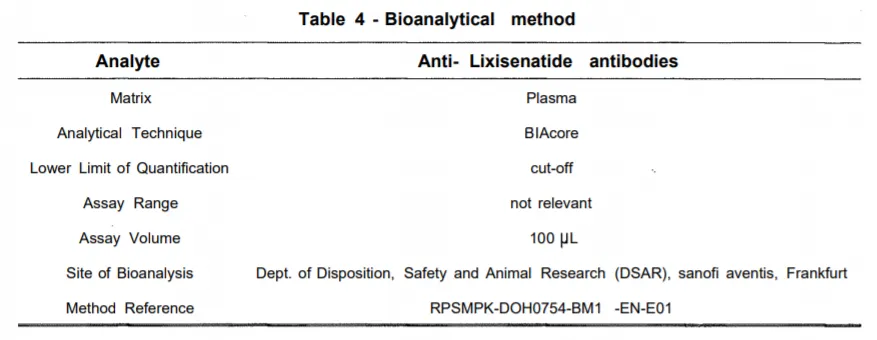
因此,Amgen 公司的依特卡肽、赛诺菲公司的利西拉肽等上市多肽药物均基于 Biacore 完成了免疫原性数据申报,结果证实了 Biacore 抗药性抗体检出率高的优势。

1. Angewandte Chemie, 2013, 52(42): 11059-11062.
2. Organic & biomolecular chemistry, 2019, 17(33): 7760-7771.
3. International journal of molecular sciences, 2016, 17(11): 1940.
4. Scientific reports, 2016, 6(1): 27174.
5. Scientific reports, 2016, 6(1): 1-13.
6. RSC Advances, 2019, 9(53): 30707-30714.
7. Xenobiotica, 2008, 38(10): 1340-1351.
8. Journal of immunological methods, 2017, 445: 37-44.
9. Diabetes care, 2013, 36(9): 2543-2550.

 收藏
收藏 询价
询价