诺奖团队+国内科研新成果见证实力!AI+SPR近期文章盘点
治疗性蛋白靶点大环肽配体的开发通常依赖于大规模筛选方法,这些方法资源消耗大且难以控制结合模式。尽管基于物理的肽设计方法和深度学习的蛋白质设计技术已取得显著进展,但目前仍缺乏可靠的蛋白质结合大环肽从头设计方法。
继去年开发了一种能从头设计生成全新蛋白质的人工智能算法:RFdiffusion后,诺奖得主David Baker实验室在Nature Chemical Biology上发布的RFpeptides——一种基于去噪扩散模型的流程【1】,可用于针对目标蛋白质设计大环肽配体。在四种不同蛋白靶点上分别测试了10-20个设计的大环肽,成功获得了所有选定靶标的中等至高亲和力配体。
相关阅读:
RFpeptides用来设计结合靶蛋白的环肽骨架;ProteinMPNN或LigandMPNN生成序列;RoseTTAFold2(RF2)、AfCycDesign(AFC)预测环肽-靶蛋白复合物结构,打分进行虚拟筛选(图1)。
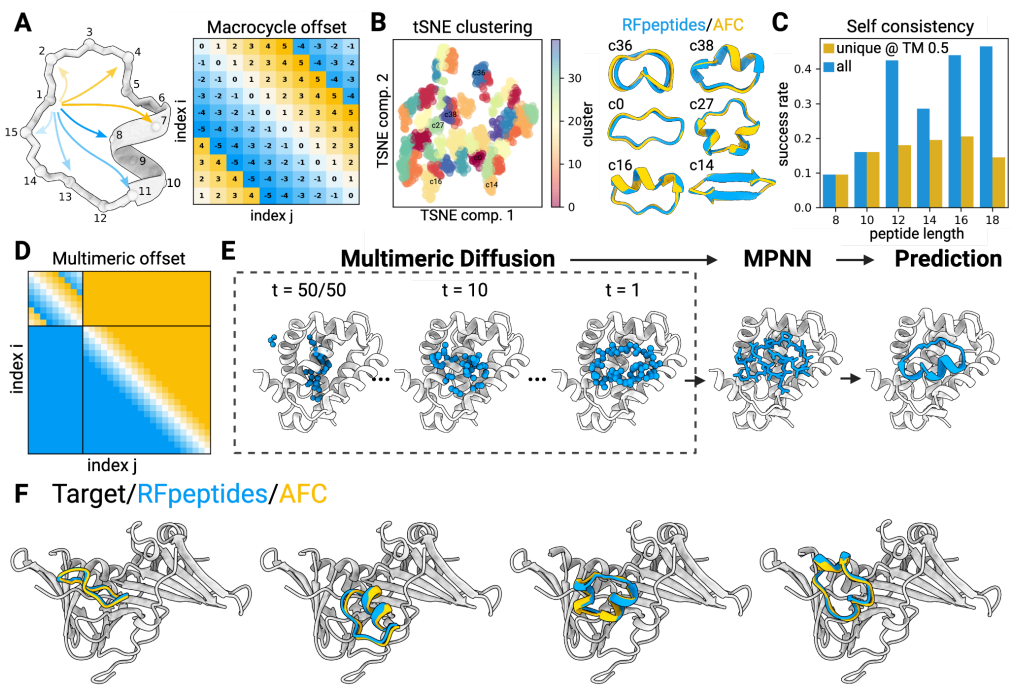
亲和力测定(验证)实验使用SPR技术(Biacore 8K),通过Biotin Capture Kit固定生物素化的目标蛋白。结合筛选阶段使用单循环动力学(SCK),10 nM,100 nM,1 μM,10 μM,100 μM连续进样5个浓度,结合60秒,解离120-150秒。测定成功设计的亲和力阶段,使用单循环动力学连续进样9个浓度,2-5倍稀释。兼顾了效率与数据质量。
以MCL1为靶蛋白,设计出9965个骨架,每个骨架4个序列,虚拟筛选后合成了27个大环肽。通过SPR筛选,验证大环肽和MCL1的互作,得到D2、D26。最终测定大环肽D2和MCL1亲和力为2 μM。
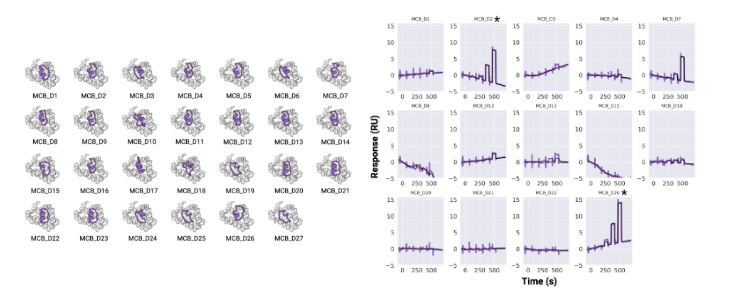
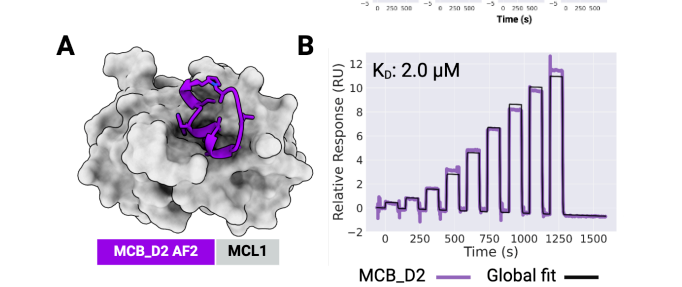
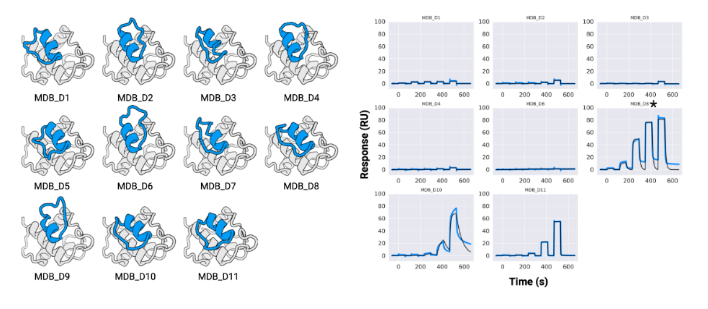
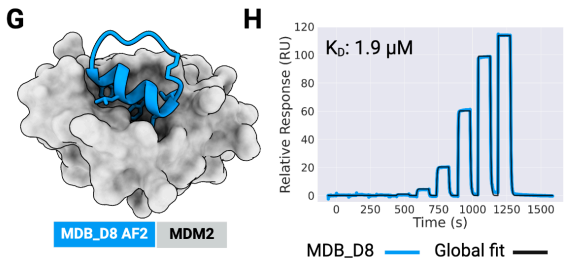
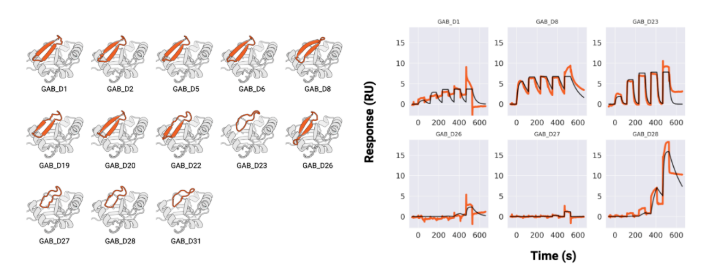
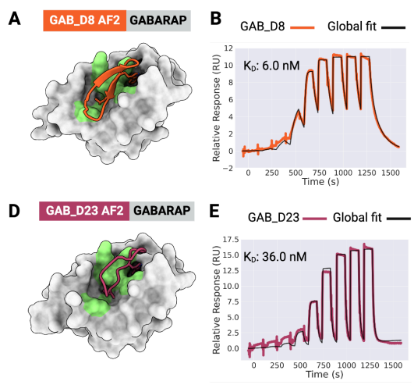
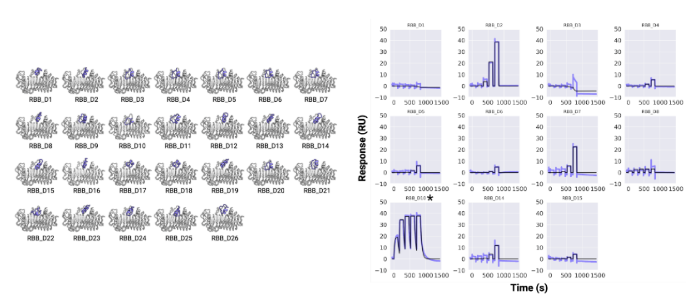
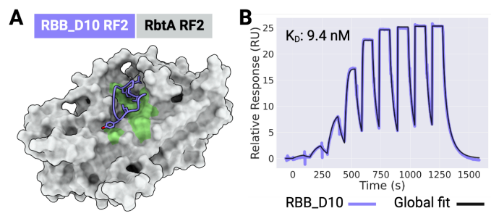
大环肽与MCL1、GABARAP和RbtA复合物的X射线晶体结构显示,其与计算设计模型高度吻合。与文库筛选方法中结合模式确定常成为主要瓶颈相比,RFpeptides生成的大环化合物结合模式可通过设计预知,这将极大促进下游优化进程。因此,RFpeptides为诊断治疗用大环肽的快速定制化设计提供了强大框架。
2025年6月10日,北大-清华生命科学联合中心/北京大学生物医学前沿创新中心/昌平实验室曹云龙团队联合中国科学院生物物理研究所王祥喜团队、美国Moderna公司Laura M. Walker团队在Nature Microbiology上发表论文【2】,提出了针对流行的高频突变病毒,通过预测病毒进化热点,快速准确筛选出广谱中和抗体的策略。发现了来自原始株康复者的广谱中和抗体BD55-1205,该抗体不但能中和所有现存的SARS-CoV-2突变株,与相同表位的其他抗体相比还对表位上的逃逸突变具有很强的抵抗能力,具有开发为新一代SARS-CoV-2广谱中和抗体药物的潜力。
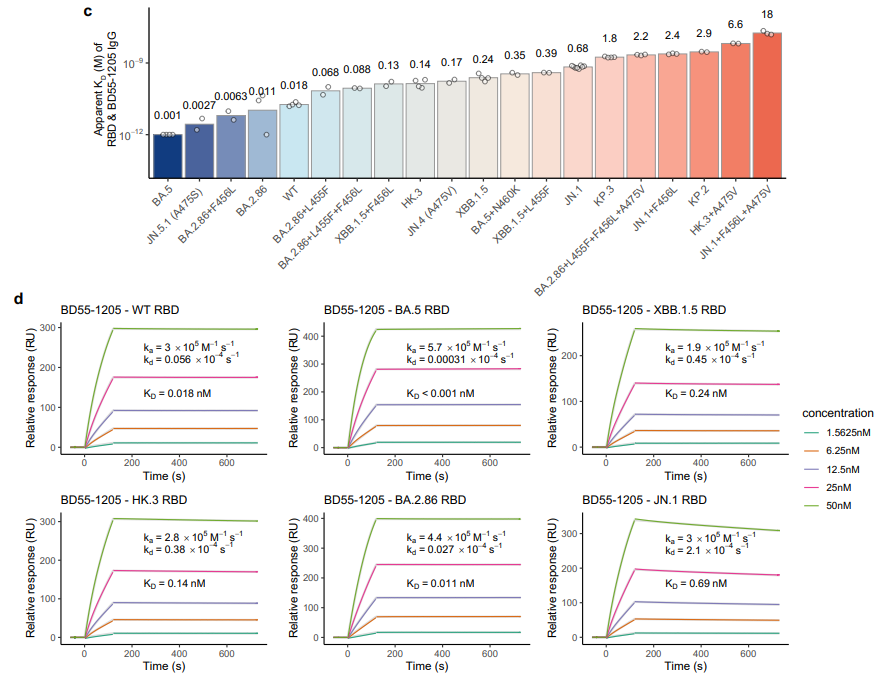
Biacore 8K(SPR)实验(ProA-mAb-RBD)表明BD55-1205 IgG对RBD各种突变显示出高亲和力,范围为1 pM至18 nM,符合其对表位突变的兼容性(图6)。
2025年6月,中国科学院微生物研究所吴边研究员团队联合高福院士团队在National Science Review杂志在线发表研究成果【3】。该研究从蛋白质折叠与互作在分子层面的一致性出发,利用多任务学习和自蒸馏策略,开发了基于结构的图神经网络模型Pythia-PPI,实现了对单点突变引起的结合自由能变化(ΔΔG)的可靠预测。相较于传统物理能量函数,Pythia-PPI在预测精度、计算效率及使用便捷性方面均展现出显著优势,为蛋白质相互作用突变效应的定量预测与蛋白理性设计提供了有效工具。
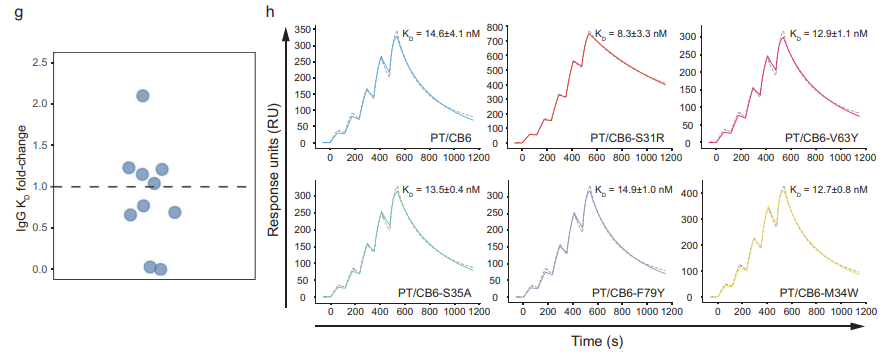
为验证Pythia-PPI的应用价值,研究团队以靶向SARS-CoV-2 PT RBD的CB6抗体为研究对象,从模型预测结果中筛选出前10个可能增强亲和力的单点突变,并通过Biacore 8K(SPR)实验进行验证(ProA-CB6-RBD)。结果显示(图7),V63Y、S35A等突变体表现出稳定的亲和力提升,其中S31R突变体与RBD的结合能力提升超过两倍,充分验证了模型在突变筛选与实验指导中的可靠性与实用性。

 收藏
收藏 询价
询价