Cell文章优选芯片:特异性捕获&牢固偶联兼得,且看Biacore NTA
Cell文章优选芯片:特异性捕获&牢固偶联兼得,且看Biacore NTA
1
串联法 (Tandem)
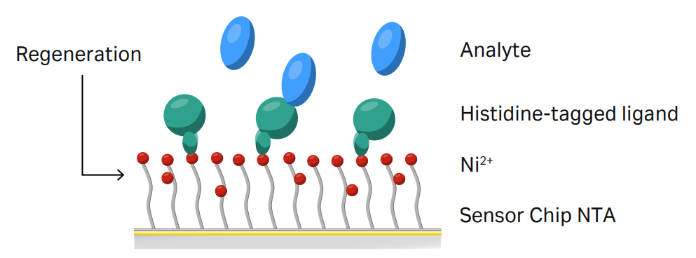
图1:抗原表位分析的实验方法示意图a夹心法、b预混法、c串联法
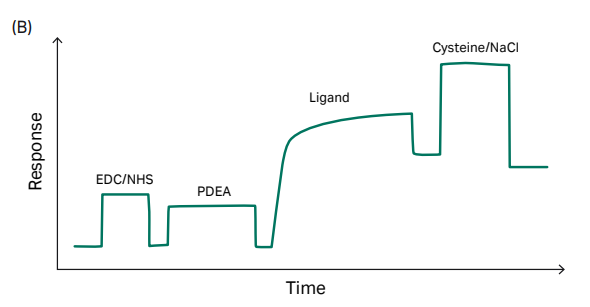
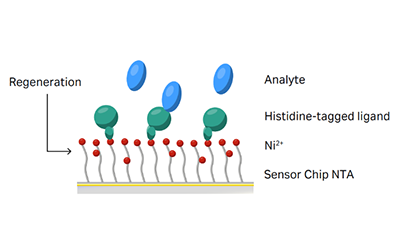
- General:芯片表面螯合Ni2+;
- Capture:捕获His标签配体 (Ligand in running buffer) ;
- Analyte:进样分析物,检测与配体的结合和解离过程。单循环实验中,可以在此步设置中一个循环设置多个浓度,直接得到浓度梯度的结果;
- Regeneration:用EDTA洗去Ni2+及配体。
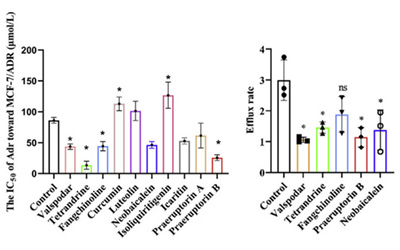
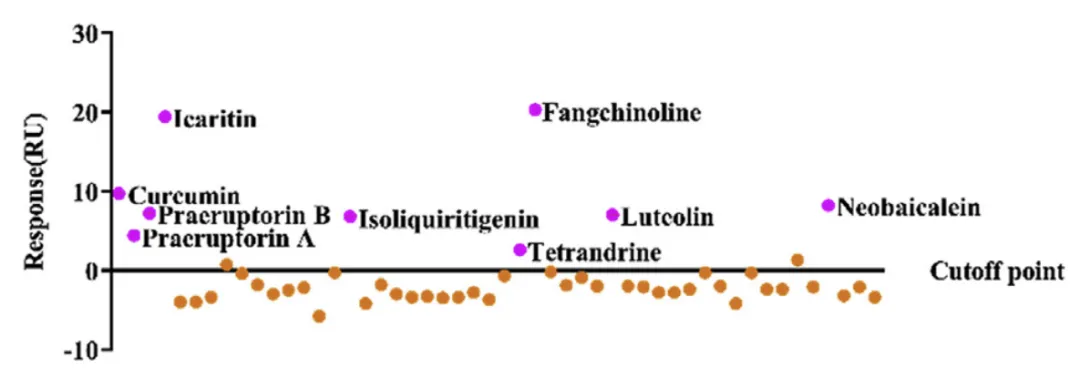
熟悉His标签的老师可能会问:必须用EDTA再生么?当然不是。Kong et al. 使用NTA捕获法检测14–3-3ζ蛋白与化合物的结合时,化合物与靶点蛋白可以完全自发解离(快解离),因此不设置再生[1];Lu et al. 使用NTA捕获法检测膜蛋白A2AR与化合物的结合,使用5 mM theophylline再生洗掉分析物而保留配体[2]。
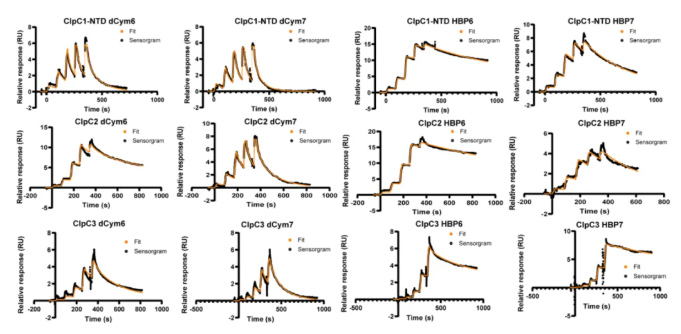
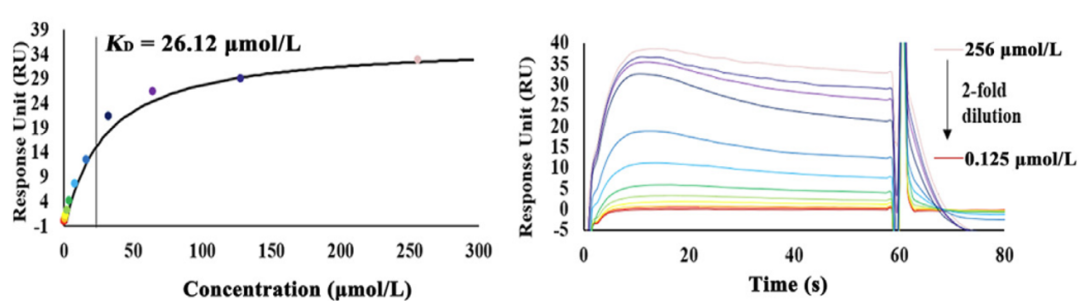
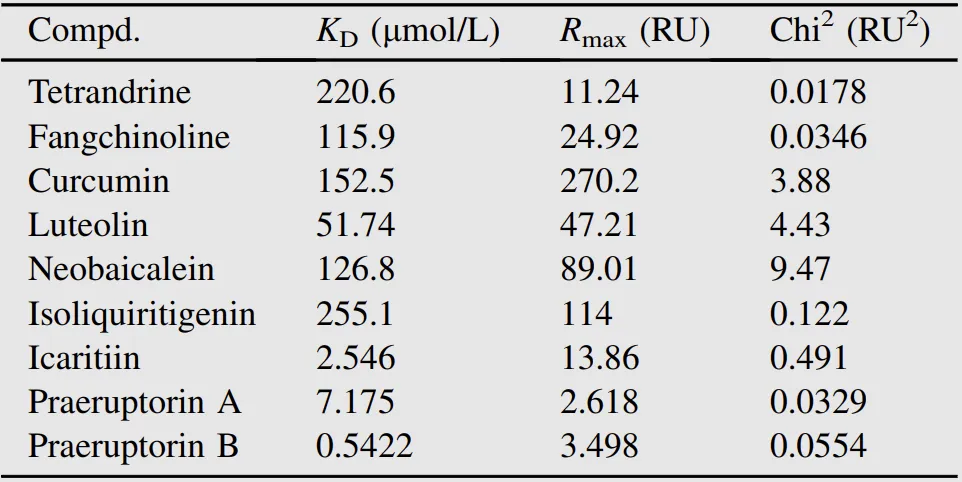
图2:NTA芯片Capture & Coupling后,单循环检测ClpC3与药物的亲和力
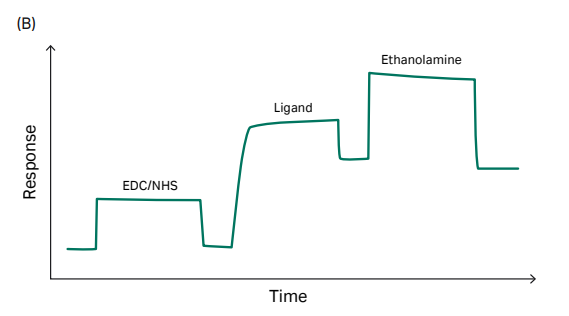
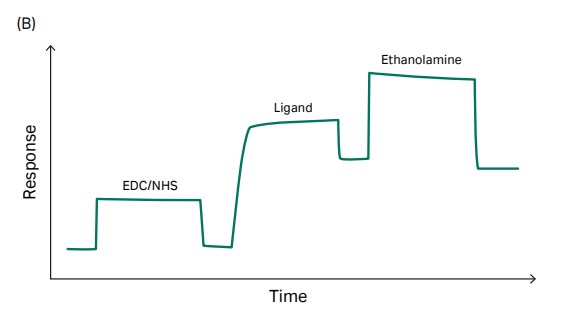
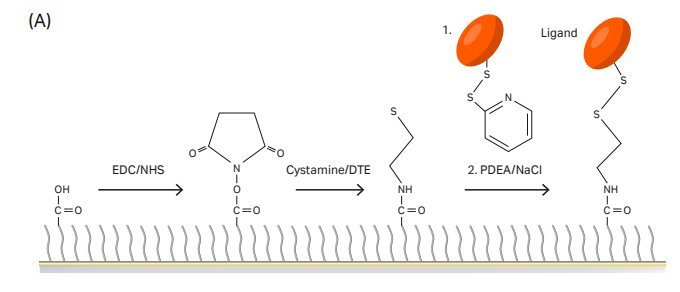
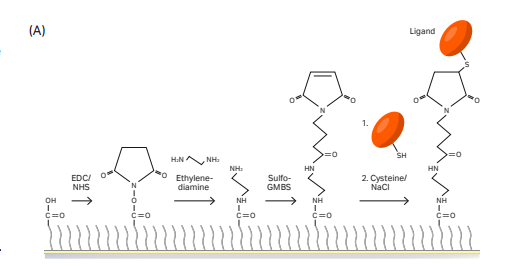
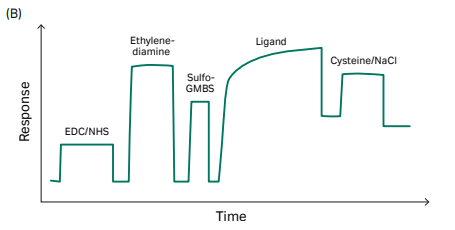
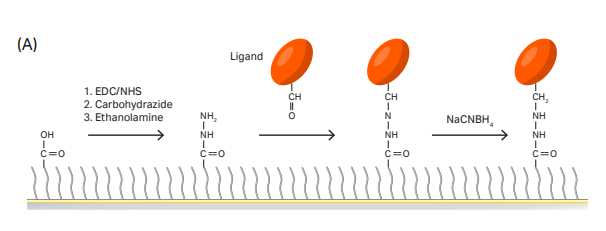
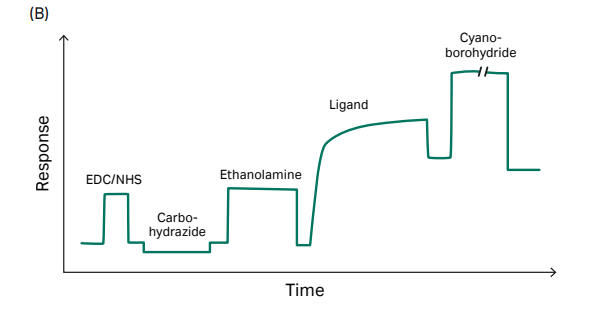
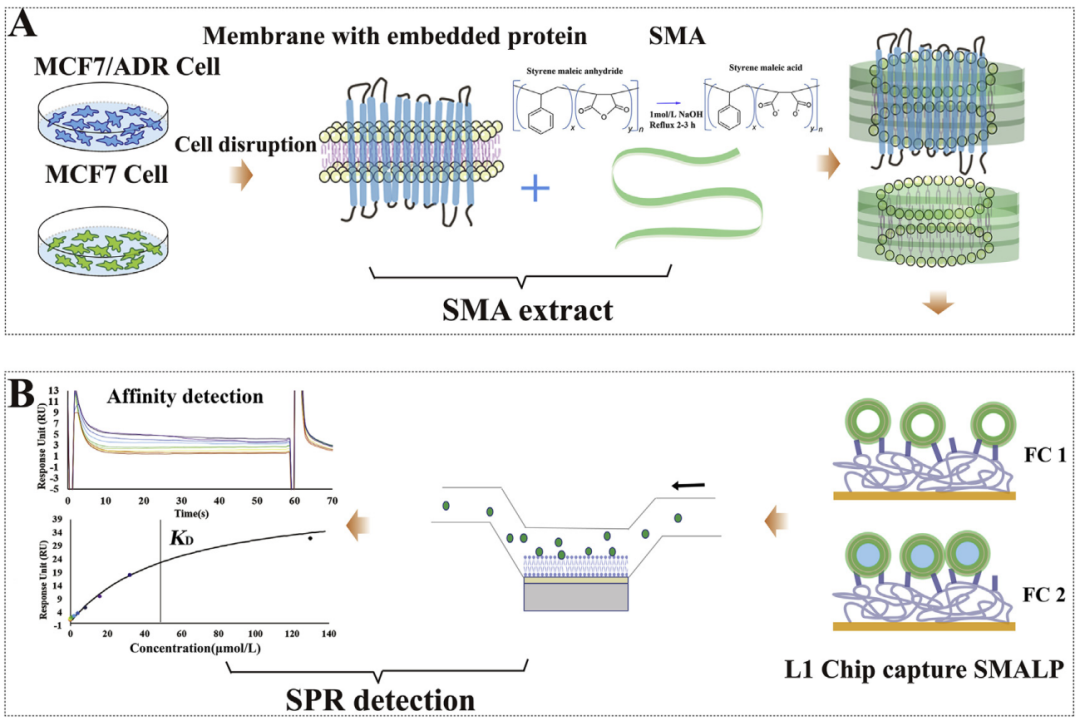
“捕获”+“偶联”可使His标签配体蛋白稳定地共价结合在芯片。区别于CM系列芯片,NTA芯片并不通过静电吸附达到富集的目的,而是利用Ni2+与His标签的特异性结合,所以配体分子不需要使用低pH的醋酸钠缓冲液,用运行缓冲液稀释即可。
在Biacore控制软件中选择Immobilization-芯片类型选择NTA-add step-NTA Amine(Insight software of 1 series and 8 series, X100、T200及S200可在偶联方法中自定义偶联方法)即可开展实验。具体实验流程包括:
- General:芯片表面螯合Ni2+;
- Activation:EDC/NHS活化;
- Capture:捕获His标签配体 (Ligand in running buffer) ,同时发生捕获和偶联。除了设置配体进样时间外,Biacore特有的Aim for target level模式,无需紧盯偶联信号,不用担心偶联多了、少了,只需要输入想要的偶联量,仪器自动调整进样时间,准确达到目标偶联量。精准偶联So Easy;
- Deactivation 1:乙醇胺封闭;
- Deactivation 2:用EDTA洗去Ni2+。
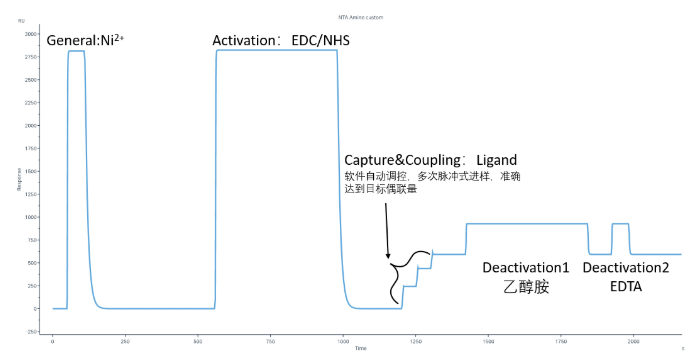
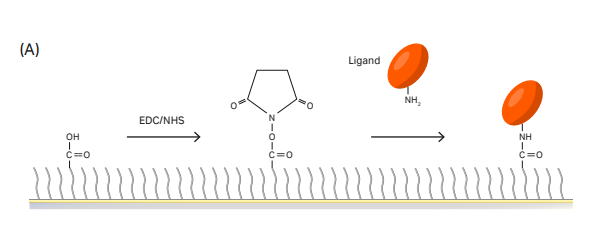
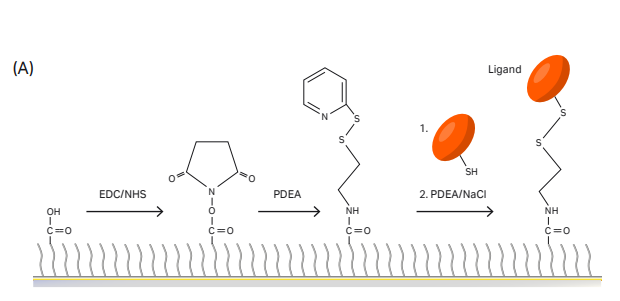
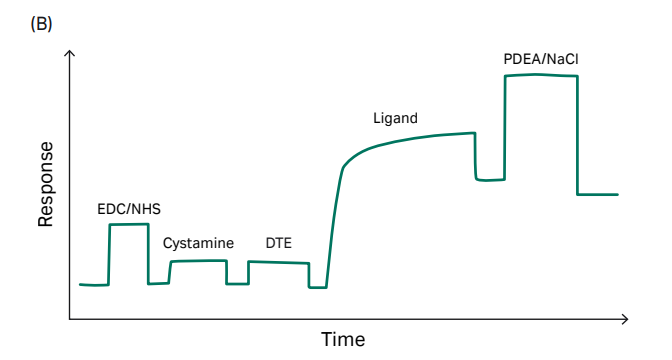
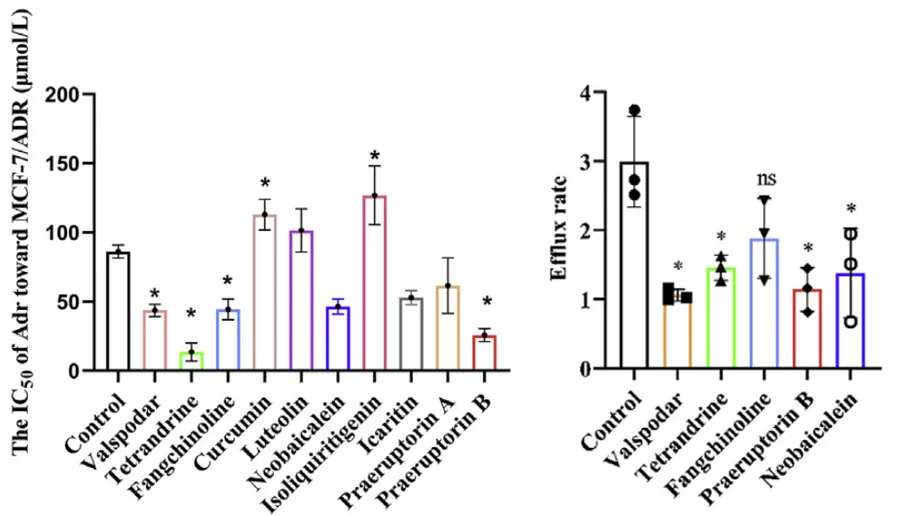
图3:NTA芯片捕获+直接偶联,target模式下自动完成目标偶联量
在夹心法和串联法中,也可以同时在第二步进有A抗体背景的B抗体(二者的混合物)3来规避掉A抗体与抗原的解离。

 收藏
收藏 询价
询价