生物过滤工艺整体解决方案:高浓制剂工艺难点攻坚!
什么是高浓制剂?
为何要引入高浓制剂?
高浓制剂,就是药物有效成分在一定体积溶液中浓度较高的制剂形式。它的出现,主要是为了解决患者需要频繁用药的问题,通过提高药物浓度,减少注射频次,提升给药效率,从而提高患者的依从性。同时,在一些大分子生物药物中,由于剂量需求较大,传统制剂形式难以满足临床需求,高浓度制剂应运而生。
通常这类液体粘度在10-50 cp,浓度大于100 mg/ml,甚至高达250 mg/ml。生物技术药物通过高浓度制剂给药时,常以皮下注射的方式替代静脉注射治疗自行给药,为患者带来生活方式的益处且可降低医疗成本。

目前,美国食品药品监督管理局(FDA)批准的单抗产品中,有超过20%属于高浓度制剂。然而,高浓度制剂的开发和生产过程仍面临诸多技术挑战,如高粘度和易形成蛋白聚体等问题,增加生产工艺开发的复杂度、降低药品稳定性并增加免疫原性风险。
高浓制剂的挑战和应对方法
高浓度制剂需要经过两个主要工艺过程,分别为UF/DF和除菌。
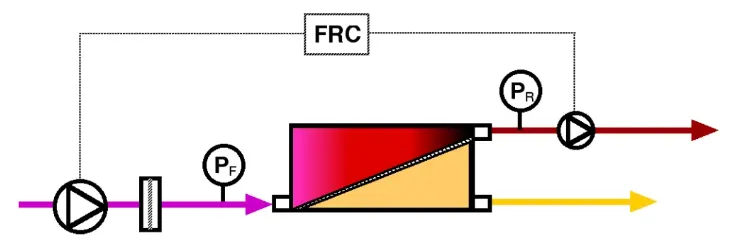
超滤/洗滤(UF/DF)步骤在高浓度抗体制剂的生产中起着关键作用。该步骤位于典型纯化工艺流程的末端,将目的产物浓缩至其目标值并将其置换到所需的制剂缓冲液中。满足药物制剂最终赋形剂浓度目标或规格对于通过匹配生理渗透条件以确保患者安全给药,同时保持药物功效和延长保质期至关重要。
为了实现这些结果,有必要克服高浓度药物底物生产中遇到的几个主要障碍,包括UF/DF过程中的赋形剂漂移、压力降限制、剪切和聚体的形成、以及收率和残留体积挑战。
超滤/洗滤应对策略
终端除菌过滤步骤在高浓度抗体制剂的生产中起着关键作用。该步骤位于典型纯化工艺流程的末端,将目的产物除菌过滤以去除料液中颗粒和微生物,满足药物制剂最终无菌要求以确保患者安全给药。高浓度蛋白的粘度通常很高,会造成除菌滤器的通量降低,过滤时间变长甚至产品损失增多。经典的膜结垢模型是孔隙收缩,孔隙堵塞和滤饼过滤。
除菌过滤优化策略
从工艺角度可以通过增加除菌滤器的面积来提高过滤通量,但是更大的滤器死体积,料液残留越多,可能会导致更多的收率损失,收率相应更低。高浓制剂推荐Prime过滤器。
相关阅读:

还可以在除菌滤器前增加预过滤器来提高除菌滤器的过滤通量;

可以在远离蛋白等电点的pH条件下进行除菌过滤,因为蛋白在等电点附近的自缔合最显著;

选择合适的除菌滤器也有助于提高过滤性能,如使用更亲水的滤器可以降低疏水性结垢和蛋白聚集;

可以用制剂缓冲液或蛋白溶液对滤器进行预处理,使结合位点达到饱和;

还可以采取缓冲液顶洗滤器的方法,尽可能降低蛋白在滤器中的残留,此时需要注意缓冲液顶洗体积,以免影响最终料液的蛋白浓度。

 收藏
收藏 询价
询价