从“一只狗”的肿瘤疫苗,看个体化mRNA癌症疫苗(PCV)真正的落地路径
近期“AI 救狗”,“宠物个体化mRNA肿瘤疫苗(PCV)”案例引发关注。AI在其中加速了肿瘤新抗原筛选与序列设计,使个体化方案成为可能;在这当中,除了关注AI 在加速新抗原识别与方案设计之外,也有一系列个体化肿瘤疫苗 (PCV)其他重要的突破:完整跑通了从测序、设计到 mRNA‑LNP制造与体内给药的工程流程。
这一案例揭示,PCV的核心不仅仅是算法,更是能否在极短时间内,稳定、可重复地完成小批量、多批次、符合GMP要求的生产与交付。宠物只是起点,真正的挑战,在于这套能力如何被复制、并最终走向人用治疗。
从宠物走向人类,个体化肿瘤疫苗(PCV)仍旧面临系列挑战:
mRNA序列设计
如何通过密码子优化、核苷酸修饰等技术,在增强mRNA稳定性和蛋白表达量的同时,又能最大限度地激发理想的免疫反应(特别是细胞免疫),这需要精细的平衡。
生产周期
与传统疫苗“批量生产、库存销售”的模式不同,个性化疫苗是“随需随制”。从获取肿瘤样本到最终产出疫苗,整个流程(测序、分析、制备、质检)必须压缩在数周内,对生产自动化、流程无缝衔接提出了极限要求。
供应链与成本
需要协调肿瘤样本的冷链运输、测序中心、生产中心和质量控制等多个可能分散的环节,管理极其复杂。单例样本制备难以规模化应用,导致成本高昂。
监管审批路径
从“批量审批”到“平台审批”的关键转变,CMC药学研究成为监管挑战的重中之重,针对个性化肿瘤疫苗监管路径的建立及完善的关键在于监管机构与产业界的紧密合作,共同建立一套基于风险、注重过程控制、灵活高效的新型监管框架,从而在确保患者安全的前提下,让这一革命性疗法早日惠及所需之人。
这些挑战,无法通过单点技术解决,而需要端到端的mRNA + LNP工艺平台支持。
正是在这一背景下,Cytiva针对PCV与个体化mRNA 疗法,构建了一套从DNA模板到LNP成品的完整解决方案并且推出了针对个体化疫苗的小体积符合GMP要求的多款新产品:
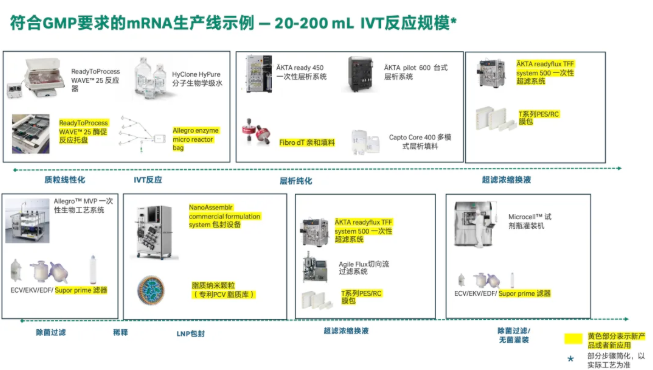
Part.1 – 个体化mRNA疗法要求制剂过程不仅高度可重复,还必须兼顾 合规、批次可追溯性和快速切换的生产节奏
NanoAssemblr商业化制剂系统正是为这一需求而设计:通过全封闭、自动化的一次性微流控制剂平台,在确保流量比精确控制和CQAs稳定的同时,满足21 CFR Part 11要求,并支持从临床到商业化的无缝放大。它使PCV的LNP制剂从“实验室工艺”真正转变为可规模化、可监管、可复制的生产能力。

NanoAssemblr Commercial Formulation System
Part.2 – 高效递送与精准的抗原递呈(Efficient Delivery & Antigen Presentation)
专有可电离脂质能够高效封装复杂的多表位 mRNA核心载荷。如下图所示:Cytiva专利的LNP平台不仅能实现高效率的递送与快速翻译(注射后数小时内即可观察到有效表达),还能促进多肽在MHC-I类分子上的成功递呈,从而精准激活免疫系统。


*体外测试了多表位mRNA,通过在JAWS II细胞中评估抗原呈递细胞(APC)的转染效率以及MHC I上的肽呈递情况。含有OVA表位肽SIINFEKL的多表位mRNA构建体,以及TriLink提供的全长OVA mRNA,均采用Cytiva自有的脂质纳米颗粒(LNP1)进行包封:(A)体外评估多表位mRNA的示意图:采用JAWS II细胞,处理不同构建体,这些构建体均包含已知可在MHC I上呈递的OVA表位肽序列(SIINFEKL)。(B)数据显示对照组及多表位mRNA LNP处理组的MHC I肽呈递情况。对照组包括未处理细胞、SIINFEKL肽处理组,以及编码全长OVA的LNP‑mRNA处理组。LNP1‑mRNA的测试浓度为1 μg/mL。
Part.3 – A:良好的安全性,支持重复给药策略(Safe for Repeated Dosing)
Part.3 – B:强效的抗肿瘤反应,显著延长生存期(Potent Anti-Tumor Efficacy)
如下图,合成了8种多表位mRNA构建体,其包含不同数量的B16F10 特异性表位、重复表位或辅助性表位,并采用Cytiva自有的脂质纳米颗粒(LNP)进行制剂。这些制剂通过肌内注射(IM)给药于此前已经皮下(SC)接种B16F10小鼠黑色素瘤细胞的C57BL/6雌性小鼠中。


(A)研究设计示意图:采用Cytiva自有的LNP制剂,对8种不同的多表位mRNA进行测试。(B)各实验动物在接种后达到肿瘤体积上限(800 mm³)或人道终点所需的天数。(C)主导多表位mRNA‑LNP组在接种后各时间点的肿瘤体积变化;当超过50%的动物达到肿瘤体积上限或人道终点后,停止肿瘤体积绘制。(D)接种后各时间点肿瘤体积低于800 mm³ 的小鼠比例,以百分比生存率形式表示。
不仅仅是更快的算法,而是更可靠的制造;不仅仅是单一突破,而是可持续交付的平台化工程能力。从宠物到人,从IIT到注册临床,PCV的未来,最终取决于谁能真正把这条复杂的mRNA‑LNP工作流,变成一套可复制、可放大的解决方案。
最后,Cytiva愿以生命科学之力,守护“毛孩子们”健康无恙、远离病痛,也愿以创新之能,驱动PCV疫苗实现平台化生产。

扫描下方二维码
即可获取更多详细资料


 收藏
收藏 询价
询价