寡核苷酸酶法合成技术全景解析:传统与创新的协同进化
寡核苷酸作为核酸药物、基因编辑、分子诊断的核心原料,其合成技术的迭代直接推动生物医药领域的发展。固相载体合成(SPOS)作为经典技术奠定了产业基础,而酶法合成凭借绿色高效、长链合成优势成为新一代技术方向。
Cytiva与上海兆维科技深耕寡核苷酸合成领域,从传统工艺优化到酶法技术创新,共同探索产业升级路径,本文为你全面解析寡核苷酸酶法合成技术的现状与未来。
固相载体合成的核心价值
固相载体合成(SPOS)作为寡核苷酸合成的第一代核心技术,凭借成熟的工艺体系成为当前产业应用的主流,其核心优势突出:
工艺成熟且标准化:
亚磷酰胺法为基础的SPOS技术经过数十年优化,合成流程、质量控制体系高度标准化,适配规模化工业生产,是短链寡核苷酸合成的首选方案。
底物兼容性强:
可高效适配各类修饰核苷(如2′-OMe、2′-F、硫代磷酸酯等),满足核酸药物的多样化修饰需求,是修饰型寡核苷酸合成的核心技术支撑。
产率稳定且成本可控:
短链合成中步骤收率可达99%以上,设备与试剂体系产业化配套完善,规模化生产下成本优势显著。
质控体系完善:
针对合成杂质的分离、检测方法成熟,可严格满足药品生产质量管理规范(GMP)要求,目前已支撑多款核酸药物成功上市。
酶法合成的技术体系与全球应用
酶法合成以温和的水相反应体系、高原子经济性、长链合成优势成为研究热点,主要包括从头酶合成和酶法拼接(酶连接)两类。
从头酶合成:TdT酶为核心,实现从头合成
酶法发展稍晚于化学合成,研究者们先后发现了多核苷酸磷酸化酶,PNPase和T4 RNA聚合酶,用于RNA合成;在DNA合成领域,1959年发现了末端脱氧核糖核酸转移酶TdT,可实现不依赖于模板的DNA合成,以及模板依赖的9°N和KOD聚合酶,通过瞬时配对或self-priming的发夹结构来实现链延伸。出于合成效率、引发剂的偏好等原因,在从头酶合成领域,TdT路线以末端脱氧核苷酸转移酶为核心催化剂,无需模板即可实现脱氧核苷酸的从头聚合,是当前酶法合成的主流技术,主要分为3′终止法、TdT-dNTP conjugate、无终止剂法三种工艺。
核心工艺与特性
3′终止法:
最广泛的技术,通过可逆终止子(RT)封闭dNTP的3′-OH,实现单步碱基精准插入,脱保护后进入下一轮合成,主流RT包括氨基烷氧基、磷酸基、叠氮甲基等,脱保护机制各有不同(如氨基烷基通过亚硝酸盐进行脱保护,磷酸基则用碱性磷酸酶或焦磷酸酶,可实现全酶反应)。
TdT-dNTP conjugate:
通过一个可切割的linker将dNTP的碱基端共价连接到天然的TdT酶上。共轭结构让酶与底物之间保持恒定的空间邻近,从而促进快速的催化加成反应。酶提供的位阻效应可以确保每轮循环只添加单个核苷酸。这种方式的优势在于不需要对TdT进行大量的工程化改造,缺点在于linker切割时会对oligo链有一定的损伤,需要额外的步骤去恢复。
无终止剂法:
使用腺苷三磷酸双磷酸酶(apyrase)降解dNTP的三磷酸基团,或者用笼状分子螯合TdT催化必需的金属离子,从而有效终止每轮碱基添加循环。这种方式的优势在于不需要改造酶或者对底物进行修饰,可以充分发挥天然TdT酶高效快速的加成反应特性,实现超长寡核苷酸的快速合成。缺点在于容易在单轮循环中添加多个重复碱基,需要额外的检查纠错步骤。
| _ | 3′终止法 | TdT-dNTP conjugate | 无终止剂法 |
| dNTP修饰 | 是 | 是 | 否 |
| TdT 需要工程化改造 | 是 | 否 | 否 |
| 是否需要其他试剂 | 否 | 是(需要可切割的linker) | 是(Apyrase或caging molecule) |
| 不足 | TdT酶改造 | linker切割会给oligo带来损伤 | 需额外的纠错步骤 |
基于TdT的三种从头酶合成路线的对比[1]
从头酶合成的技术路线虽然优势众多,但其发展受酶催化效率限制,大多集中在科研端,且合成规模较小。
酶法拼接:酶连接为核心,传统与创新的融合
酶法拼接的核心思路为:先通过SPOS合成短片段寡核苷酸,再利用连接酶(DNA/RNA连接酶)将短片段精准连接为长链,实现“短片段化学合成+长片段酶法拼接”的协同,代表技术包括Almac BOOST技术、上海兆维科技短片段连接技术等。
核心工艺与特性
Almac 3-2-3-2 BOOST技术:
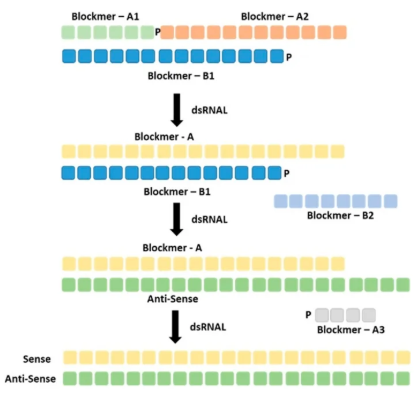
(图片来源:ACS Chemical Biology 2023 18 (10), 2183-2187)
优势:
① 反应体系中最多只含有3个blockmers,避免副反应和杂质的累积。
② 多个QC points,每一步都可以检测反应情况,确保在加入下一个blockmer之前,每个拼接步骤都完全反应,提高合成可靠性。
上海兆维科技短片段连接技术:
针对siRNA、sgRNA等核酸药物,将目标序列拆分为数个短片段,通过杂交形成粘性末端,利用DNA/RNA连接酶催化连接,结合UF/DF(超滤/渗滤)、HPLC纯化,实现高纯度长链合成。

(图片来源:兆维公众号)
酶法拼接拥有非常高的oligo片段转化率,拼接过程几乎不产生新的杂质,下游纯化流程得以简化。上海兆维科技已通过酶法技术实现临床级核酸药物原料合成,助力两款药物候选物获IND批准。
Cytiva × 上海兆维科技的寡核苷酸合成解决方案
Cytiva与上海兆维科技深耕寡核苷酸合成领域,分别从工艺平台与设备、酶法技术与产业化出发,为客户提供从实验室研发到工业生产的全链条解决方案,推动传统固相合成与创新酶法合成的协同应用。
Cytiva:寡核苷酸合成全流程工艺与设备支撑
Cytiva作为全球生物制药工艺解决方案提供商,为寡核苷酸合成提供从原料、合成设备到下游纯化的全链条技术支撑:
固相合成体系:
提供高纯度合成单体、固相载体、合成柱,优化亚磷酰胺法的耦合效率与修饰兼容性,适配GMP级短链寡核苷酸生产。

酶法合成配套:
提供温度控制精准的反应设备,适配酶法合成的温和反应需求;多样的纯化选择,适配简化的下游处理方案。针对酶法拼接不同步骤的杂质特性(酶、未连接片段、缓冲液添加剂等),提供各类材质和截留分子量超滤膜包、及匹配的硬件设备,实现杂质的高效去除,满足药品质控要求。

(Cytiva酶拼接整体解决方案,C2P)
工艺优化经验:
结合多年生物制药工艺经验,提供灵活的寡核苷酸合成纯化方案,同时支持固相合成与酶法拼接。
上海兆维科技(Hongene):寡核苷酸酶法合成产业化核心技术

上海兆维科技作为国内核酸药物原料合成的领军企业之一,聚焦酶法拼接技术的产业化应用,为客户提供临床级长链寡核苷酸的酶法合成服务与技术解决方案:
核心酶法技术:
成熟的siRNA、sgRNA、exRNA等长链寡核苷酸酶法连接合成技术,产物纯度>96%,适配核酸药物的临床前研发与中试生产。
定制化合成服务:
提供修饰型寡核苷酸的定制化合成,兼容2′-OMe、2′-F、硫代磷酸酯、GalNAc等多种修饰,满足不同核酸药物的研发需求。
工艺降本方案:
开发C2P、C2C酶法合成方案,省去过柱纯化步骤,大幅降低长链寡核苷酸的生产成本,推动核酸药物的规模化应用。
质控体系:
建立符合GMP要求的质量控制体系,针对酶法合成产物的杂质进行严格检测,确保产物符合药品研发与生产的质控标准。
传统与创新的双向赋能
寡核苷酸合成技术的发展并非“非此即彼”,而是固相载体合成与酶法合成的双向赋能:
- SPOS作为成熟技术,将继续支撑短链、修饰型寡核苷酸的规模化生产;
- 酶法合成将聚焦长链、复杂序列寡核苷酸的合成,弥补SPOS的技术短板,
- 而酶法拼接则实现了两者的有机融合,成为当前核酸药物产业化的最优解之一。
未来,随着酶工程技术的进步、可逆终止子的优化、合成工艺的整合,酶法合成将进一步提升修饰兼容性、合成精度、规模化效率,而Cytiva与上海兆维科技也将继续深化合作,从工艺平台、设备优化、技术产业化出发,共同推动寡核苷酸合成技术的升级,为核酸药物、基因编辑、分子诊断等领域的发展提供核心原料支撑,助力生物医药产业的创新突破。

(图片来源:Nature Communications | ( 2024) 15:8009)
教学课程
市场活动
资料下载
产品

 收藏
收藏 询价
询价