金牌背后的伤痕,愿为你抚平 — Biacore助力伤口愈合新机制研究
图片
2019年,美国芝加哥大学分子工程研究所的 Jeffrey A. Hubbell教授团队,在血液学顶级期刊Blood(IF:22.113)上发表了一篇题为“The heparin binding domain of von Willebrand factor binds to growth factors and promotes angiogenesis in wound healing”,揭示了加速伤口愈合的全新机制。该团队发现血管性血友病因子(VWF)与多种生长因子(GFs),可以通过VWF A1结构域内的肝素结合结构域(HBD)结合,进一步提高GF在创面部位的保留时间,促进血管生成,加速伤口愈合。作为分子互作金标准的Biacore,在证明VWF与多种GFs结合的重要环节上起到关键作用。
在伤口愈合过程中,生长因子(GFs)的分布、作用发挥和信号转导是通过它们与伤口微环境中的细胞外基质成分结合来协调的。细胞外基质蛋白与GF结合被证明可以用来调节血管生成和促进伤口愈合。血管性血友病因子(VWF)是由内皮细胞(ECs)和巨核细胞合成的一种大型血浆糖蛋白。它最主要的功能是介导血小板粘附在损伤部位的内皮下,并作为凝血因子VIII(FVIII)的载体,完成止血作用。常见的遗传性出血疾病血管性血友病(VWD),就是由VWF缺陷或缺乏引起的。而在一些VWD患者中发现了迟发性伤口愈合的症状,那是否VWF在伤口愈合中也发挥重要作用呢?
研究人员在进行动物实验后确定VWF缺乏会导致小鼠伤口愈合延迟,确认VWF的确参与了促进皮肤组织修复。随后,他们使用Biacore将血浆来源的VWF固定在C1芯片上,将不同类型的生长因子,包括VEGF121、VEGF-A165、PDGF-BB、NT-3、PDGF-DD等作为分析物流经芯片表面进行亲和力/动力学检测。结果显示,不含HBD结构域的VEGF121与VWF不结合(图1);而其他含有HBD结构域的GFs(VEGF-A165、PDGF-BB、NT-3、PDGF-DD)均能与VWF结合(图2),其中VEGF-A165与VWF的亲和力KD值为27 .4nM,PDGF-DD和VWF的KD值为12.6 nM,这些数据表明,VWF A1域的HBD是介导WWF与GF结合的关键结构。
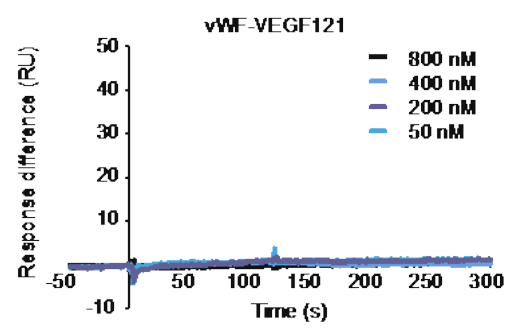
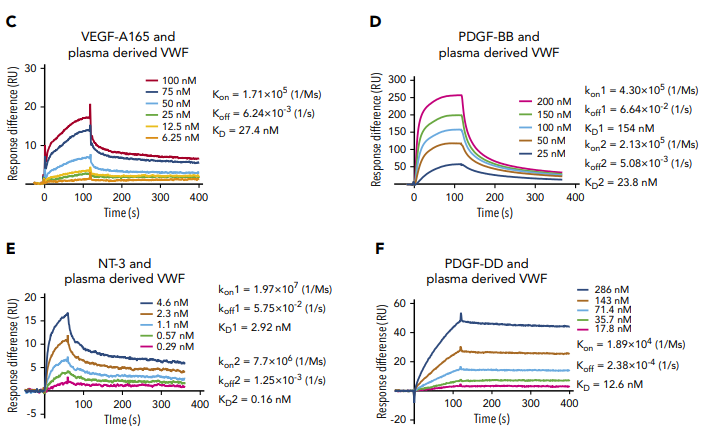
后续实验中,研究人员合成带有HBD结构域的VWF-HBD肽,并使用其将纤维蛋白基质功能化。使用VWF-HBD功能化的纤维蛋白基质治疗VWF缺陷小鼠伤口时,小鼠伤口中GFs的数量增加并促进血管生成,加速伤口愈合。该研究证明VWF是一种新型的具有保留GFs能力的保存库,可以促进伤口愈合,同时VWF-HBD也可以作为一种可能的新型工具来促进伤口愈合。

冬奥会马上就要落下帷幕,恭喜所有奖牌获得者的同时,也感谢所有参赛者们。感谢你们向我们展示了真正的奥林匹克精神,我们将在你们的精神鼓舞下努力生活!而Biacore也将助力更多伤口愈合全新机制的探究,致力于给到各类满是伤痕的患者与运动员一种更快、更有效的伤口愈合方式,希望大家远离伤病,在自己的体育道路、人生道路中飞得更高,走得更远!
Biacore,
for a better life

 收藏
收藏 询价
询价