Biacore高效筛选开启胰腺癌治疗新思路
Biacore高效筛选开启胰腺癌治疗新思路
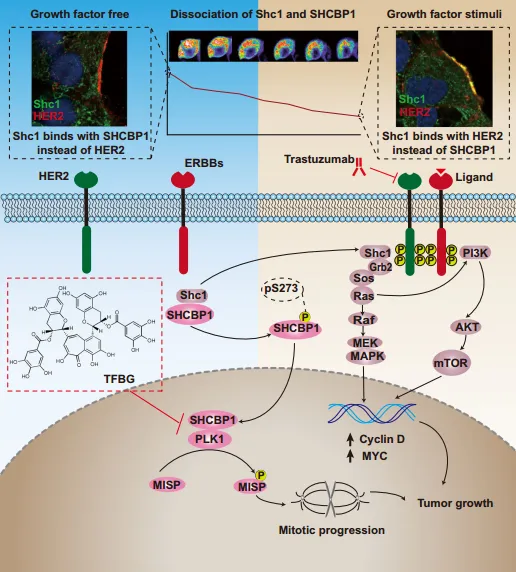
研究揭示了Sorcin蛋白在胰腺癌中作为铁死亡抑制因子的作用机制:Sorcin通过与PAX5相互作用阻止其核转位,降低FBXL12表达,减少ALDH1A1泛素化,从而抑制铁死亡。在聚焦到Sorcin蛋白之后,研究人员在Biacore上对天然产物文库进行了筛选,期望快速找到与Sorcin蛋白结合的潜在药物。
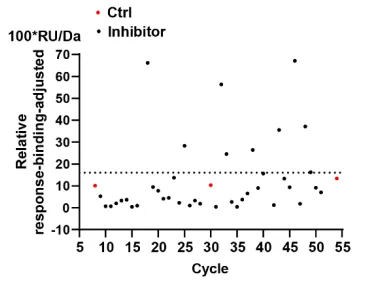
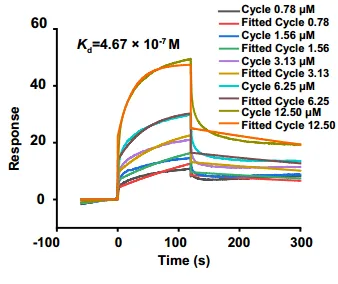
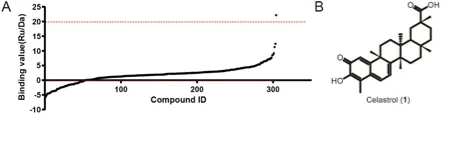
实验中将Sorcin蛋白氨基偶联于传感芯片,Biacore预设的筛选程序自动完成304个天然产物的单浓度进样,得到每个药物与靶点蛋白的结合响应值(RU),经过分析软件的分子量校准之后,成功鉴定出雷公藤红素(Celastrol)能够与Sorcin蛋白发生特异性结合(图1)。


 收藏
收藏 询价
询价