诊断原料替代,想说“I do”口难开
诊断原料替代,想说“I do”口难开
体外诊断市场现状及原料企业的挑战
中国体外诊断市场规模从2015年约427.5亿元增长至2019年约805.7亿元,年化复合增长率达到17.2%。体外诊断市场的快速增长,带来了上游核心原料需求的快速增长。目前,体外诊断试剂核心原料外采占比依然较大,国产替代空间广阔。其中分子诊断酶和单抗产品是两项最大产品,也是目前国内生物原料企业必争之地。

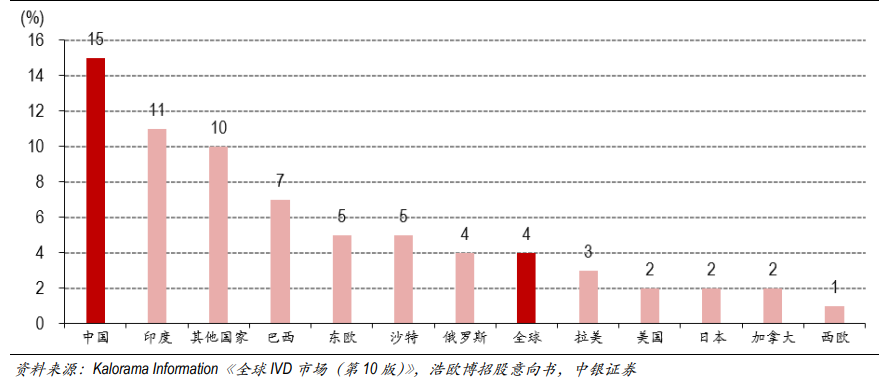
图1:2016~2021年全球各地区IVD市场预计复合年均增长率 (%)
原料企业想要不断地扩大市场份额不是一件容易的事。很多细分赛道如生化、免疫已是发展多年的成熟市场,因此,对原料企业,特别是众多后来入场的国产原料企业而言,相当多的业务“机会”需要试剂厂家进行原料替换才能变现。
然而,IVD试剂厂家任何一个投产项目都经历了严谨而耗时的开发流程,包括原料筛选、配方开发、临床验证或试验、注册检、试生产和放大生产等,从立项到上市,整个时间跨度以年计。若进行原料替换,试剂厂家基本上相当于重走一遍开发流程,时间和人力成本甚巨;此外,原料替换对试剂品质的未知风险使得决策人承担巨大压力而不敢轻举妄动。 事实上,试剂厂家替换原料往往是客观情势下的被迫之举,不得不换。所以,原料企业要想取代试剂厂家的原有供应商,大多数情况下仰仗于竞争对手犯错,或者重大突发事件的助力。
原料企业的机会点
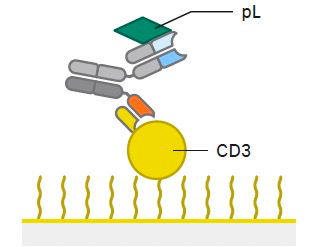
产品性能绝对是试剂厂家进行原料替换的最大动力。 抗原、抗体以及高品质的免疫干扰阻断剂等是免疫检测的核心关键原料,对产品的功能实现和性能具有决定性作用。因此,抗原、抗体性能与质量的优劣以及对常见免疫反应干扰的消除对诊断试剂的灵敏度、特异性等指标,乃至诊断试剂的整体性能与质量优劣有很大影响。在免疫检测领域,确保产品检测结果可靠、稳定及一致性是获得市场成功及良好声誉的关键。
1、原料筛选
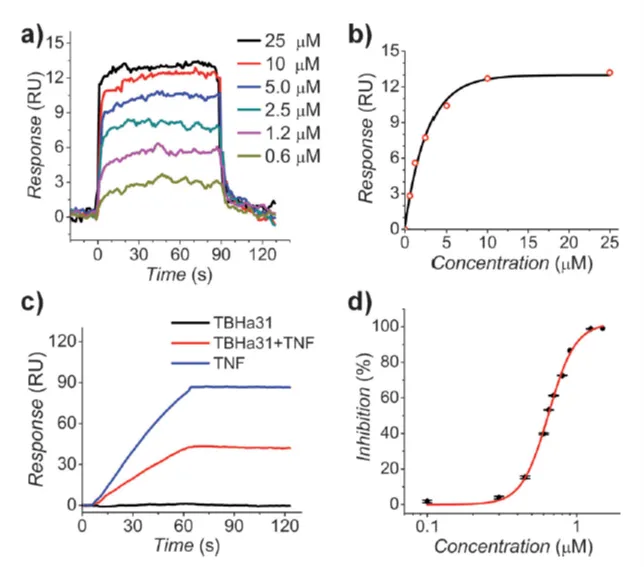
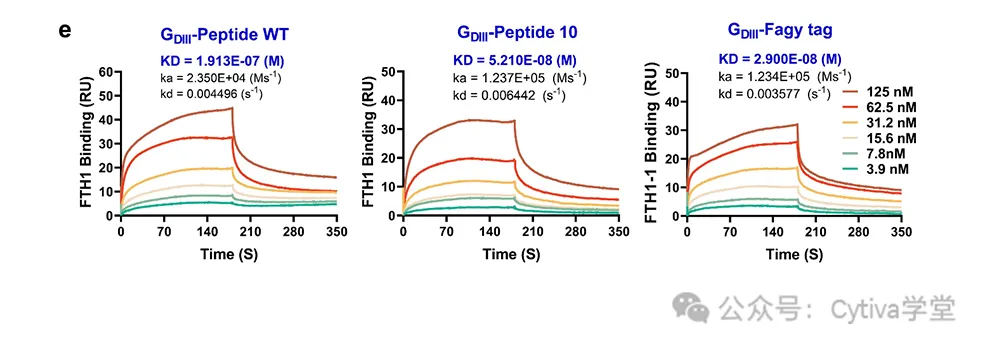
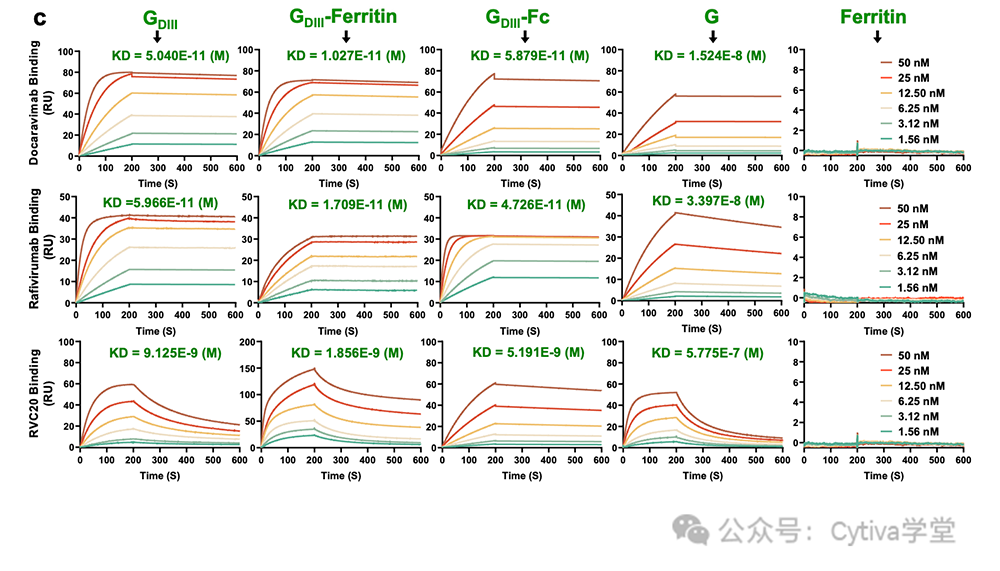
对于体外诊断试剂的品质来说影响因素颇多,其中非常关键的一项就是原料的筛选。在选择了你的检测目标后,或者在寻求改善现有检测的性能时,非常值得花时间和精力做好原料的筛选工作。随着行业的发展与发现技术的进步,库容越来越大,所筛抗体亲和力越来越高, IVD企业急需自动化程度高、通量高、筛选速度快、灵敏度高、检测范围宽、成本低的筛选设备。Biacore 8K/8K+作为高通量高质量的互作检测设备,可同时放置1,536或4,608个样品,实现超过60或72小时无人值守,每小时筛选数百个样品,并且每个样品的筛选成本不到1块钱。
作为筛选的标准,表达量的高低决定了后续生产难度,动力学数据在原料抗体筛选中也十分关键,因为原料抗体与抗原的结合速率决定了检测信号出现的速度,而解离速率则决定了检测信号持续的时间长短。在靶点滞留时间越长的抗体越能耐受缓冲液冲洗,从而获得的诊断试剂信号持续时间越久,并且具有更高的灵敏度和稳定性。Biacore在筛选阶段能无需纯化,直接检测表达上清,同时提供动力学/亲和力和浓度测定的结果,做到浓度测定与亲和力/动力学检测二合一,相比 ELISA等其他技术,Biacore只需要一次实验即可得到三个维度的数据,极大地提高了检测效率,同时还可有效降低实验成本和时间成本。
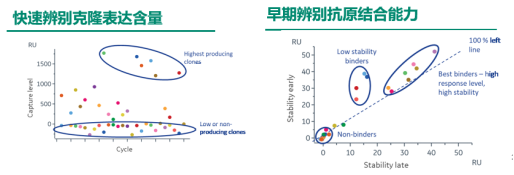
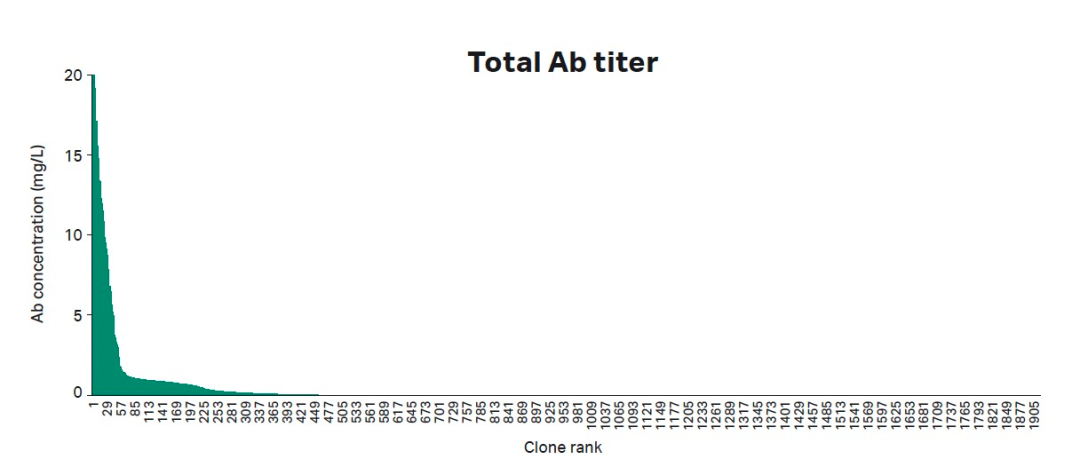
图2:初始筛选剔除非生产性克隆,并鉴定出具有所需特异性及亲和力的抗体
2、活性/效价/亲和力
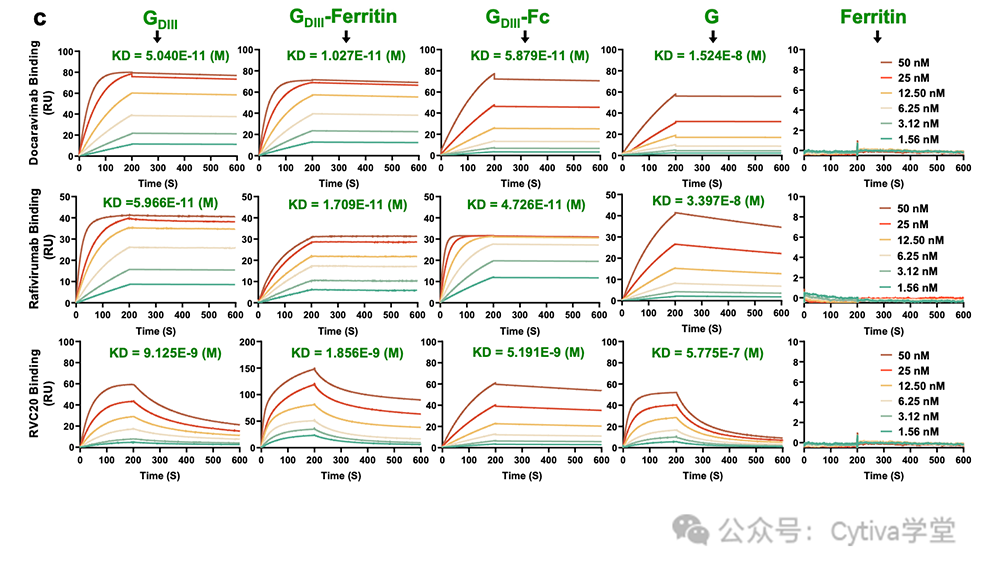
是反应抗体与抗原之间反应性的直接指标,现阶段大多数抗体供应商对于效价的检测是在ELISA平台上通过重组或者天然抗原对抗体进行测试,通过信号值对抗体的活性进行考察。传统方法提供的信息有限,不论是自主研发筛选或外部获得的原料抗体,都需要进一步进行亲和力/动力学检测,多维度评估,选出与研发目的高度匹配的原料抗体,即识别更快、解离更慢、亲和力更强。Biacore宽泛的亲和力/动力学检测范围与更高的分辨率,能够快速精确地帮助研发人员优中选优,强中选强。
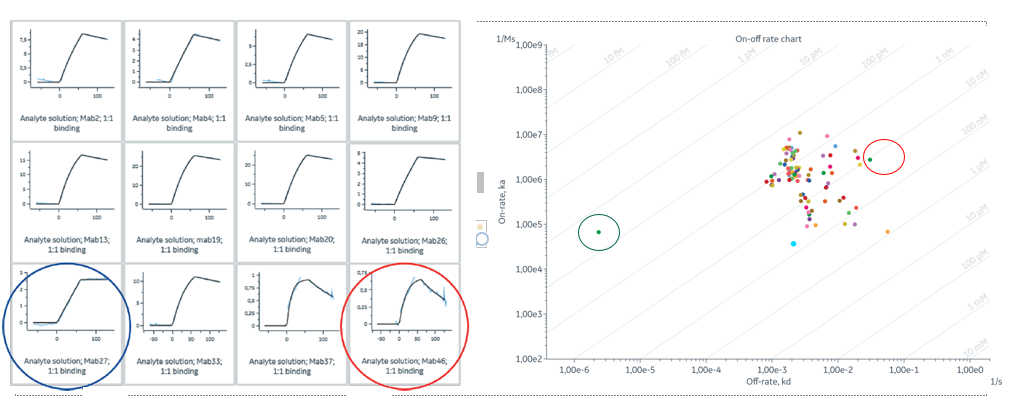
图3:在单个图中可视化动力学和亲和力,以便更明智地选择抗体
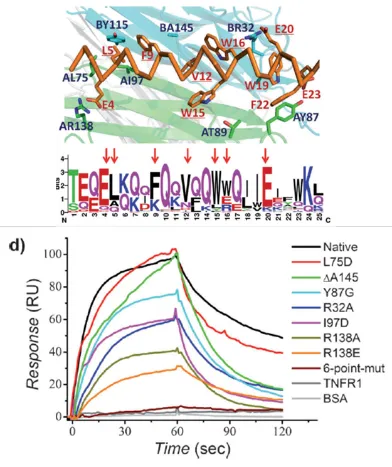
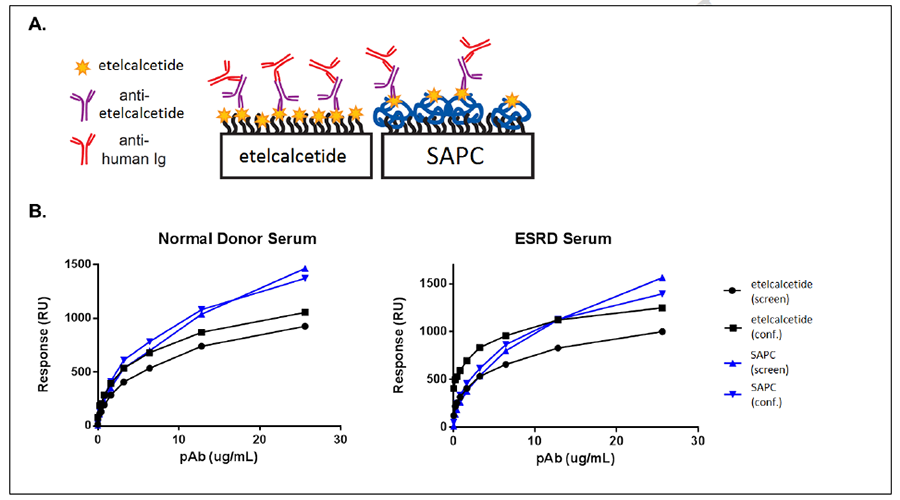
3、特异性/结合位点
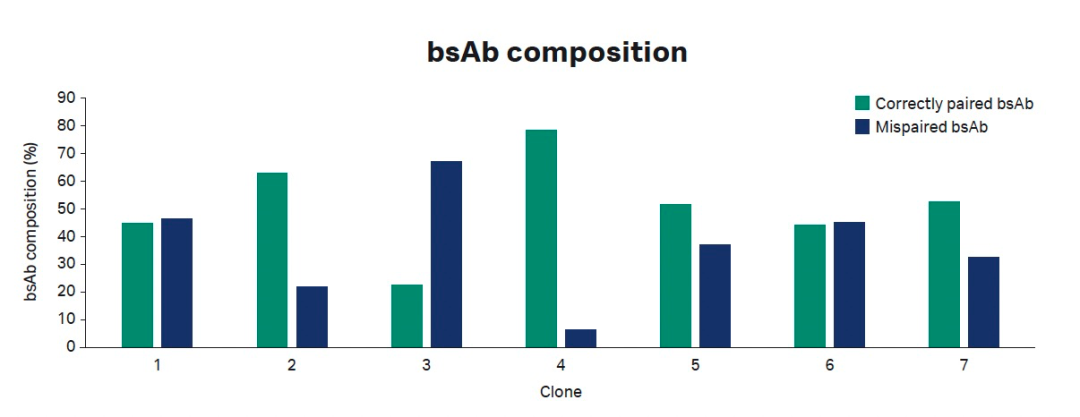
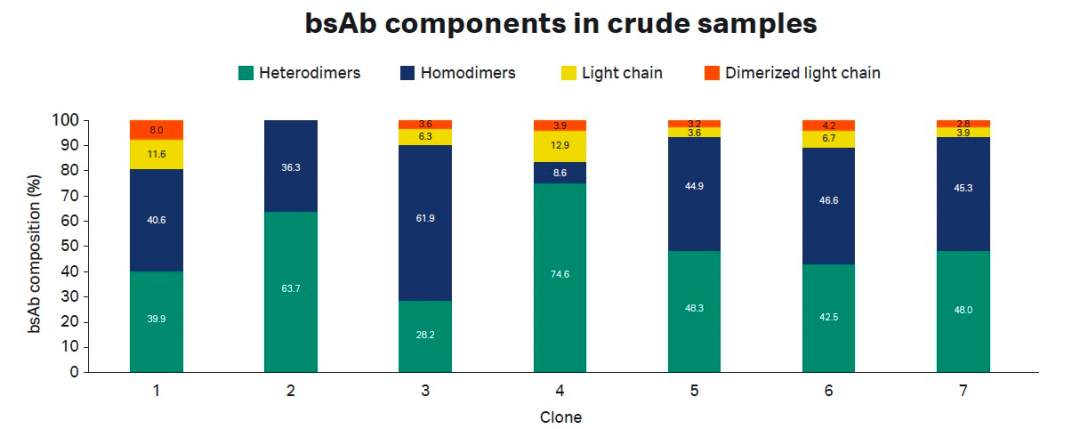
特异性指抗体单一性识别某种特定抗原的能力。该指标虽然不直接影响试剂整体反应性,但是却对于检测结果有着很重要的影响。外周循环中除了待测标志物之外,还存在许多其他分子。这些分子可能和待测物具有类似的结构或构象;当抗体所识别的线性表位的氨基酸序列或者构象表位的结构域存在于其他分子中时,便会导致测试结果的假阳性或者假阴性。这既是抗体特异性差所导致的结果,也可以理解为抗体识别的抗原表位不够专一所致。因此,抗体的识别位点是决定抗原特异性的关键性因素。Biacore 8K/8K+及最新款Biacore 1系列设备软件内置epitope binning实验与分析模块,能够更快、更好地展现配对分析的结果,助力原料抗体配对成功,鉴定抗体识别位点。
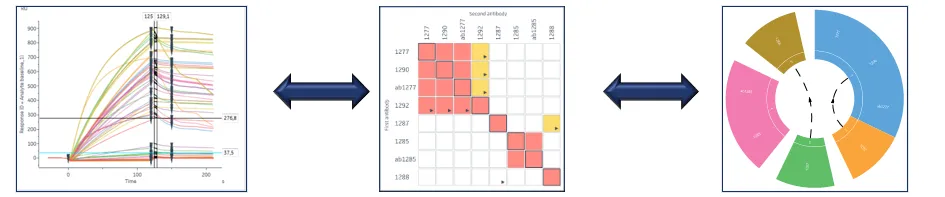
图4:软件自动可视化表位多样性的特征——叠加传感器图、热图和饼图
4、重复性/批间差
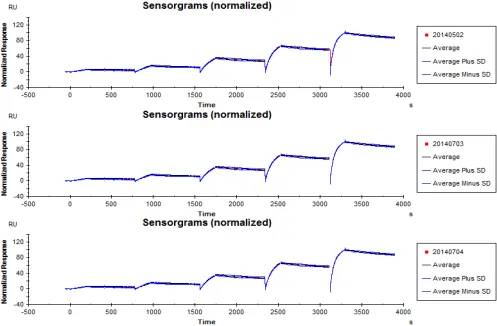
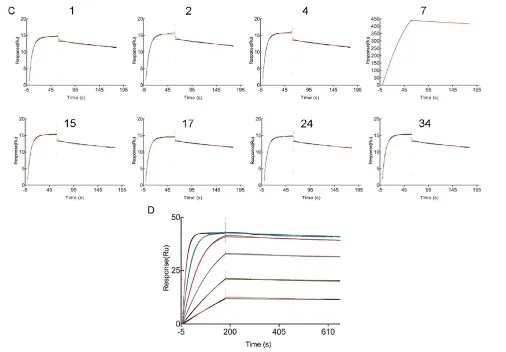
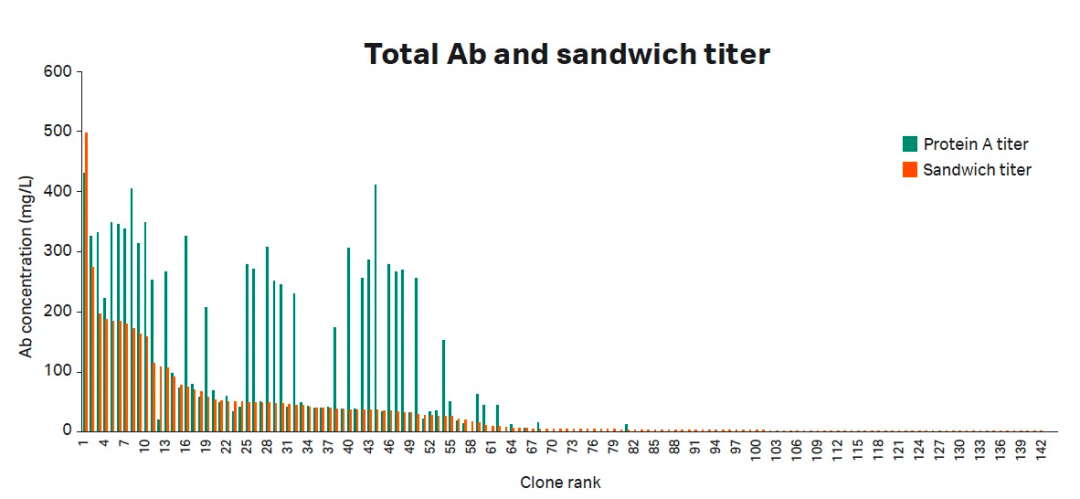
图5:根据亲和力及传感图重复性,评价批间相似度
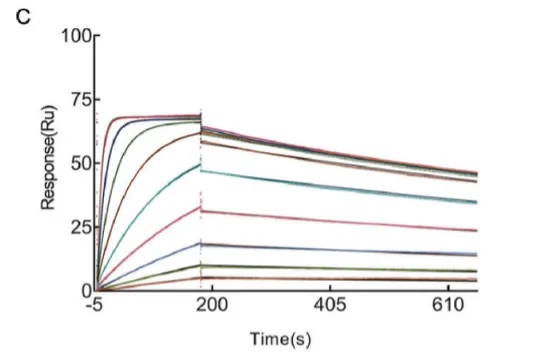
5、稳定性
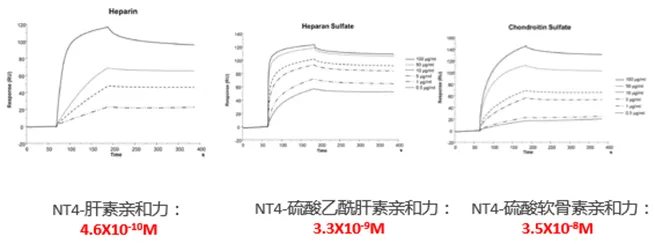
在特定的储存条件下,一定时间内抗体是否能保持其活性也很重要。常见对于原料稳定性的影响因素有温度及PH。目前大多数体外诊断生产公司倾向于使用37℃的加速破坏试验以模拟抗体的长期稳定性。其原理主要基于阿伦尼乌斯的经验公式推理而得,但是实际上加速稳定性并不能体现抗体的真实稳定性,试剂的使用场景决定了原料需要在不同的温度条件下表现依然稳定。Biacore不仅可以检测压力测试后的样品活性,其具有独立的控温系统,可在4-40℃的温控范围内进行亲和力检测,帮助更好地评估原料真实的性能。
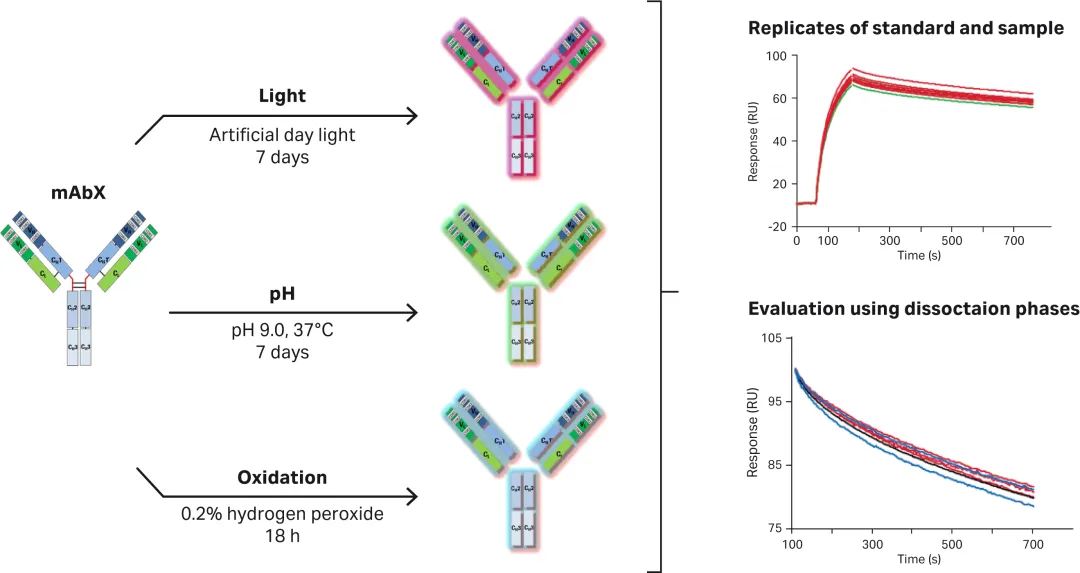
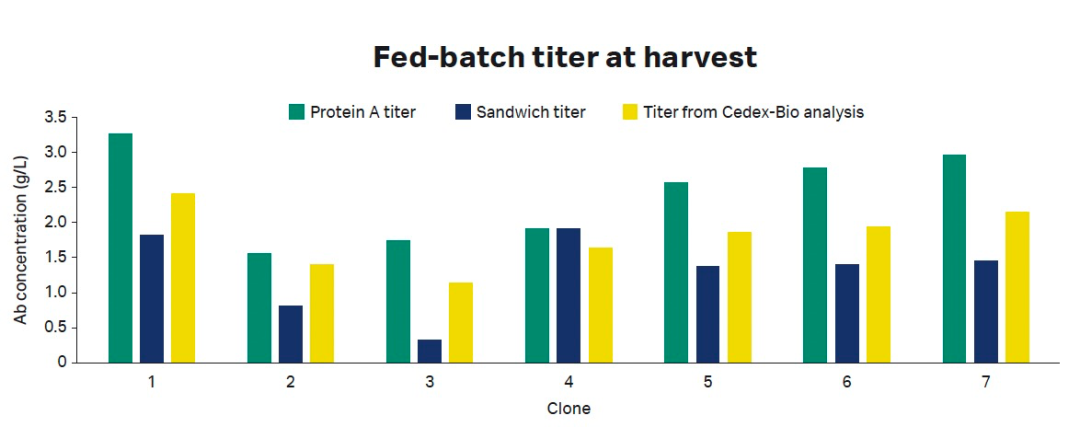
图6:压力测试后检测抗体结合能力的变化
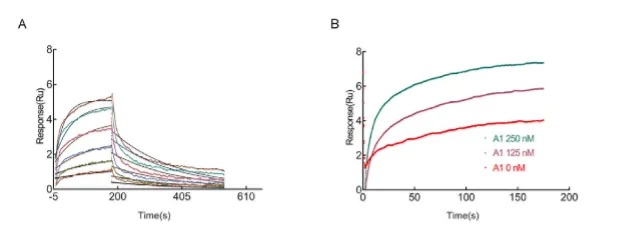
6、缓冲液体系
缓冲液“设置了环境”,在免疫诊断试剂中为结合提供合适的条件很重要。不仅要尝试不同的缓冲溶液,还要尝试这些溶液的不同浓度。即使是一个很小的浓度差异也能使检测成功或失败。在开发早期对不同缓冲液对抗体的亲和力影响进行评估,能够有效降低开发后期的风险。通过Biacore独有的A-B-A功能单次可以在保持连续流的基础上快速、便捷地检测高达4,608种不同缓冲液成分对抗体与抗原(待检测物)的影响,找到最合适的缓冲体系。
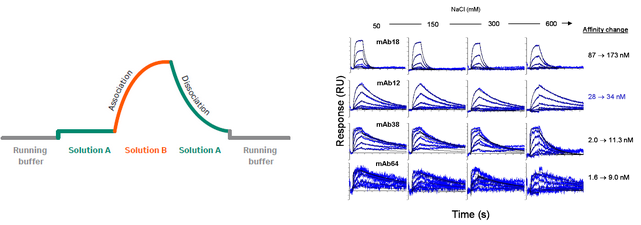
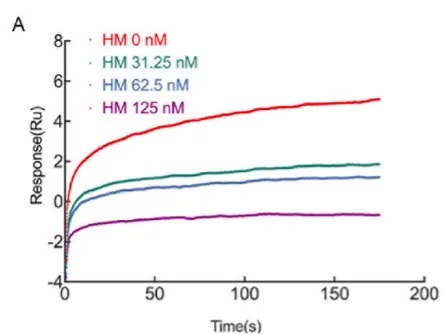
图7:使用ABA模式筛选不同离子强度对结合的影响(分析物分子量较低,响应值低,有部分噪音)
总 结
随着行业的发展,试剂厂家主动进行原料替换的情形或案例越来越多。比如企业自身实力快速壮大,未雨绸缪,降低单一品牌原料依赖性,逐步切换供应商。再比如,越来越多的试剂厂家,通过收购原料供应商,或者自建原料开发平台,以期一劳永逸解决潜在“卡脖子”风险。
面对机遇,原料企业需要足够的战略定力,精益求精、打磨产品品质。如果开发出的原料品种,相比市面上的竞品有显著性能上的优势乃至形成代差,例如抗体的灵敏度有数量级的提升,或者酶的活性及稳定性成倍的增强,无疑将大大增加试剂厂家进行原料替换的动力。
如何能在高手如云的原料企业中占得先机,一个稳定、高效、精准的检测利器必不可少。Biacore作为中美日等多国药典收录的互作检测技术,其使用贯穿整个诊断原料研发及生产的始终,包括早期原料抗体的筛选、亲和力/动力学表征、结合特异性、缓冲体系的筛选和配对分析,以及生产阶段基于活性浓度测定或批次间活性检测(亲和力/动力学)的质量控制等。在原料替换的风口来临之时,必能助力企业顺势而起,扶摇直上。

 收藏
收藏 询价
询价