Biacore 2025年度回顾:从分子到世界,见证创新力量
Biacore 2025年度回顾:从分子到世界,见证创新力量
让我们一起回顾这一年Biacore的高光时刻,感受科学的温度,洞察未来的方向。
一卓越贡献 | 探索前沿,点亮科学星河
让我们一起回顾这一年Biacore的高光时刻,感受科学的温度,洞察未来的方向。
一卓越贡献 | 探索前沿,点亮科学星河
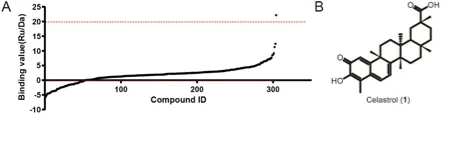
研究揭示了Sorcin蛋白在胰腺癌中作为铁死亡抑制因子的作用机制:Sorcin通过与PAX5相互作用阻止其核转位,降低FBXL12表达,减少ALDH1A1泛素化,从而抑制铁死亡。在聚焦到Sorcin蛋白之后,研究人员在Biacore上对天然产物文库进行了筛选,期望快速找到与Sorcin蛋白结合的潜在药物。
实验中将Sorcin蛋白氨基偶联于传感芯片,Biacore预设的筛选程序自动完成304个天然产物的单浓度进样,得到每个药物与靶点蛋白的结合响应值(RU),经过分析软件的分子量校准之后,成功鉴定出雷公藤红素(Celastrol)能够与Sorcin蛋白发生特异性结合(图1)。

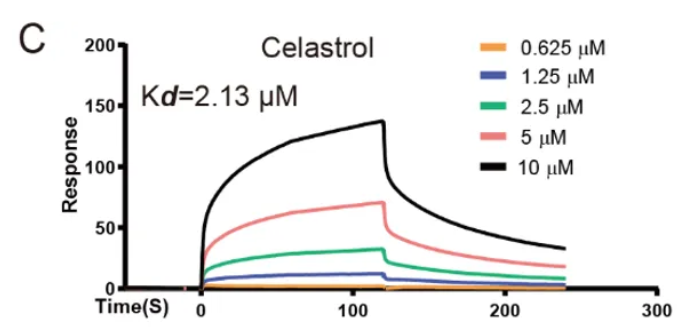
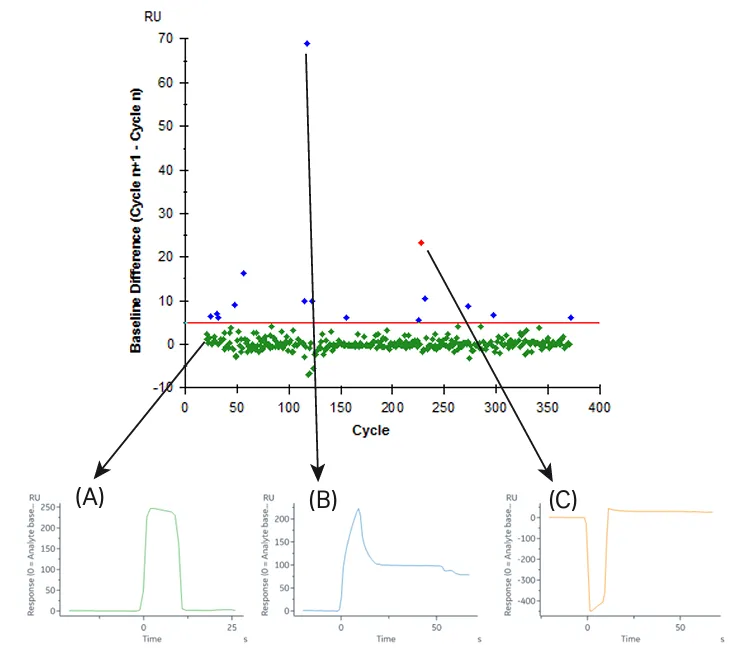
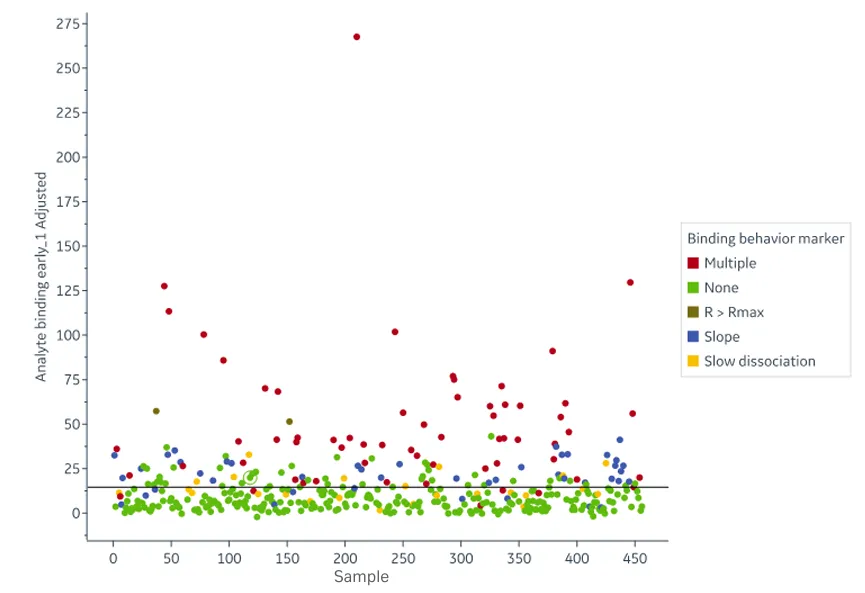
跨膜蛋白175(TMEM175)的上调通过促进α-突触核蛋白聚集体的清除,具有改善帕金森病(PD)的潜力。理解TMEM175激动剂的结构基础对于揭示其PD治疗潜力至关重要。
近日,中山药物创新研究院、中国科学院上海药物研究所、南京中医药大学药学院及中南大学湘雅医院等13家单位联合在《Neuron》发表最新研究,首次解析人源TMEM175离子通道与三种激动剂的冷冻电镜结构,为基于结构的药物设计奠定了基础,并验证了TMEM175激动剂可有效降低病理性α-synuclein水平,为开发治疗PD的新型DMT提供了重要思路。
在帕金森病靶点TMEM175激动剂的研发中,精确测定小分子与靶蛋白的结合亲和力是优化先导化合物的关键一步。研究团队如何运用Biacore 8K系统,为DCY1020、DCY1040等候选分子提供关键的动力学数据支撑?
研究人员使用Biacore 8K SPR系统,对候选分子与TMEM175的结合进行了精准量化:
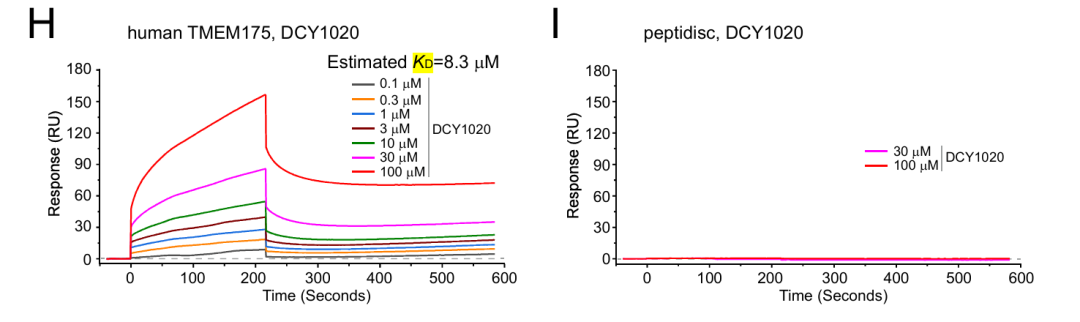
图2:DCY1020与人类TMEM175结合
DCY1020未显示与peptidisc的结合
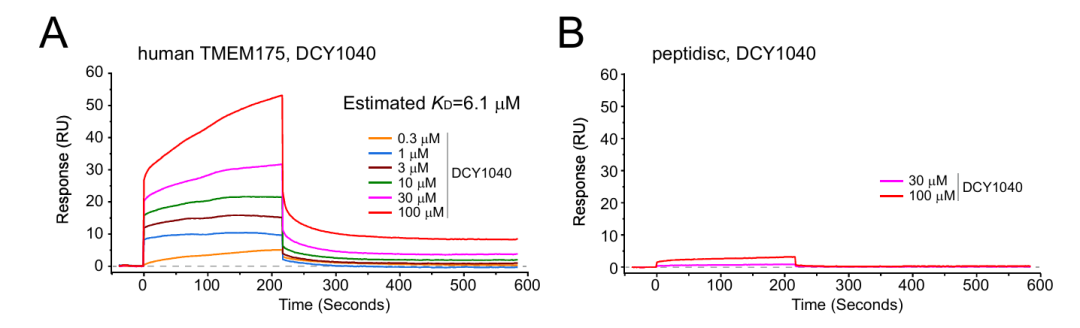
DCY1040未显示与peptidisc的结合
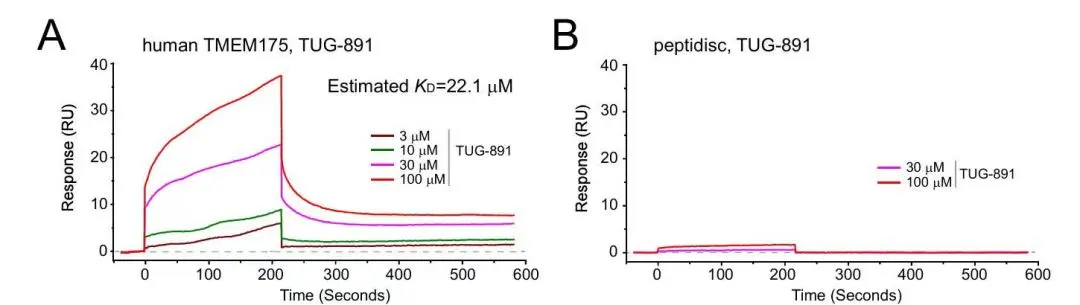
TUG-891未显示与peptidisc的结合
由此可见,此项研究成功地将精准的动力学数据(Biacore)、清晰的原子结构(Cryo-EM)与可靠的功能验证相结合,完整地诠释了TMEM175的激活机制。这不仅为帕金森病的药物开发指明了新方向,也再次证明,多技术平台的紧密协同,是攻克复杂靶点、推动源头创新的有效路径。
无论是破解病理谜题,还是推动药物的临床转化,Biacore都如科研路上的“精准导航仪”,助力科学家突破技术瓶颈。以技术创新赋能基础研究,以全流程支撑加速药物落地,最终让更多像帕金森病这样的难治性疾病患者看到希望,持续为生命科学进步与人类健康保驾护航。
然而,在临床实践中,ADC药物仍面临两大核心挑战:耐药性和治疗窗口窄。前者让初始有效的药物最终失效,后者则限制了给药剂量,使得疗效难以进一步提升。
2025年8月,映恩生物的研发人员就基于以上背景开发出了名为DB-1419的新型双抗ADC。并在国际期刊Clinical Cancer Research上发表题为“Preclinical evaluation of DB-1419, a novel bifunctional and bispecific anti-B7-H3/PD-L1 antibody-drug conjugate”的研究论文,详细阐述了DB-1419的设计以及临床前研究数据,为ADC疗法的未来发展提供了重要参考。
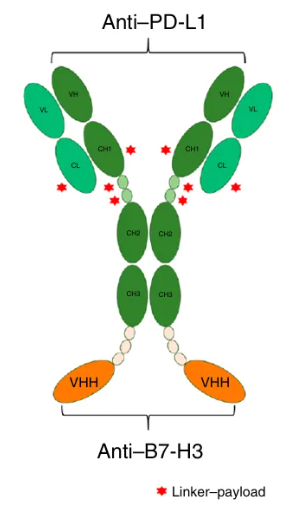
首先研究人员就对DB-1419进行了全方位的质量评估,包括结合特异性、亲和力、血浆稳定性,以及药代动力学特征等。在这其中,就用到了Biacore从分子水平上直接验证双抗ADC是否可以精准的识别并准确结合在靶点上以及结合的强度如何。
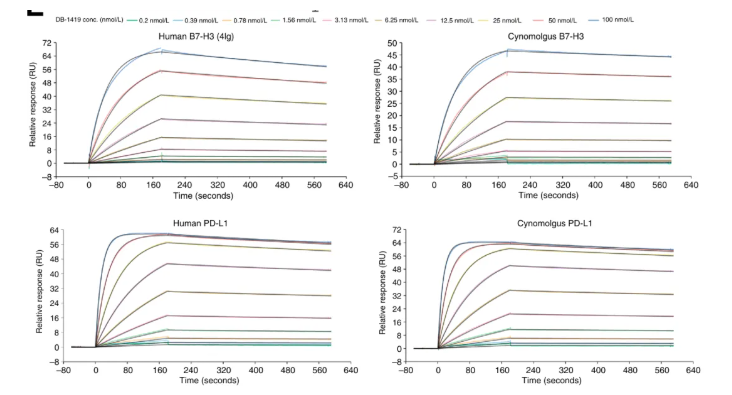
作者选择了使用Human Antibody Capture Kit与CM5芯片搭配使用,制作了一张捕获芯片,将DB-1419捕获到传感芯片上,然后以人和食蟹猴的B7-H3和PD-L1作为分析物依次流过芯片表面进行特异性及亲和力动力学的检测。
Biacore的检测结果表明,DB-1419对食蟹猴和人B7-H3和PD-L1具有强结合,亲和力分别为1.51×10-9;7.31×10-10;3.07×10-10;2.36×10-10(如图2所示)。

食蟹猴的B7-H3和PD-L1的物种交叉反应性
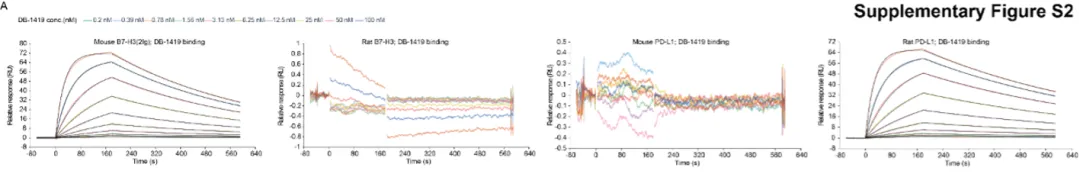
综上所述,DB-1419凭借其“化疗+免疫”双管齐下的创新设计,在临床前研究中展现了卓越的抗肿瘤活性、良好的药代动力学特性和可控的安全性。它不仅是一款药物,更代表了新一代ADC药物的发展方向。
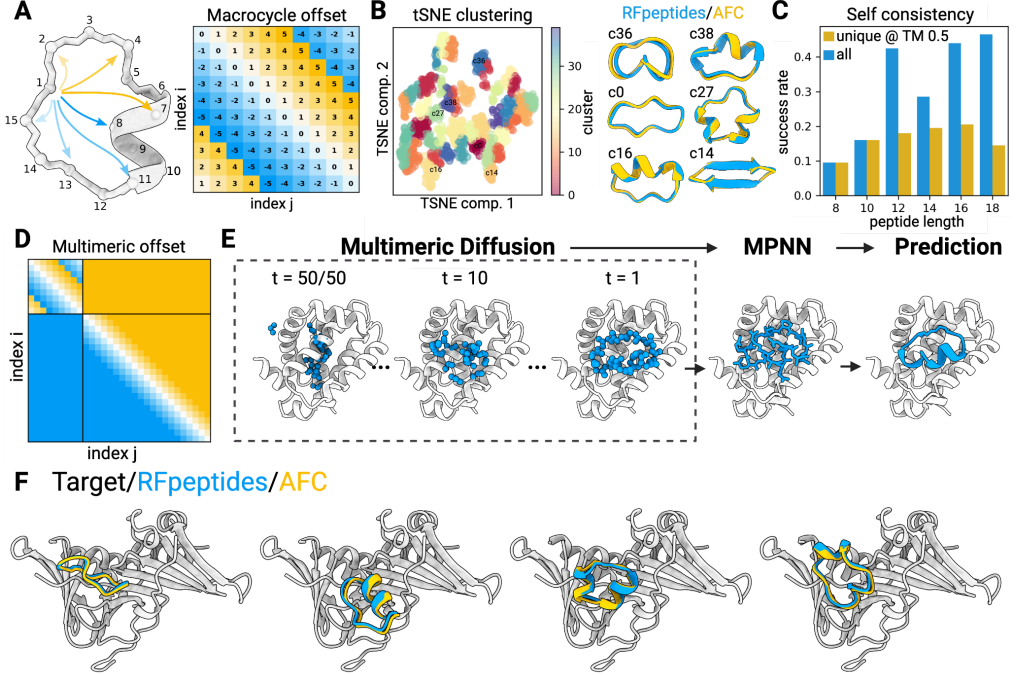
治疗性蛋白靶点大环肽配体的开发通常依赖于大规模筛选方法,这些方法资源消耗大且难以控制结合模式。尽管基于物理的肽设计方法和深度学习的蛋白质设计技术已取得显著进展,但目前仍缺乏可靠的蛋白质结合大环肽从头设计方法。
继去年开发了一种能从头设计生成全新蛋白质的人工智能算法:RFdiffusion后,诺奖得主David Baker实验室在Nature Chemical Biology上发布的RFpeptides——一种基于去噪扩散模型的流程【1】,可用于针对目标蛋白质设计大环肽配体。在四种不同蛋白靶点上分别测试了10-20个设计的大环肽,成功获得了所有选定靶标的中等至高亲和力配体。
相关阅读:
RFpeptides用来设计结合靶蛋白的环肽骨架;ProteinMPNN或LigandMPNN生成序列;RoseTTAFold2(RF2)、AfCycDesign(AFC)预测环肽-靶蛋白复合物结构,打分进行虚拟筛选(图1)。
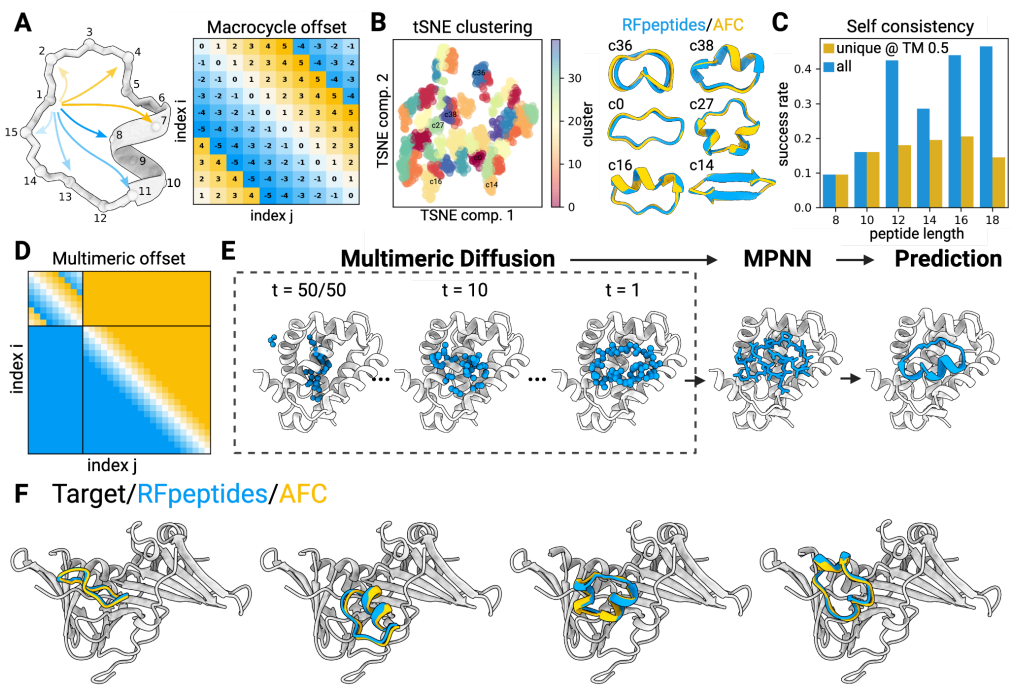
以MCL1为靶蛋白,设计出9965个骨架,每个骨架4个序列,虚拟筛选后合成了27个大环肽。通过SPR筛选,验证大环肽和MCL1的互作,得到D2、D26。最终测定大环肽D2和MCL1亲和力为2 μM。
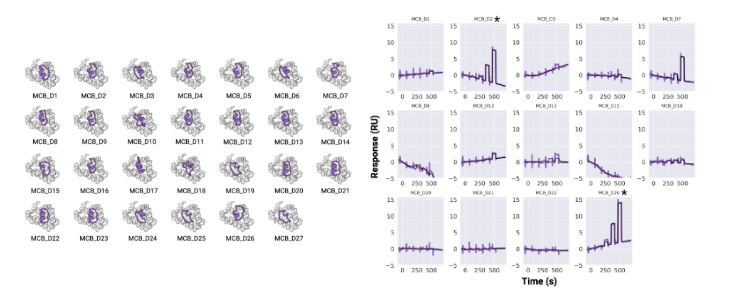
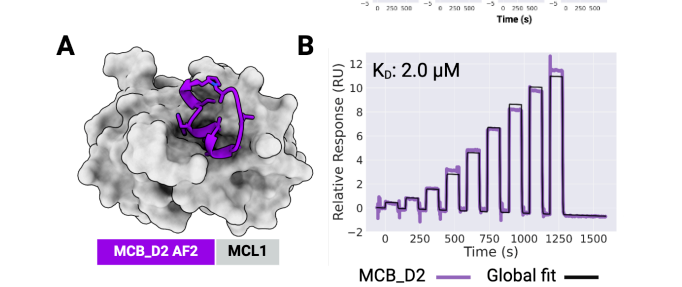
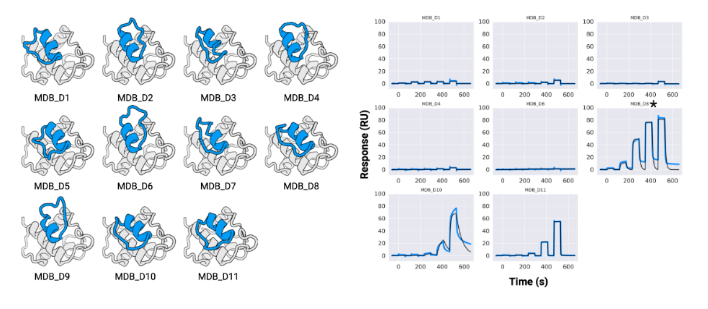
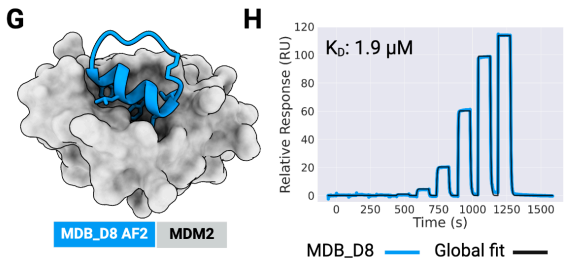
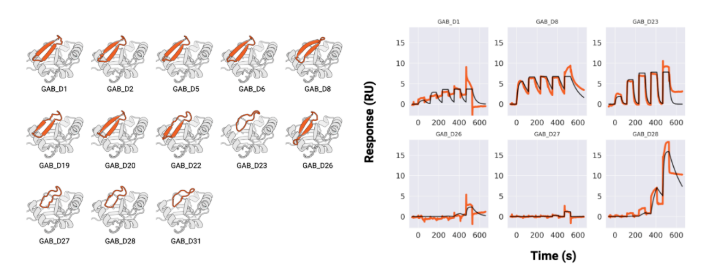
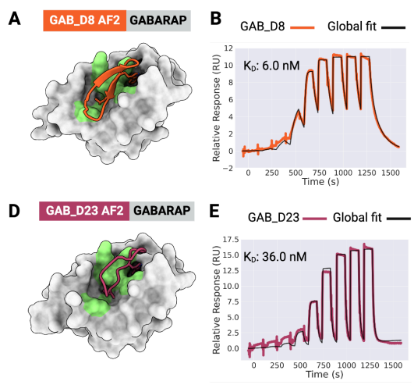
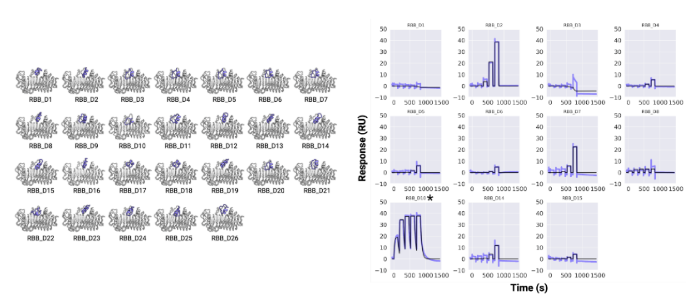
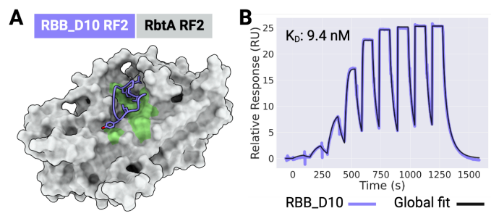
大环肽与MCL1、GABARAP和RbtA复合物的X射线晶体结构显示,其与计算设计模型高度吻合。与文库筛选方法中结合模式确定常成为主要瓶颈相比,RFpeptides生成的大环化合物结合模式可通过设计预知,这将极大促进下游优化进程。因此,RFpeptides为诊断治疗用大环肽的快速定制化设计提供了强大框架。
2025年6月10日,北大-清华生命科学联合中心/北京大学生物医学前沿创新中心/昌平实验室曹云龙团队联合中国科学院生物物理研究所王祥喜团队、美国Moderna公司Laura M. Walker团队在Nature Microbiology上发表论文【2】,提出了针对流行的高频突变病毒,通过预测病毒进化热点,快速准确筛选出广谱中和抗体的策略。发现了来自原始株康复者的广谱中和抗体BD55-1205,该抗体不但能中和所有现存的SARS-CoV-2突变株,与相同表位的其他抗体相比还对表位上的逃逸突变具有很强的抵抗能力,具有开发为新一代SARS-CoV-2广谱中和抗体药物的潜力。
Biacore 8K(SPR)实验(ProA-mAb-RBD)表明BD55-1205 IgG对RBD各种突变显示出高亲和力,范围为1 pM至18 nM,符合其对表位突变的兼容性(图6)。
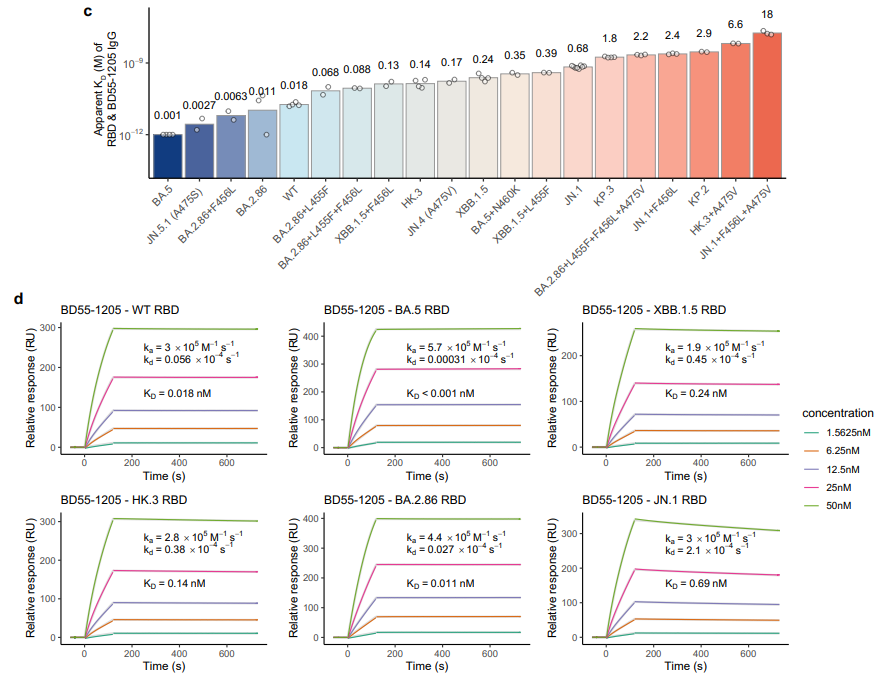
2025年6月,中国科学院微生物研究所吴边研究员团队联合高福院士团队在National Science Review杂志在线发表研究成果【3】。该研究从蛋白质折叠与互作在分子层面的一致性出发,利用多任务学习和自蒸馏策略,开发了基于结构的图神经网络模型Pythia-PPI,实现了对单点突变引起的结合自由能变化(ΔΔG)的可靠预测。相较于传统物理能量函数,Pythia-PPI在预测精度、计算效率及使用便捷性方面均展现出显著优势,为蛋白质相互作用突变效应的定量预测与蛋白理性设计提供了有效工具。
为验证Pythia-PPI的应用价值,研究团队以靶向SARS-CoV-2 PT RBD的CB6抗体为研究对象,从模型预测结果中筛选出前10个可能增强亲和力的单点突变,并通过Biacore 8K(SPR)实验进行验证(ProA-CB6-RBD)。结果显示(图7),V63Y、S35A等突变体表现出稳定的亲和力提升,其中S31R突变体与RBD的结合能力提升超过两倍,充分验证了模型在突变筛选与实验指导中的可靠性与实用性。
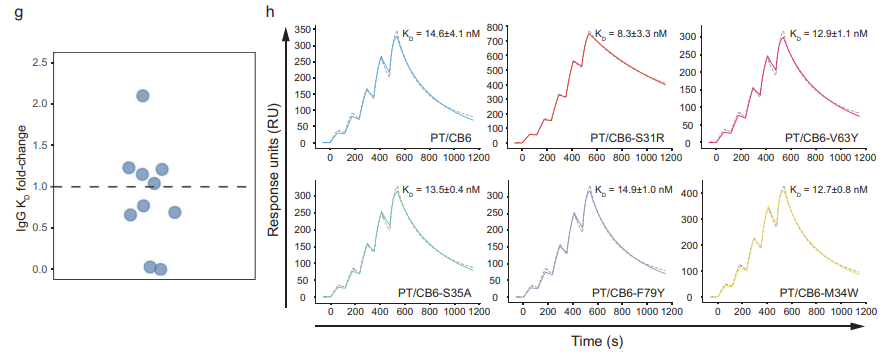
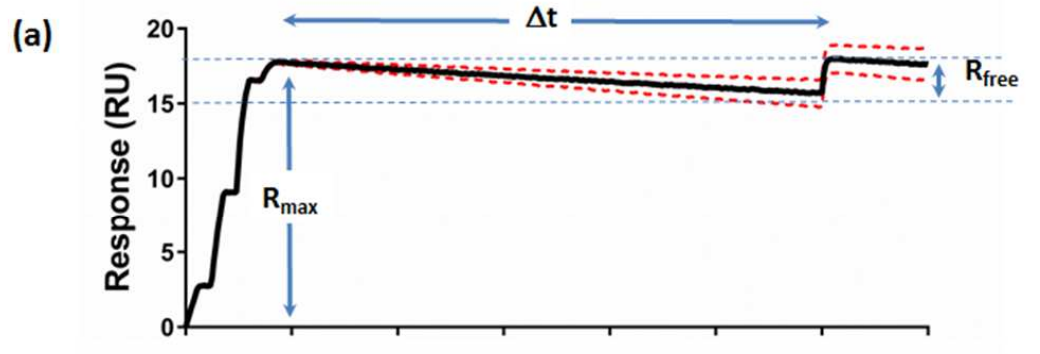
今天带大家看看基因泰克、Sygnature Discovery等Biacore用户如何利用Chaser Assay检测超慢解离-超高亲和力互作。

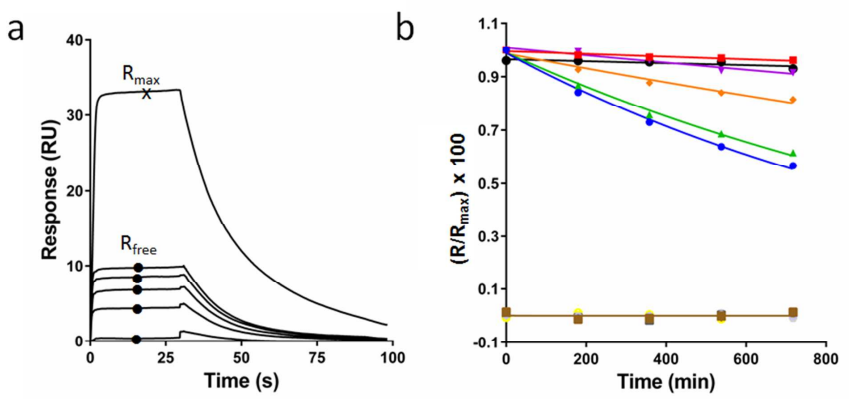
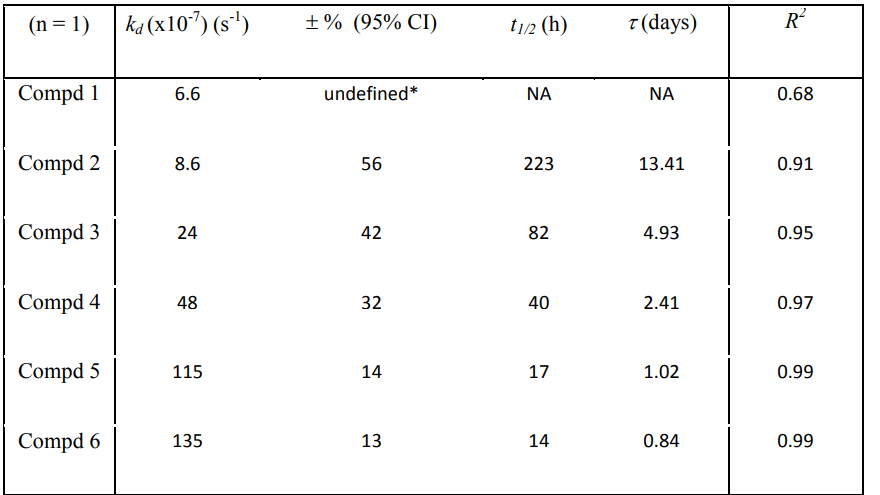
IL-13 vs IL-13Ra2超慢解离
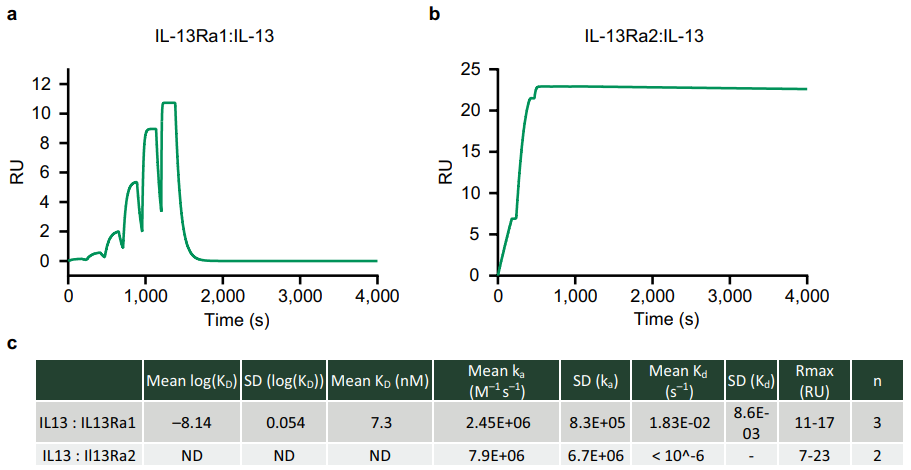
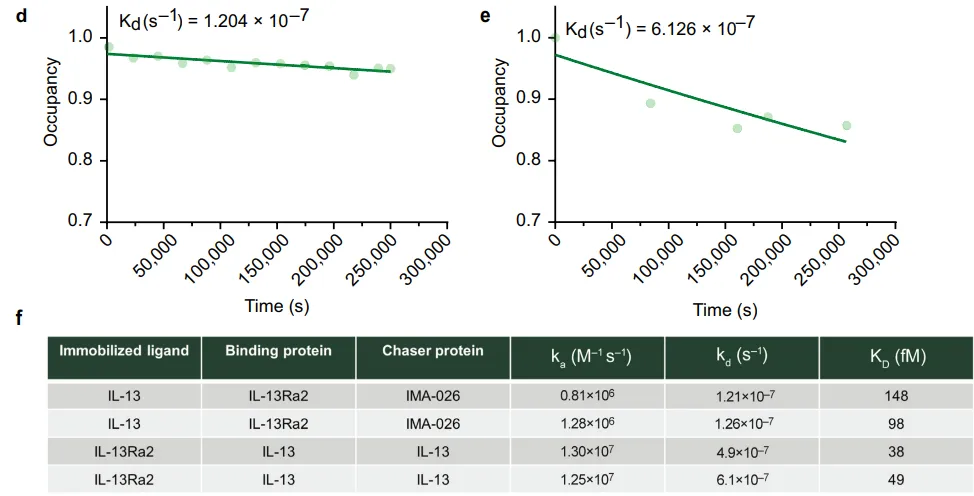
为了阐明曲罗芦单抗通过IL-13Ra2干扰IL-13内源性调节的程度,IL-13 vs IL-13Ra2的亲和力检测迫在眉睫。为此,参考基因泰克2018年发表的文章,作者进一步开发了一种简单而有效的办法:使用分析物本身或抗体作为chaser,引入芯片上配体分子的结合率(occupancy)概念,来计算超长时间(300000 s约3.5 d)的解离速率kd,再将此解离速率代入到常规二元单循环动力学实验中,拟合得到ka和KD【2】。
操作三步曲
饱和结合
首先,在Biacore芯片上固定配体,进样高浓度分析物以达到饱和。此时,芯片表面为“IL-13/IL-13Ra2”复合物。
在不同的解离时间点,进样高浓度chaser。在这个实验中,当IL-13被固定时,chaser是faster-dissociating IL-13R-competitive anti-IL-13 antibody,而当IL-13Ra2被固定时,由于没有合适的抗体,选择了分析物IL-13本身作为chaser!
想象一下,当芯片上的复合物中有分析物自然解离下来后,高浓度的chaser会结合在free的配体上,通过检测chaser的结合信号,即可反推得到此时芯片上配体分子的结合率(occupancy)。而当IL-13作为chaser的实验中,由于chaser本身是慢解离,则使用Biacore 8K的不同channel检测不同解离时间点的occupancy。
需要注意的是,为了排除长时间实验中配体活性变化的影响,chaser assay中,在第一步中设置只捕获配体的对照组以确定实时的配体结合能力。
使用Prism软件绘制occupancy-time并拟合单一指数衰减获得速率常数k,即为解离速率kd。将此解离速率代入到对应的二元单循环动力学实验中,拟合得到ka和KD。
通过Biacore Chaser Assay,研究人员成功测定IL-13与IL-13Ra2的解离速率低到10-7 S-1,亲和力高达38-148 fM。这一数据,为后续所有机制研究奠定了坚实的基础。相关研究于2023年发表。
候选化合物VS靶点超慢解离
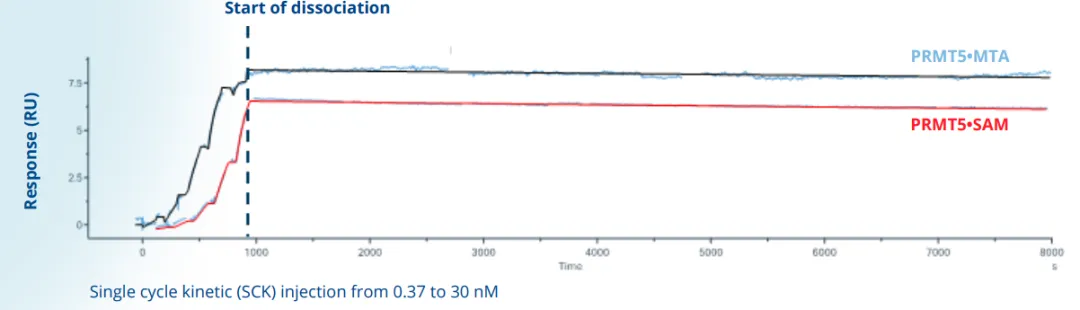
为了明确MRTX1719与PRMT5的亲和力,研究人员引入了与MRTX1719竞争性结合PRMT5的小分子作为chaser,首先在芯片表面构建MRTX1719-PRMT5•SAM/PRMT5•MTA药物-靶点复合物作为三元实验组,PRMT5•SAM/PRMT5•MTA作为二元对照组,在不同时间进样chaser。可以看出,三元实验组通道上,随着解离时间的延长,MRTX1719解离量增加,chaser结合信号提高。通过计算芯片上配体的结合率,来获得解离速率和半衰期数据【3】。
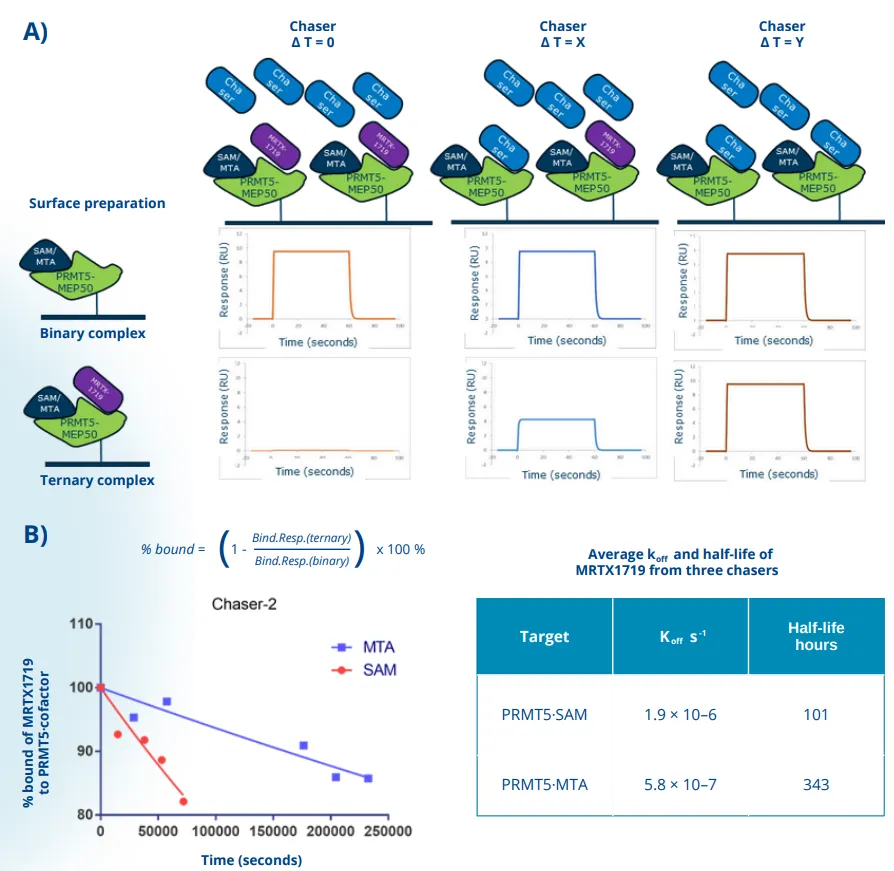
技术是设备的升华,设备是技术的基石!基于设备,又延展了设备检测能力边界的Chaser assay,离不开Biacore长时稳定的流路系统、稳定的芯片,和高灵敏度带来的低RU时依然稳定的信号。