AI+SPR:Science+NCB顶刊教你“玩转”表位识别
1. 针对肽-MHC-I复合物的高特异性binder蛋白设计
针对10个不同的pMHC复合物(涵盖病毒抗原、肿瘤相关抗原、neoantigen),设计并筛选出高特异性结合蛋白。全基因合成后克隆到pET29b(+) 载体中,大肠杆菌表达后,使用Ni柱和凝胶过滤(Superdex 75 10/300GL)两步纯化。
结合动力学分析在Biacore8K通过Biotin CAPture Kit捕获法完成。捕获生物素化的肽-MHC单体约250 RU,蛋白binder(分析物)在HBS-EP+缓冲液中,以30 µL/min 流速进样,浓度范围为1 nM 至1 µM。
结果显示,设计的蛋白与目标 pMHC 的结合亲和力在 几到几十纳摩尔(nM)范围(图1,图2),显示出高亲和力。
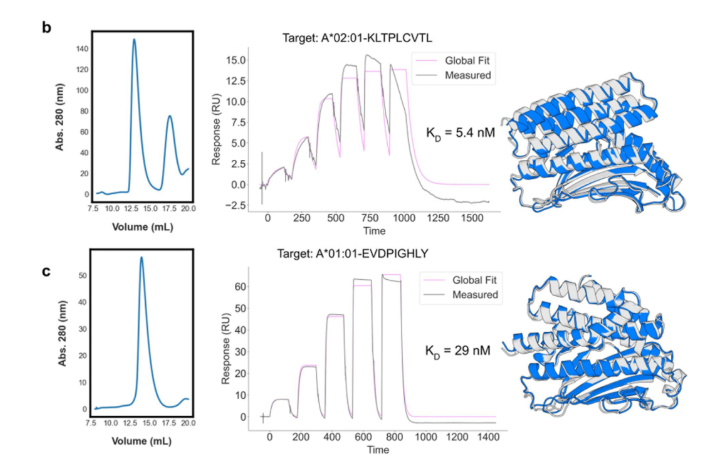
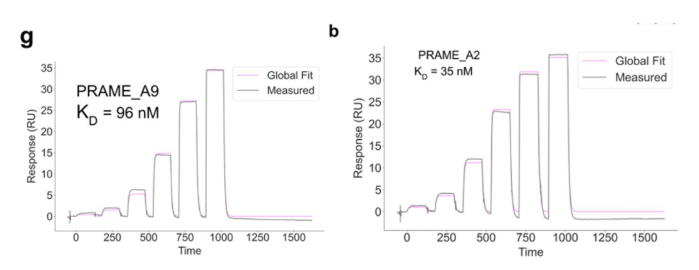
▶ Biotin CAPture Kit方案:轻松搞定生物素化配体可逆捕获!
此外,我们的新品Biacore cap-tag捕获试剂盒,通过独特的寡核苷酸标签(cap-tag)技术,无需依赖传统标签,即可将目标蛋白高效捕获到传感芯片上,可参考:
2. 利用深度学习精确设计单域蛋白支架呈现三个非重叠表位
诺奖得主David Baker团队在Nature Chemical Biology上发表文章,利用深度学习方法(RoseTTAFold、RFjoint2 Inpainting)和ProteinMPNN,设计了小型单域免疫原(小于130 aa),在一个支架上呈现三个RSV(呼吸道合胞病毒)融合蛋白表位(II、IV、V)。
设计的免疫原支架全基因合成后克隆到pET11b载体中,E. coli BL21 (DE3)表达后,使用Ni柱和凝胶过滤(HiLoad 16/600 Superdex 75 column)两步纯化。
RSVF蛋白ExpiCHO细胞表达,使用Ni柱,StrepTrap HP affinity column和凝胶过滤(Superdex200 Increase 10/300 GL column)三步纯化。
抗体IgG和Fab蛋白HEK-293T细胞表达,使用5 ml HiTrap Protein A HP 柱纯化IgG,使用5 ml kappa-select 柱纯化 Fab,通过Superdex200 Increase 10/300 GL柱进行 凝胶过滤进一步纯化。
SPR测定在Biacore 8K仪器上使用CM5芯片完成。固定设计的免疫原支架以及 RSVF 三聚体,流过Fab抗体(图3)。或者固定各种IgG ,流过设计的单体蛋白(图4)。分析物3倍或6倍梯度稀释进样,结合120s,解离600s,使用0.1 M Glycine (pH 3.0)再生。
结果显示,单表位设计(RSVFV-1 至 RSVFV-4):KD 范围:54–241 nM(比天然 RSVF 三聚体的0.9 nM 差约50倍,但比之前报道的设计0.9 μM提高约20倍)。
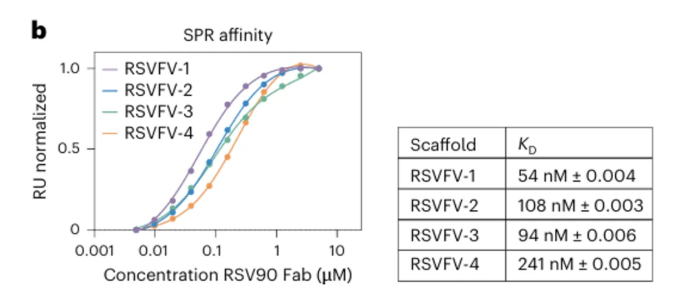
- Site II(motavizumab):14–47 nM(天然 RSVF ~15 pM);
- Site IV(101F):343–890 nM(天然 RSVF ~2 nM);
- Site V(RSV90):>1 μM(天然 RSVF ~0.9 nM)。
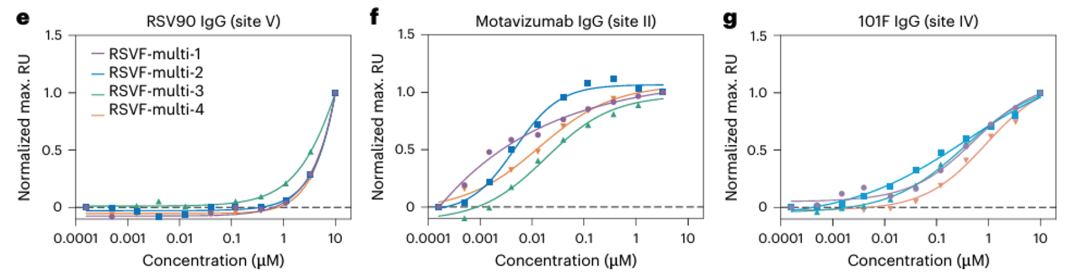
3. 抗体结构引导的in silico表位疫苗设计——针对新兴病毒诱导强效免疫应答
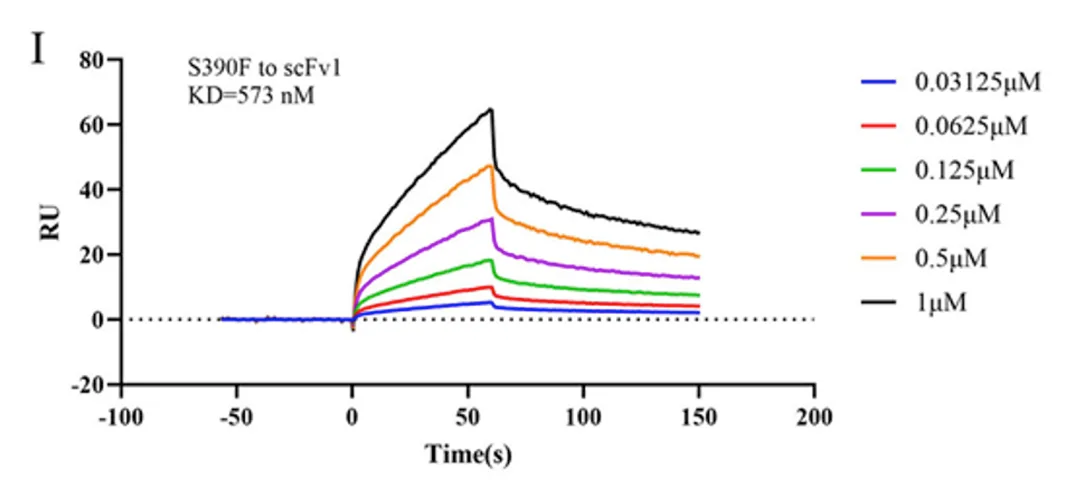
研究使用计算机辅助设计结合实验验证:通过ELISA、Western blot、免疫组化、SPR等方法验证表位与抗体结合能力及免疫效果。SPR测定在 Biacore T200仪器上使用CM5芯片完成。将 S390F肽通过氨基偶联固定在FC2上,FC1作为参比。运行缓冲液为1×PBS(pH 7.4)+5% DMSO。通过不同浓度的DMSO(4.5%–5.8%)自动生成溶剂校正曲线。将稀释后的抗体scFv1进样,使用10 mM Gly-HCl(pH 2.0)再生。

 收藏
收藏 询价
询价