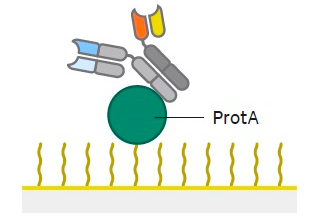
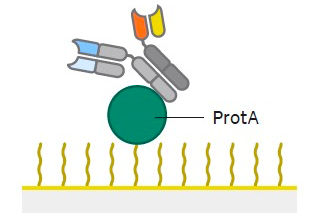
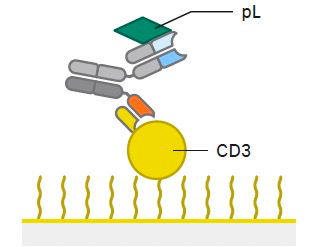
单域抗体研究“多面手” :Biacore助力对抗肉毒杆菌毒素
单域抗体研究“多面手” :Biacore助力对抗肉毒杆菌毒素
肉毒杆菌毒素(Botulinum toxin,BoNT)是一种由厌氧细菌产生的剧毒物质,会导致神经麻痹,目前没有官方批准的特效药。
单域抗体(sdAbs)由于其高亲和力、稳定性、溶解性和组织渗透性,被认为是对抗BoNT的很有潜力的候选药物。
2025年2月北京药理毒理研究所,首都医科大学附属北京友谊医院北京热带医学研究所等单位在《Heliyon》发表文章,报道了他们获得的一种针对肉毒杆菌毒素A(BoNT/A)的单域抗体(sdAbs)。
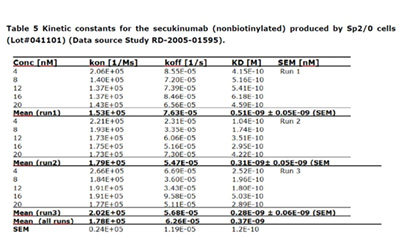
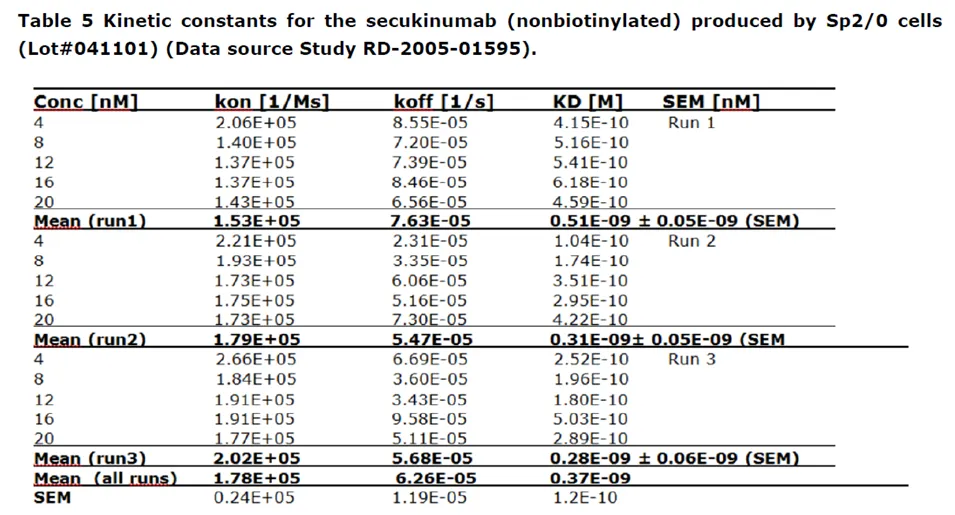
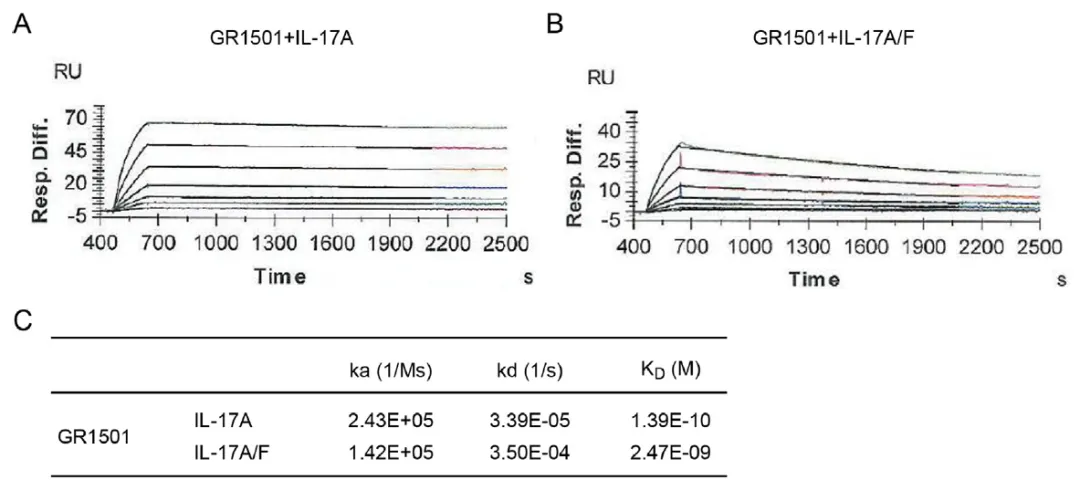
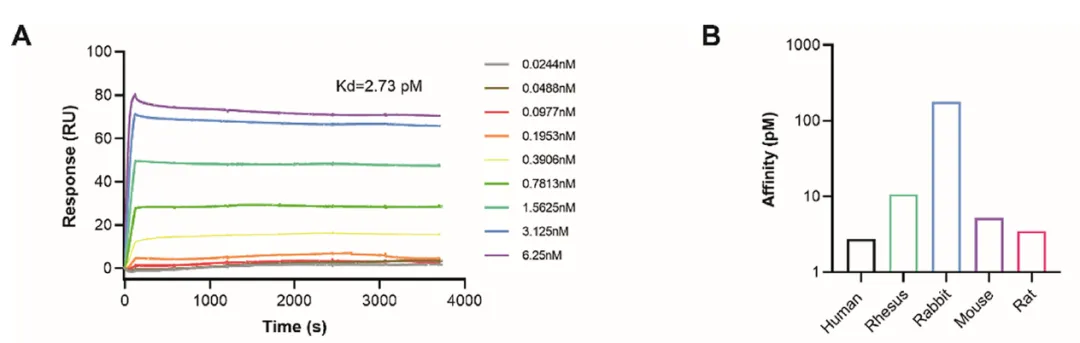
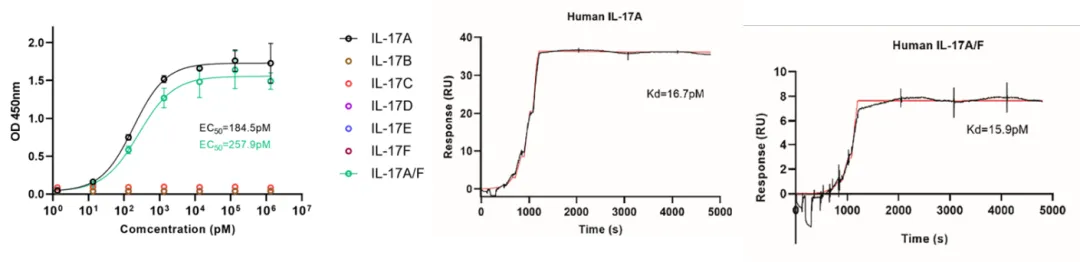
研究人员使用BoNT/A的受体结合域(BoNT/AHCC)免疫双峰驼,构建了纳米抗体噬菌体文库。从文库中得到的抗体A1与BoNT/AHCC具有高亲和力(KD=3.624E-10M,图1)。
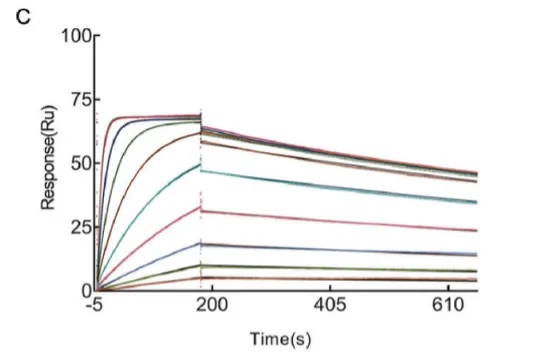
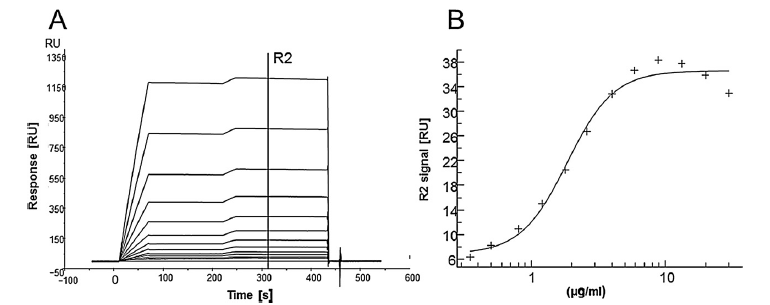
图1:SPR分子互作系统检测抗体A1与AHCC的亲和力
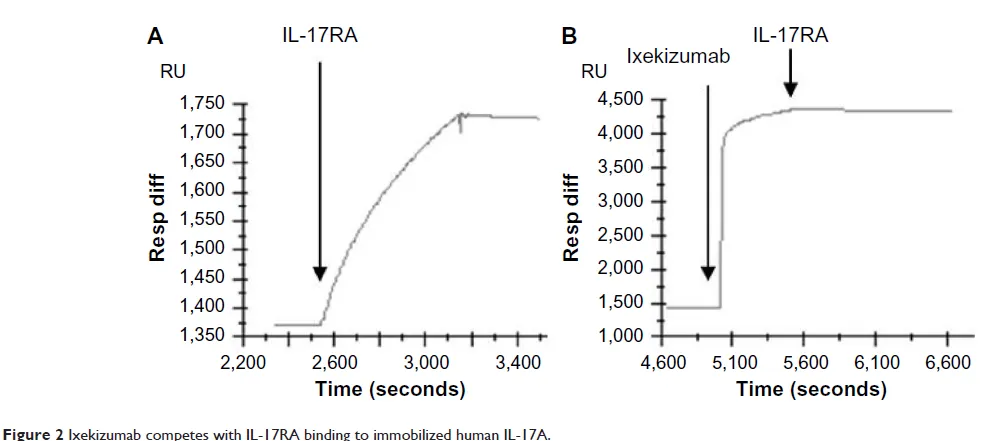
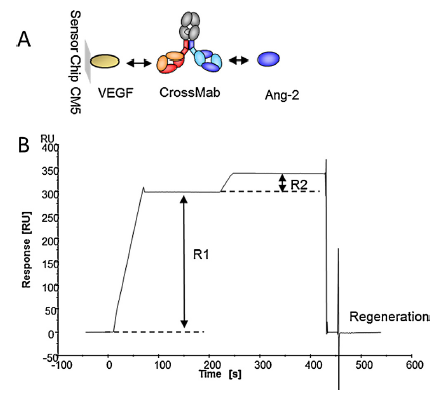
在CM5芯片上固定SV2C,测定与BoNT/AHCC的亲和力为6.539E-8M(图2A),接着将A1抗体与BoNT/AHCC混合作为流动相,随着A1抗体浓度的增加,Ru值并没有减弱(如果A1抗体能够阻止BoNT/AHCC与SV2C的结合,那么随着A1抗体浓度的增加,BoNT/AHCC与SV2C的结合信号会减弱),反而增强了(图2B)。
这表明A1抗体并不能阻止BoNT/AHCC与SV2C的结合,进一步的分析表明,A1抗体结合到了BoNT/AHCC的非活性位点,远离SV2C的结合位点。
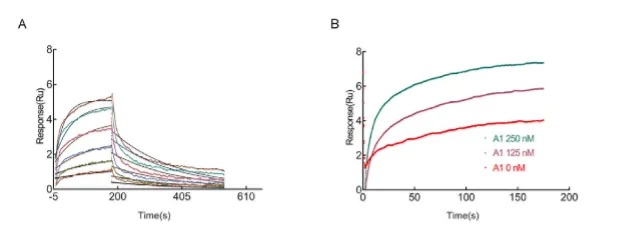
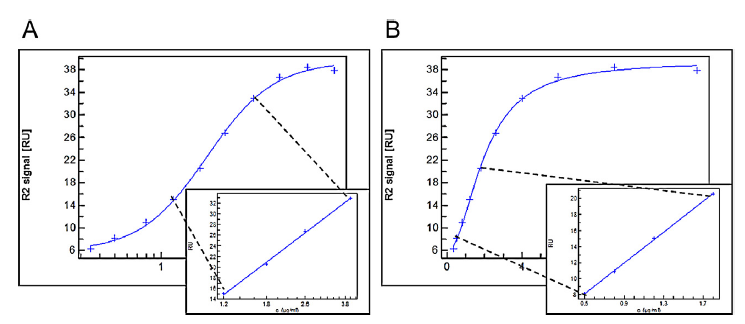
图2:SPR分子互作系统竞争实验测定A1抗体的中和能力
虽然A1抗体并不是一种能够中和BoNT/A的抗体,但研究人员利用A1抗体开发了一种间接筛选策略,即将A1抗体涂覆在免疫管上,利用A1抗体与BoNT/AHCC的高亲和力来捕获毒素,然后,加入噬菌体文库,使得噬菌体展示的VHH抗体有机会与BoNT/AHCC的活性位点结合,从而筛选出了能够有效中和BoNT/A的抗体。
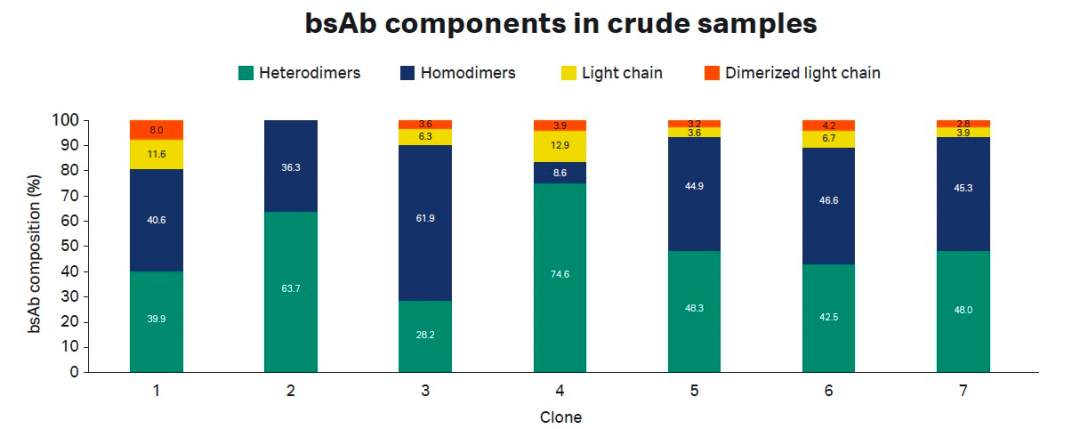
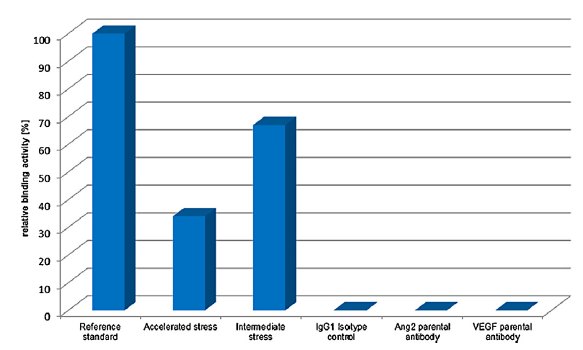
接下来研究人员用SPR筛选阳性克隆,直接将Anti-M13固定在CM5芯片表面,与噬菌体反应从而将抗体捕获在芯片表面,然后进样BoNT/AHCC,用Stability报告点的响应值作为筛选标准,有8个克隆展现较高响应值(图3),进一步对这8个克隆进行Fc融合并在293T细胞中真核表达。

图3:SPR分子互作系统筛选中和抗体
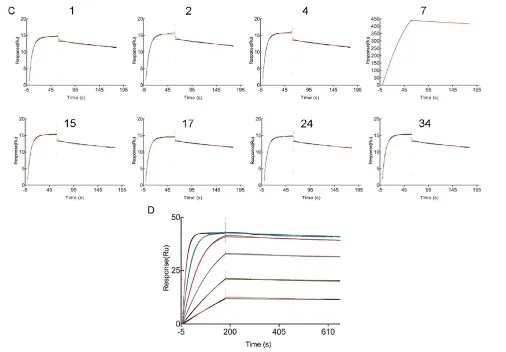
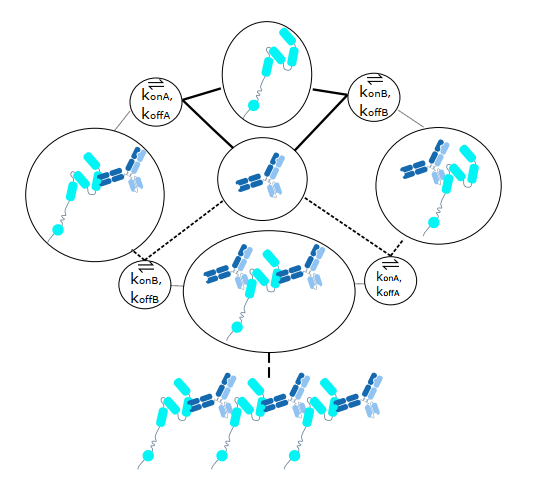
图4:SPR分子互作系统筛选细胞上清(上)及表征纯化的抗体(下)
和之前A1抗体的表现不同,随着HM抗体浓度增加,Ru值下降,这表明HM抗体可以阻断AHCC和SV2C的结合(图5)。
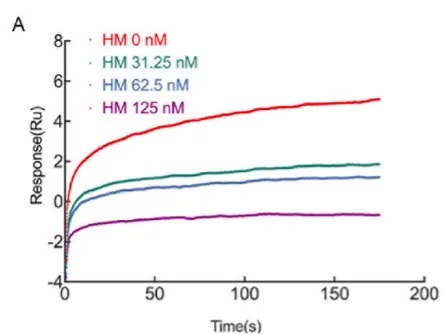
图5:SPR分子互作系统竞争实验测定HM抗体的中和能力
纵观整篇文章,HM抗体是通过间接筛选策略,从免疫双峰骆驼产生的噬菌体文库中成功分离得到的。
这种筛选策略强调了保持抗原的正确构象和暴露关键表位的重要性,为开发针对BoNT/A的特效药物提供了新的思路,而其中SPR技术在抗体筛选,亲和力表征,以及中和能力测定方面展现了“多面手”的强大实力:
- 细胞上清,噬菌体,纯化抗体,各种样品类型“通通拿下”
- 拥有mM-fM亲和力检测范围的Biacore分子互作系统,轻松测定A1/HM与AHCC的亲和力
- 不仅是测定亲和力和筛选抗体的一把好手,还能研究抗体的中和能力

 收藏
收藏 询价
询价