2022年2月,
中国农业大学韩振海、吴婷老师团队在著名植物学期刊《Plant Cell》发表了关于苹果果皮褪绿机制的最新研究成果“
Phosphorylation of MdERF17 by MdMPK4 promotes apple fruit peel degreening during light/dark transitions”。该研究发现,MdMPK4与MdERF17结合并使其磷酸化,进而调控苹果褪绿过程,并且这一过程受昼夜的光照影响。研究团队
利用Biacore鉴定了MdMPK4与MdERF17的结合,并且利用Biacore发现不同MdMPK4与MdERF17之间结合能力的差异,为文章的关键发现了提供了重要数据。
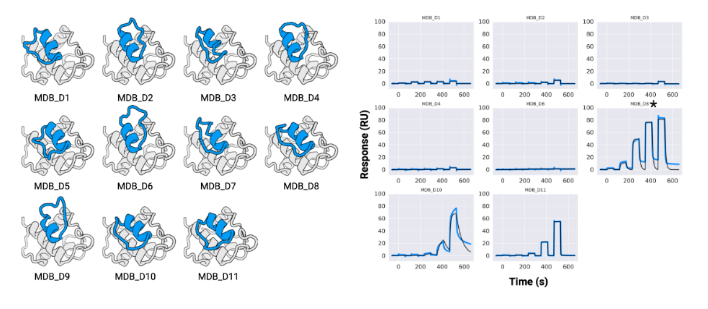
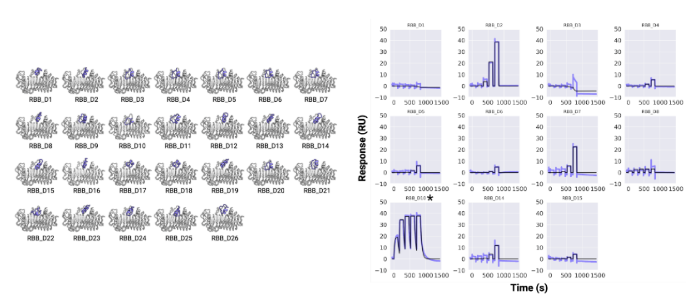
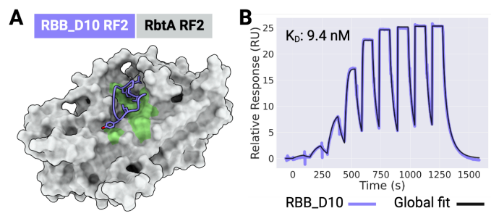
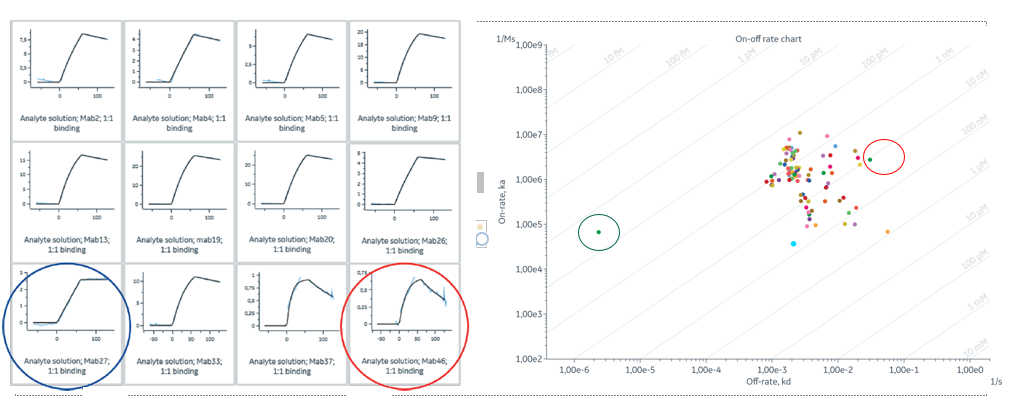
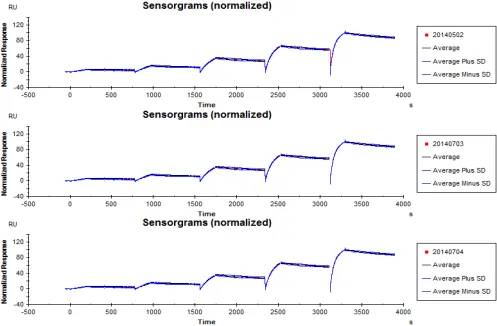
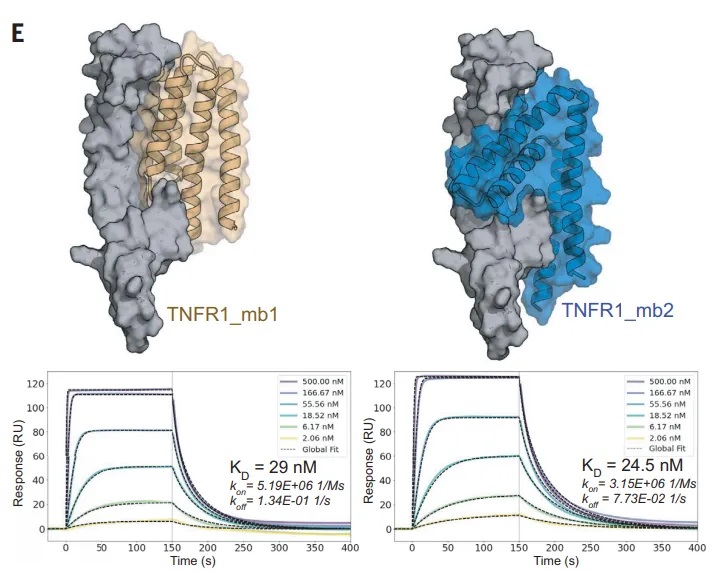
苹果变红包括叶绿素降解(褪绿)和花青素积累。早在2018年,韩振海、吴婷老师团队发表在《Plant Physiology》的研究成果中,就发现乙烯响应因子ETHYLENE RESPONSE FACTOR17 (MdERF17)通过结合褪绿相关基因PPH、NYC的启动子来调控褪绿过程,其中Biacore提供了MdERF17与启动子结合的关键信息。近期文章中,作者首先利用免疫印迹法鉴定出与MdERF17相互作用的激酶MAP KINASE4(MdMPK4),利用Biacore T200,将MdMPK4固定在CM5芯片上,使MdERF17流过芯片表面检测动力学/亲和力,结果明确了MdMPK4-06G/14G与MdERF17-8s/3s的相互作用(图1)。
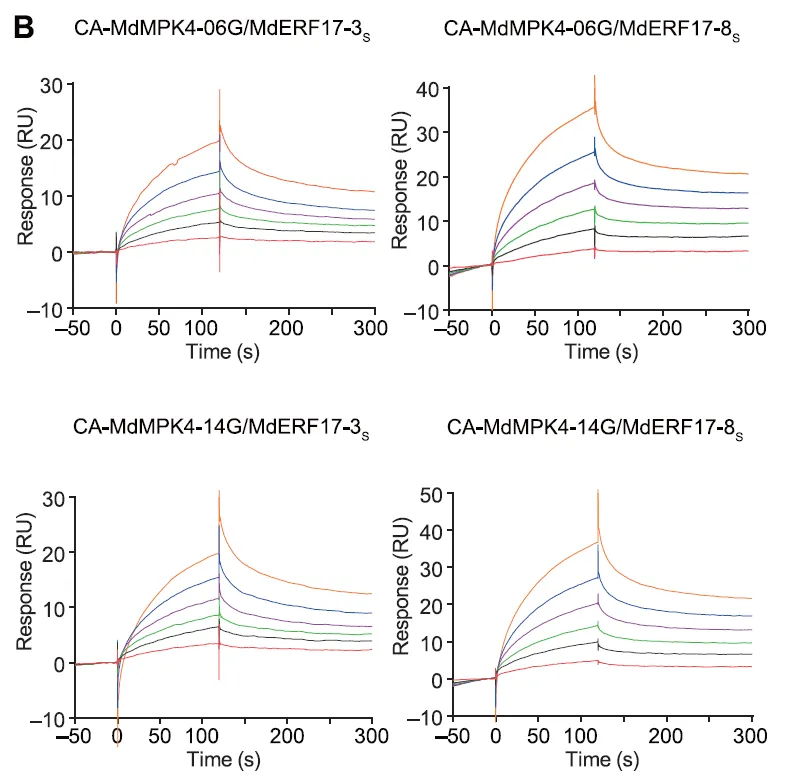
图1 Biacore检测MdMPK4与MdERF17的结合能力
随后作者利用免疫印迹和LC-MS发现MdMPK4-14G可以在Thr67位点磷酸化MdERF17-8s,而MdMPK4-06G则不能,这为后续昼夜调控的研究埋下了伏笔。沿着前文研究的信号通路,作者设计了以MdMPK4-14G和MdERF17为效应子,以PPH-LUC、NYC-LUC为报告基因来检测体内的互作,发现只有在MdERF17受MdMPK4-14G磷酸化后才会激活下游PPH、NYC的转录。
为了进一步研究这一机制对叶绿素降解的调节,作者比较转入了空载或MdERF17的苹果果实,发现转入MdERF17的果实中PPH、NYC表达水平升高,叶绿素含量降低,且这一现象仅在MdERF17能被磷酸化的一组中出现,说明MdERF17的磷酸化促进了叶绿素的降解。
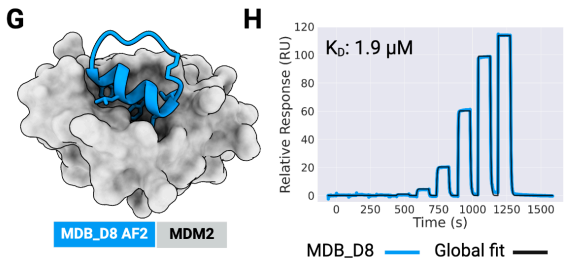
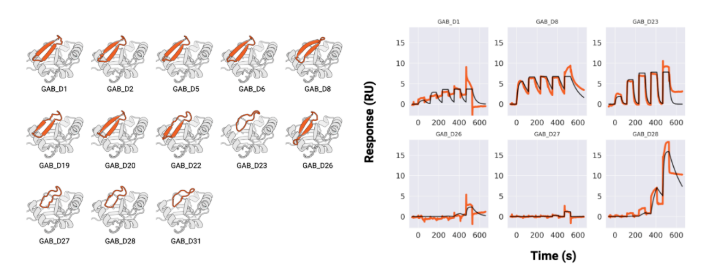
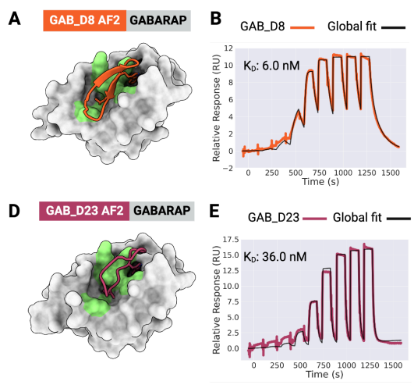
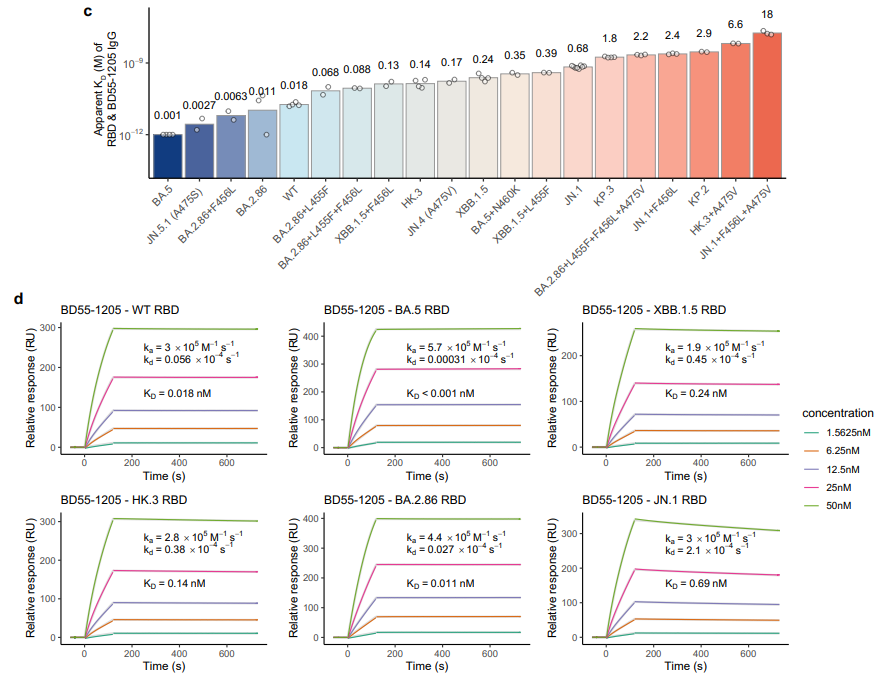
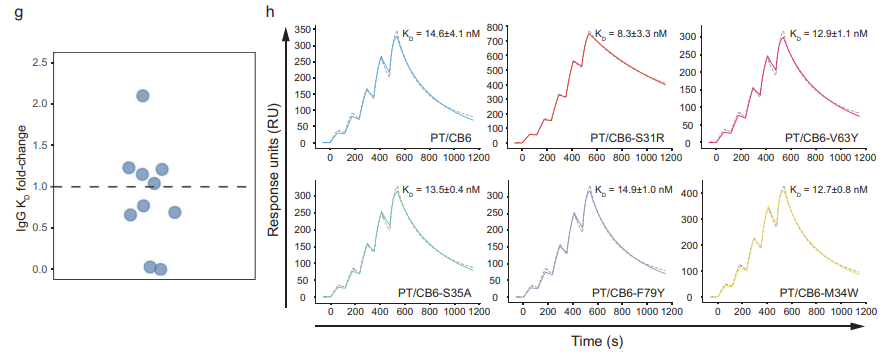
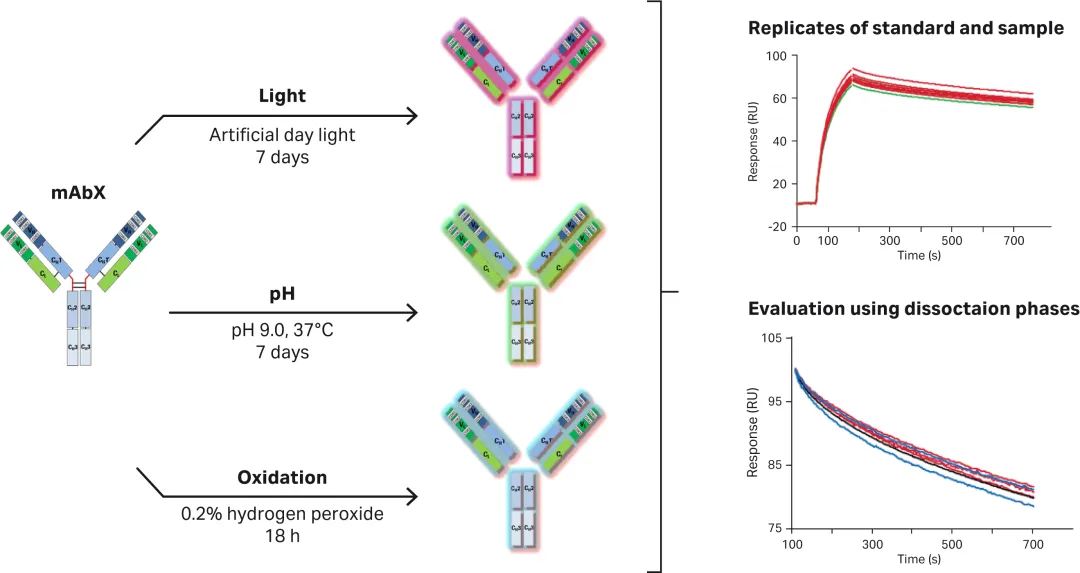
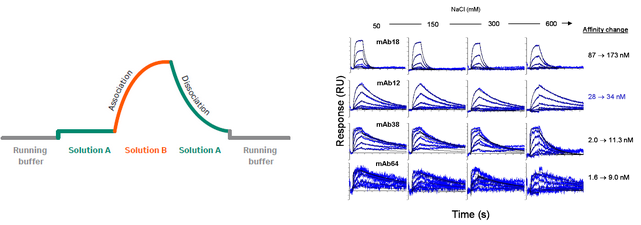
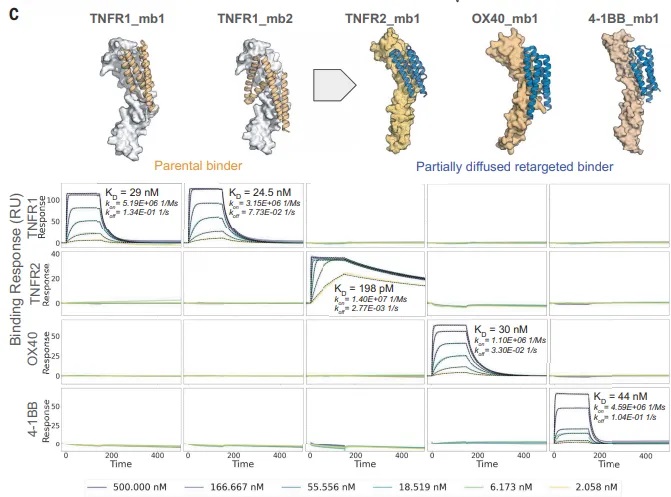
研究团队之前的文章中利用Biacore发现ERF17基因重复编码区,丝氨酸残基增多,对下游叶绿素降解相关基因PPH、NYC启动子的结合能力和稳定性也随之增强(图2)。本文同样利用Biacore研究了不同长度丝氨酸的影响,在Biacore结果发现MdERF17-8S与MdMPK4的亲和力更强(表1)之后,作者选择了MdERF17-3S纯合子的紫塞明珠和MdERF17-6S/8S的红富士,发现果实成熟期间叶绿素降解与MdERF17磷酸化呈现正相关的关系,进一步说明MdERF17重复编码区中丝氨酸个数与其磷酸化和下游叶绿素降解的关系。
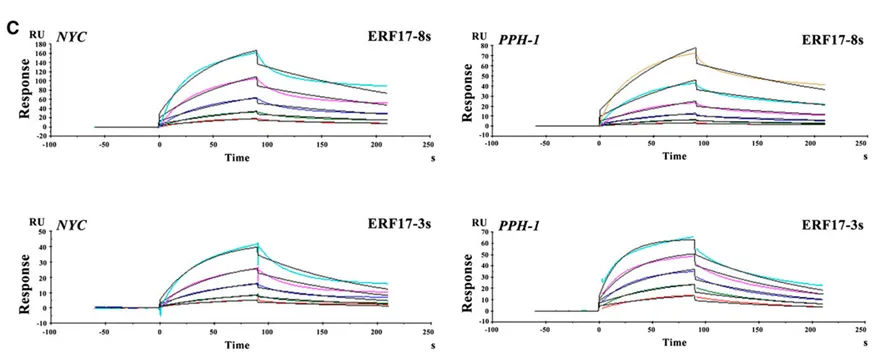
图2 Biacore检测发现ERF17中重复丝氨酸的数量影响与下游启动子的结合能力
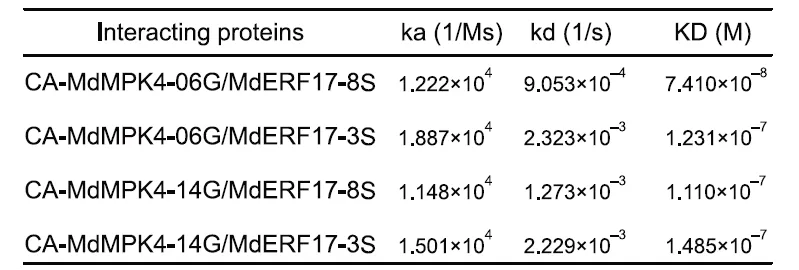
表1 Biacore 测定MdERF17与MdMPK4的动力学参数
聊完了MdERF17,继续关注上游的激酶MdMPK4。前面提到,MdMPK4-14G可以磷酸化MdERF17,而MdMPK4-06G则不能。作者进一步比较MdMPK4-14G和MdMPK4-06G启动子上游的基因序列后,发现MdMPK4-14G独有一个昼夜节律相关的原件。由此团队研究了白天和夜晚时MdMPK4-14G的表达水平,蛋白丰度及MdERF17的磷酸化水平,发现MdMPK4-14G是个不折不扣的夜猫子!不仅在晚上表达水平高,蛋白丰度高,引起的MdERF17的磷酸化程度也更高。作者对嘎啦苹果过程成熟中进行持续暗处理,发现MdMPK4-14G直接参与黑暗条件下叶绿素的降解。
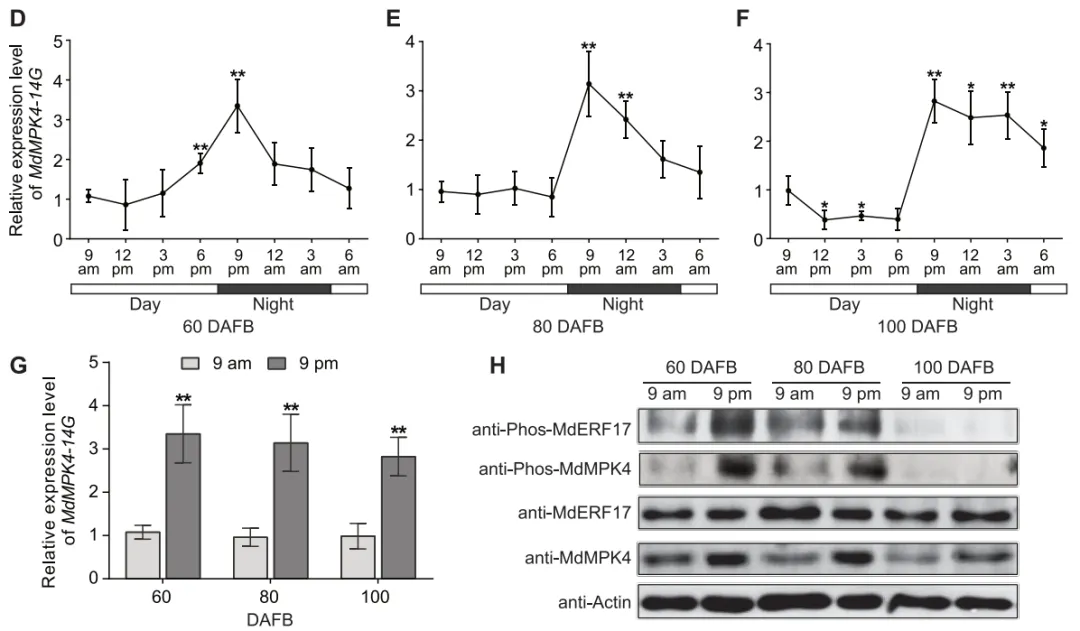
图3 黑暗条件下MdMPK4-14G的表达水平和磷酸化能力提高
至此,脉络逐渐清晰起来。基于大量的研究成果,作者提出了一个调控苹果变色的模型(图4)。晚上黑暗条件下,MdMPK4-14G带领着下游分子工作,降解叶绿素,给苹果褪绿,白天光照时,MdMPK4-14G休息,轮到MdMPK4-06G上场,积累花青素给苹果着红色。生物分子受光调节,同心协力,才结出了红的黄的绿的苹果,地球日过去不久,希望大家一直珍惜粮食呀!
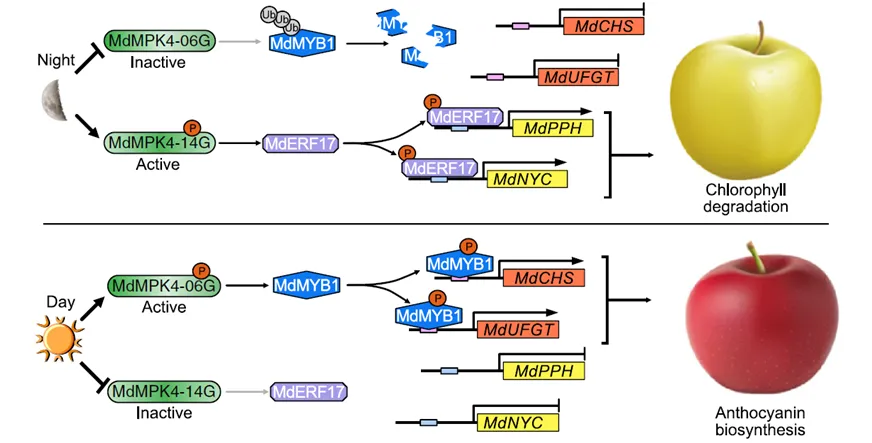
图4 苹果果实中MdMPK4-14G介导的MdERF17磷酸化调控叶绿素降解
植物学的研究总是厚积薄发,并且关系着农业、食品、环境、药物等等,哪一个都与我们的生活息息相关。从生长发育机制到抗逆,从天然活性成分的发现到农残检测,Biacore一直全力支持着植物学研究者。劳动节刚刚过去,北方夏收即将到来,在这里祝农民朋友,科技工作者,参与粮食生产的每一位劳动者丰收!


 收藏
收藏 询价
询价