Biotin CAPture Kit方案:轻松搞定生物素化配体可逆捕获!
Biotin CAPture Kit方案:轻松搞定生物素化配体可逆捕获!
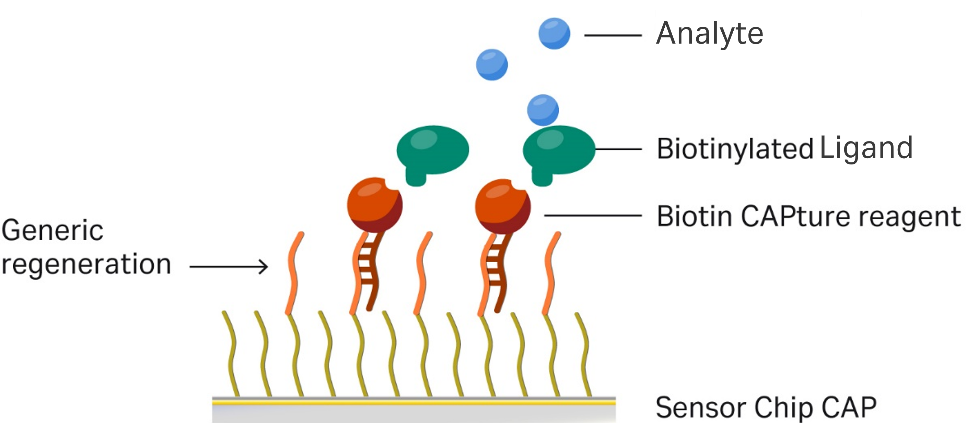
什么是Biotin CAPture Kit?

“Inject and elute”是一个强大的功能模块,它可以用来从传感器芯片的配体上洗脱结合的分析物,并将其收集到目标样品管中。通过重复的“上样-洗脱-回收循环”,可以将目标组分从复杂的样品溶液中“钓出”,并显著提高其浓度,从而方便进行后续的成分鉴定及分析。
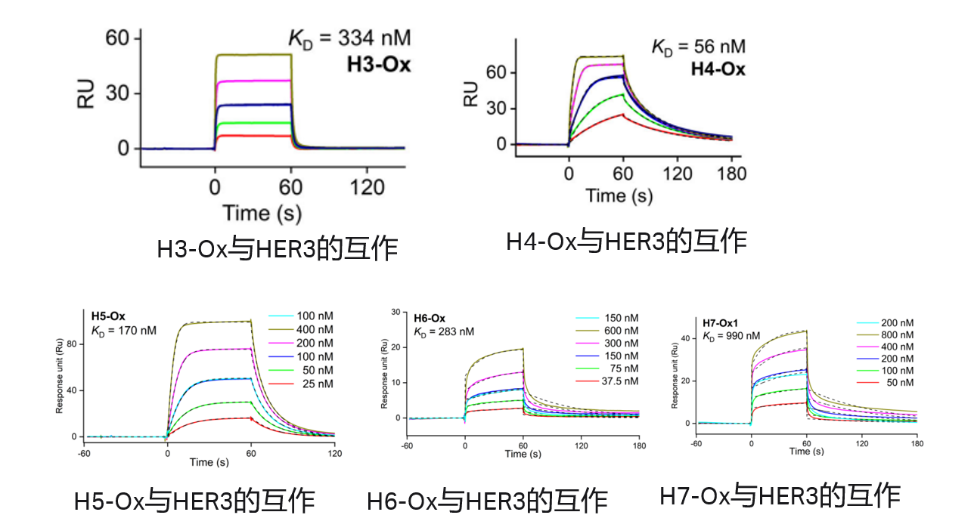
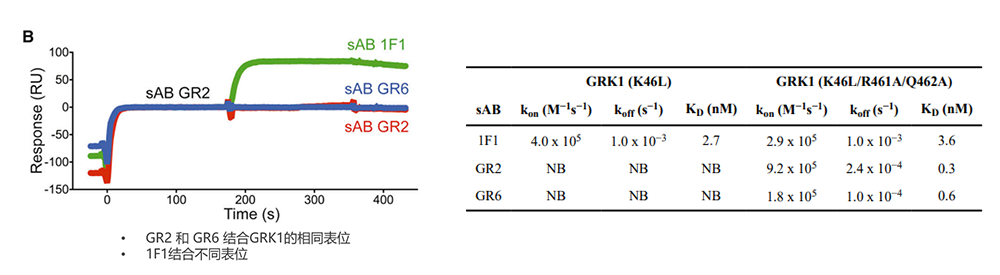
检测抗体和GPCR的互作
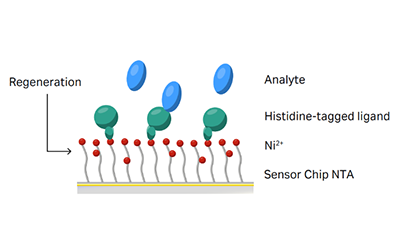
Biotin CAPture Kit
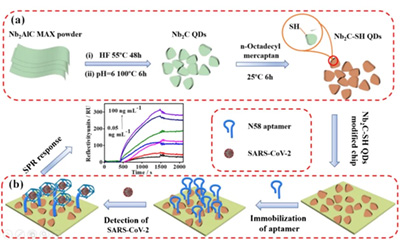
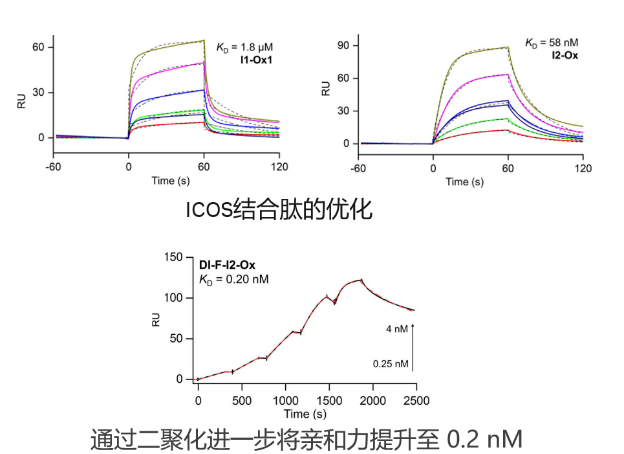
检测多肽/小分子和蛋白的互作
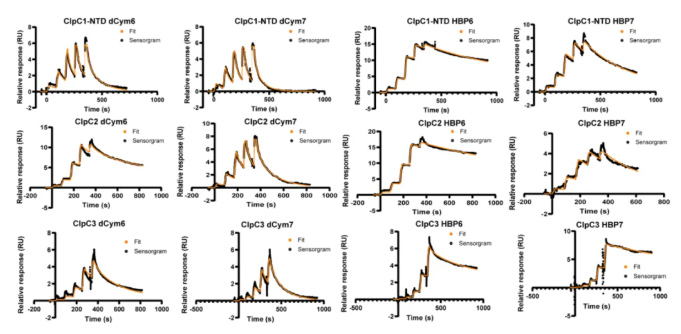
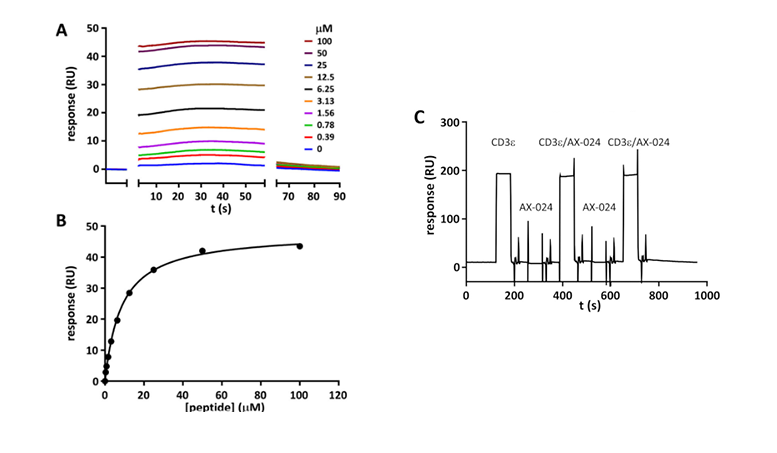
结果表明接头蛋白Nck与TCR的CD3ε亚基结合,对TCR信号传导至关重要,但AX-024并未与Nck1-SH3.1直接结合,其作用机制可能并非通过抑制Nck/TCR相互作用来实现,AX-024的确切靶点仍需进一步研究。

 收藏
收藏 询价
询价