4月15日,第28届全国肿瘤防治宣传周正式展开,本次宣传主题为“整合资源,科学防癌”。活动响应《“健康中国2030”规划纲要》要求,首次将宣传重点推向了 “科学防癌,关口前移”、“关注早筛,防患未然”等方面。根据世界卫生组织国际癌症研究机构发布的2020年全球最新癌症数据,2020年我国癌症新发病例457万例,每分钟有8人被确诊癌症!通过此次宣传,中国抗癌协会旨在推动癌症防治,倡导做到早预防、早发现、早诊断、早治疗,降低癌症发病率和死亡率。
肝细胞癌(Hepatocellular carcinoma,HCC)是最常见的原发性肝癌,是全球发病率前十的癌症之一,但它却是全球第二大癌症死亡原因(占所有癌症死亡的9.1%)。肝癌防治过程中最大的挑战,便是往往就诊已晚期,失去接受根治性手术的机会。因此完善肝癌早期筛查对于挽救肝癌患者至关重要。检测血清生物标志物是早期HCC筛查的关键手段。一系列用于HCC诊断的血清生物标志物已被报道,如甲胎蛋白(AFP),脱氧-γ-羧基凝血酶原(DCP) 、中基蛋白 (MDK)和 Dickkopf-1(DKK1)等。DKK1最早于1998年被发现,是典型Wnt信号通路的分泌拮抗剂,在来自HCC及其他癌细胞系的培养基中可以检测到高水平的DKK1分泌。DKK1早期诊断HCC的敏感性为70.9%,特异性为90.5%,是HCC的潜在诊断标志物,是非常好的早期筛查指标。
复旦大学附属华山医院消化科团队在生物分析化学杂志Talanta发表了题为“Developing Slow-off Dickkopf-1 Aptamers for Early-diagnosis of Hepatocellular Carcinoma”的文章,该团队开发了针对Dickkopf-1的慢解离核酸适配体,可配合抗体形成核酸适配体-靶标-抗体的HCC早期筛查ELISA方法,进一步降低筛查成本,提高筛查的效率。在筛选与改造过程中,Biacore为核酸适配体的筛选指标提供了关键数据。
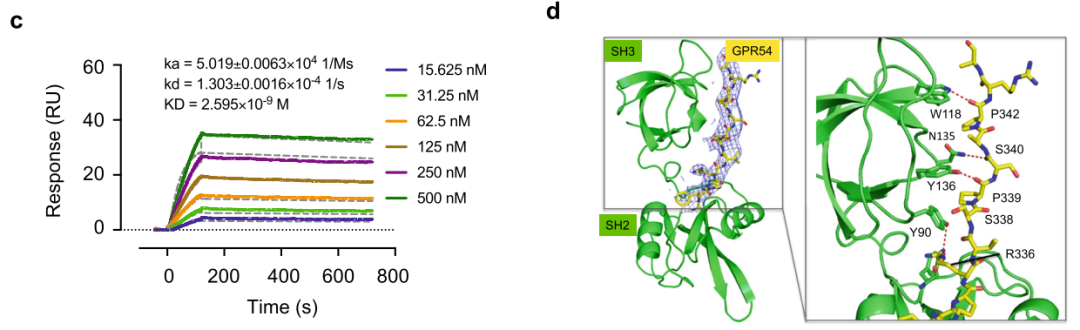
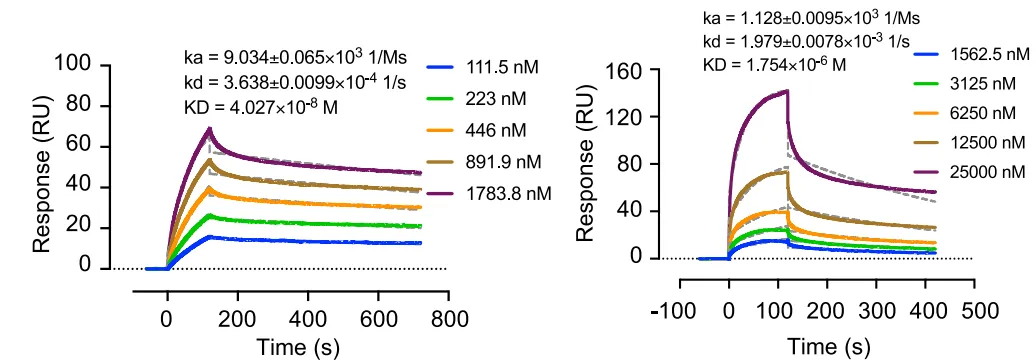
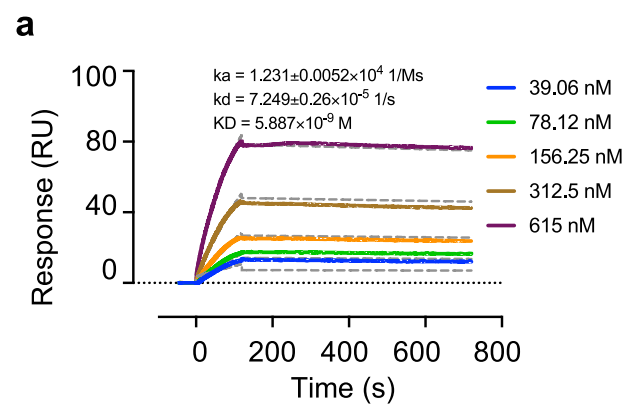
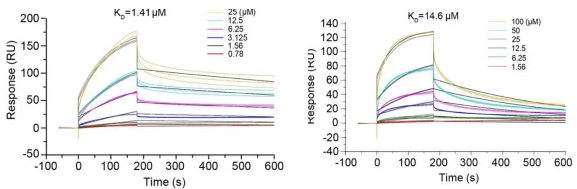
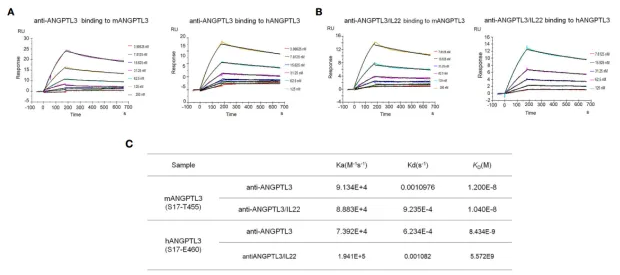
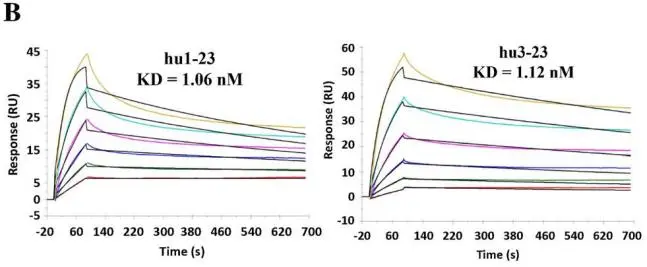
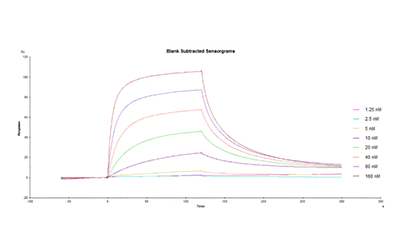
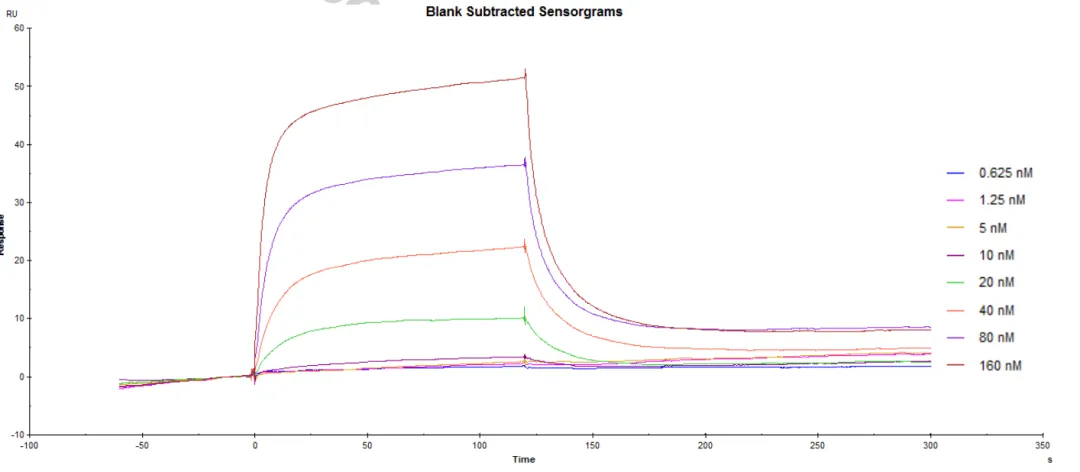
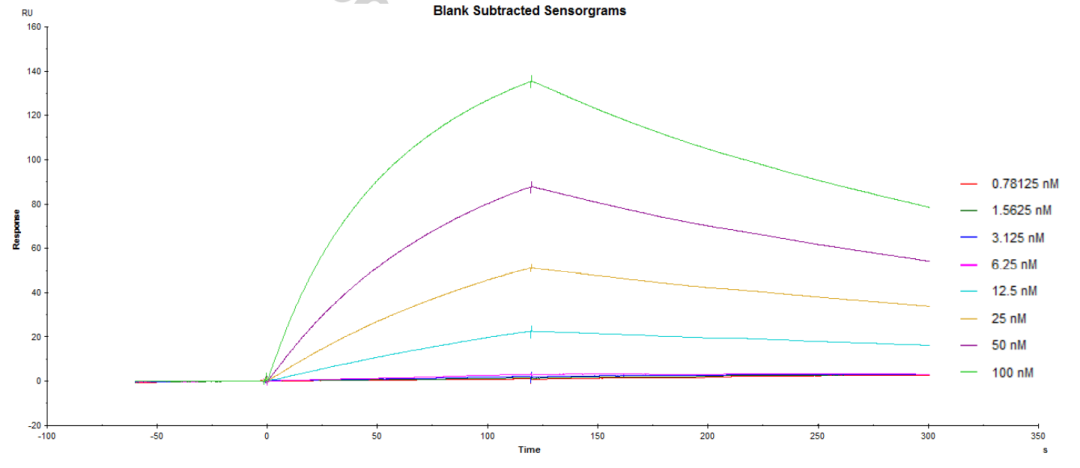
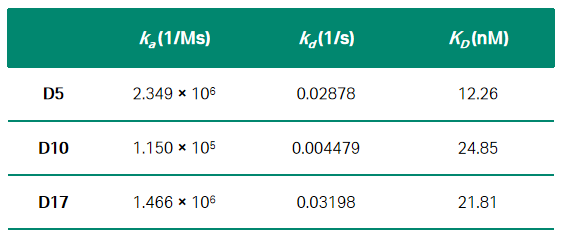
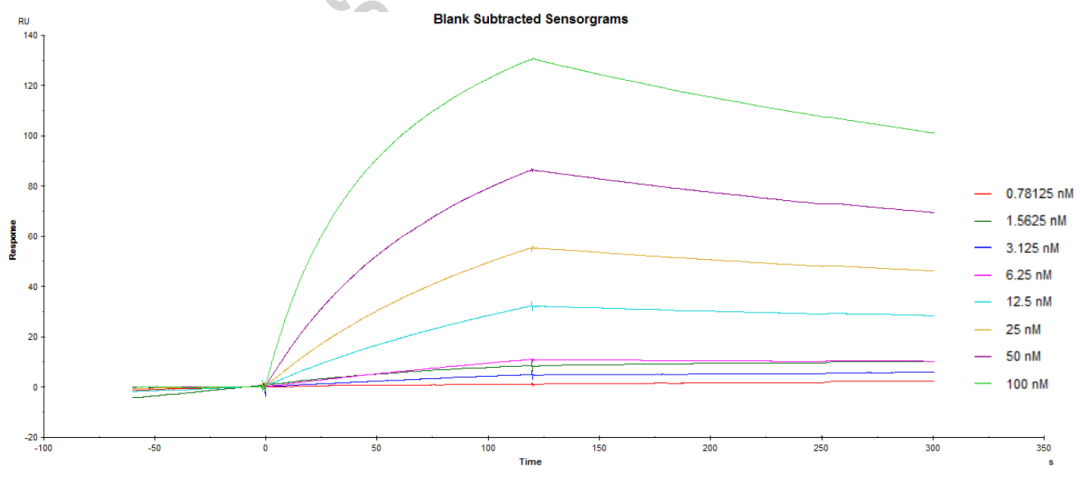
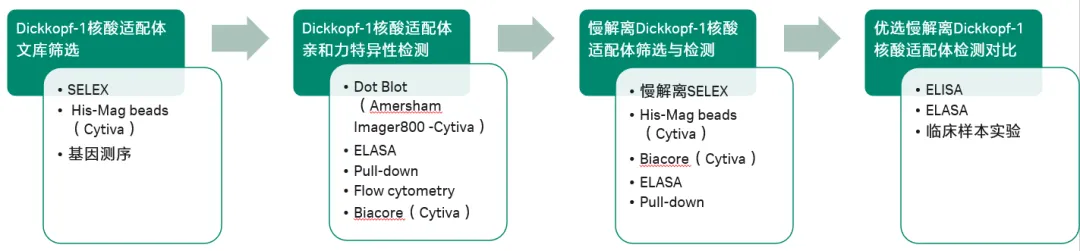
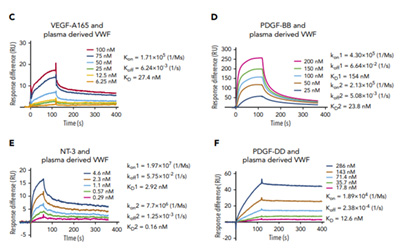
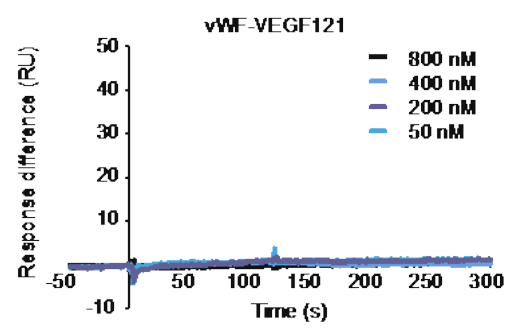
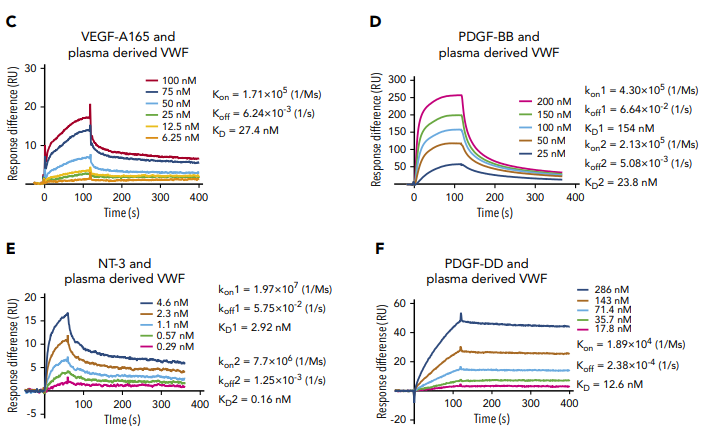
研究人员在以指数富集的配体系统进化技术(Systematic Evolution of Ligands by Exponential Enrichment,SELEX)对DKK1核酸适配体文库筛选后,使用Biacore T200将DKK1固定在CM5传感器芯片上,并将候选适配体作为分析物进行亲和力/动力学检测。如图1、2、3及表1所示,筛选获得的三类核酸适配体D5/D10/D17与DKK1的KD分别为12.26nM、24.85 nM、21.81 nM,均在同一数量级,而三者的解离速率却大有不同,其中D10的kd值是D5和D17的10倍。与快速解离的核酸适配体相比,慢解离的适配体可以大大降低基于适配体的临床ELISA检测的假阴性,极大地提高了HCC早期筛查的准确率与效率。
候选核酸适配体D5(图1 )、D10(图2)与DKK1的亲和力/动力学传感图
检测过程中,研究人员使用了包括点印迹法、酶联核酸适配体吸附试验(ELASA)、Pull-down、流式细胞术和Biacore进行检测。结果表明,不同的方法对相同的序列可能会得到不同结果,相互比较后,
研究者强烈建议通过使用Biacore完成候选适配体性能验证,因为这种方法同时提供实时的动力学信息。
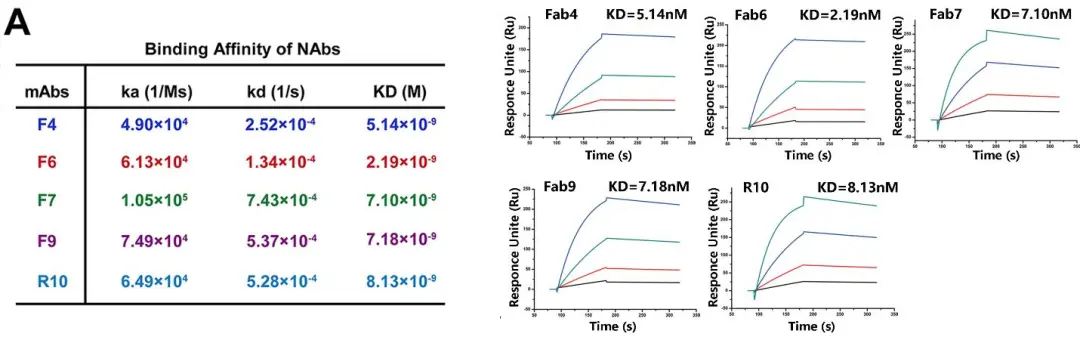
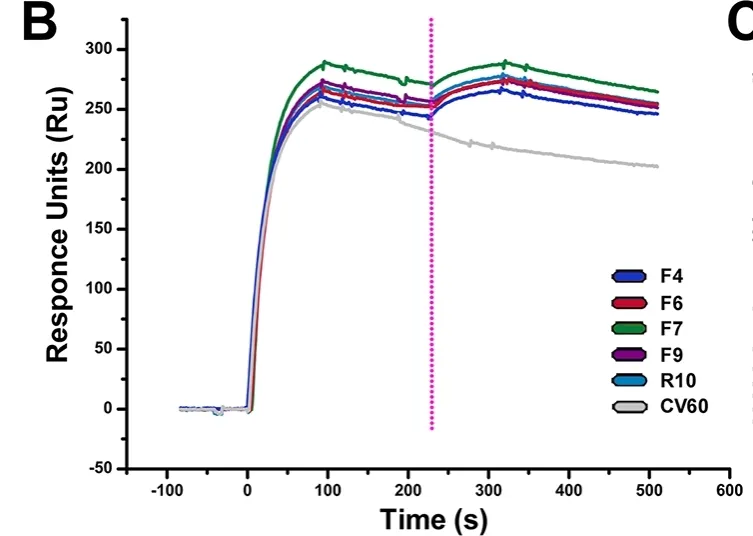
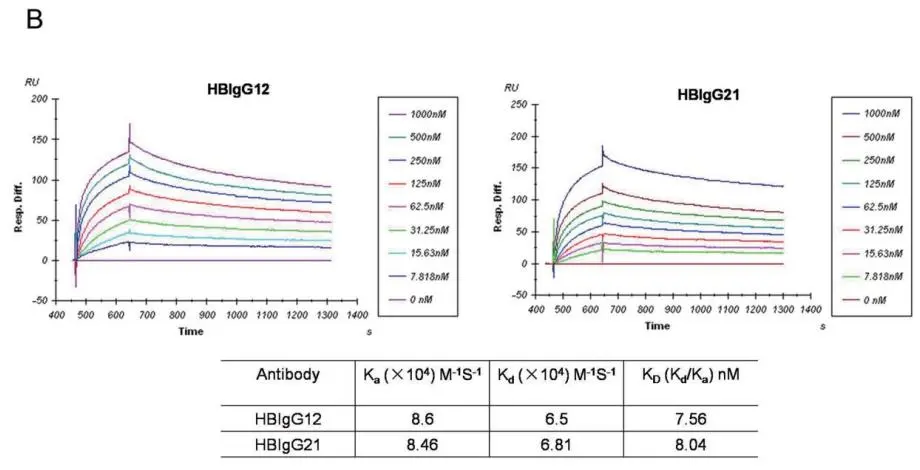
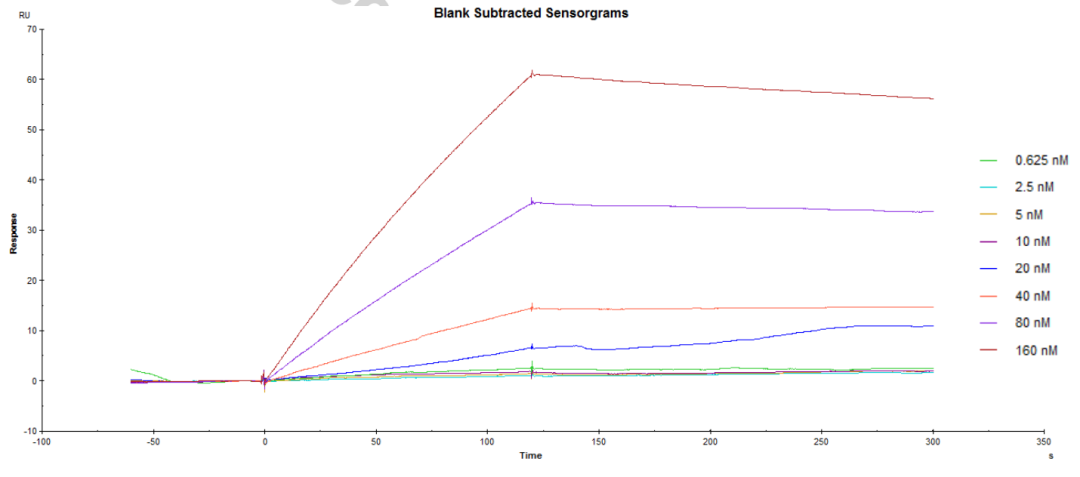
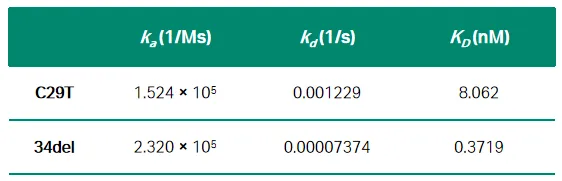
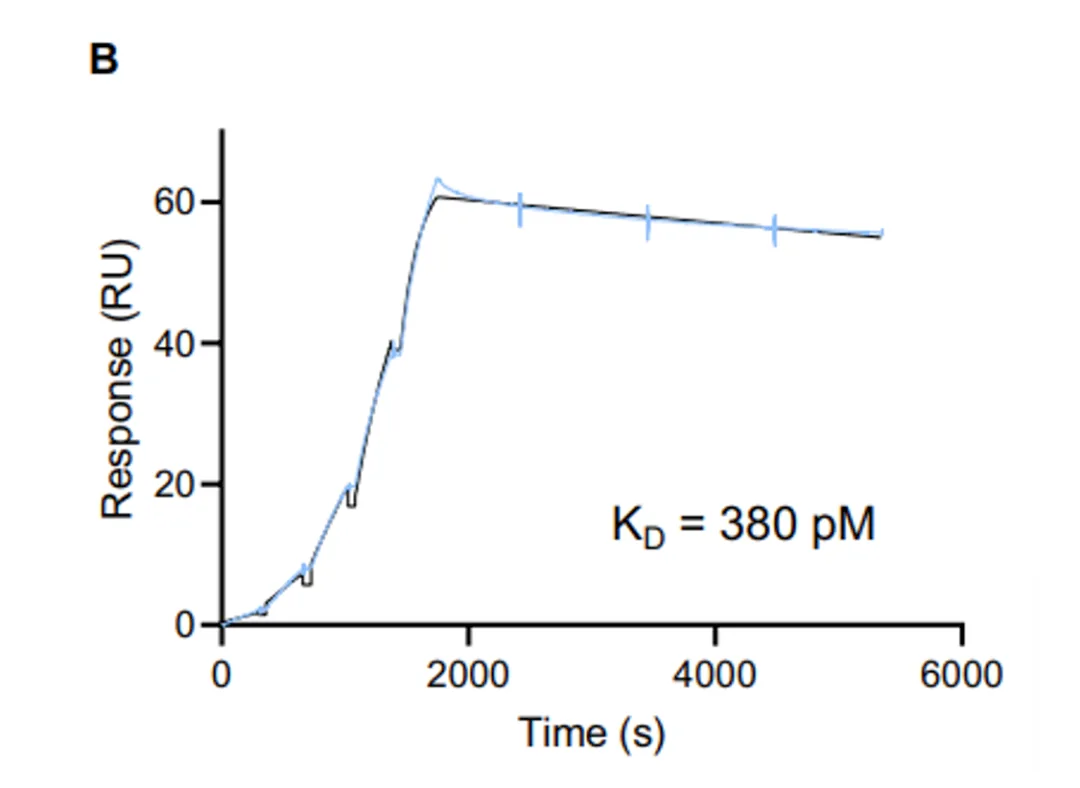
基于对核酸适配体D10的检测结果,对DKK1核酸适配体文库进一步进行慢解离筛选,获得适配体D10的突变体C29T,及C29T基础上34位缺失的34del。研究人员使用Biacore以及上述已固定DKK1的CM5传感芯片,以C29T、34del作为分析物,对全新的候选适配体进行亲和力/动力学检测,结果如图4、5及表2所示。候选核酸适配体C29T与34del的KD分别为8.062nM、371.9 pM,比适配体D10的亲和力提高了3.1倍和66.8倍。除此之外,适配体34del的kd已经达到了7.374×10-5s-1,获得了极慢解离的核酸适配体。在对其进行结构预测后,证明截短序列可以进一步提高结合能力,并在其基础上进一步截短,获得全新优化的核酸适配体TD10,将其用于后续HCC筛查。
候选核酸适配体C29T(图1)、34del(图2)与DKK1的亲和力/动力学传感图
表2 慢解离候选核酸适配体与DKK1的亲和力/动力学
后续实验中,研究人员使用优化后的DKK1核酸适配体TD10,将其与商业化HCC早期筛查抗体试剂盒进行对比,发现两者检测范围均能达到62.5 ~ 4000 pg/ml,并且使用基于适配体的ELISA的DKK1水平相对于传统方法而言,可以通过修正系数进行调整。此外,基于适配体的ELISA可以进一步降低筛查成本,提高筛查效率,为肝癌早期筛查进一步助力。
在该研究中,研究者使用了不同检测方法后,强烈推荐使用Biacore对适配体性能进行筛查,因为Biacore不仅仅提供亲和力检测数据,同时还呈现了动力学数据,ka表示结合速率常数,代表结合快慢;kd表示解离速率常数,代表解离快慢,通过kd的数据比较获得了优选的慢解离核酸适配体。同时,由于Biacore的动力学检测范围非常广,并且具有极佳的基线稳定性,对于高亲和样品的检测毫无压力,非常适合pM亲和力级别的核酸适配体筛选。除此之外,由于Biacore的传感芯片可以在保证固定分子活性情况下,无限次使用,所以在多批次多类型候选适配体检测过程中,只需要使用1/2块CM5芯片,如果是基于Biacore 8K Series系统,只需要使用1/8块CM5芯片,大大降低研发成本。
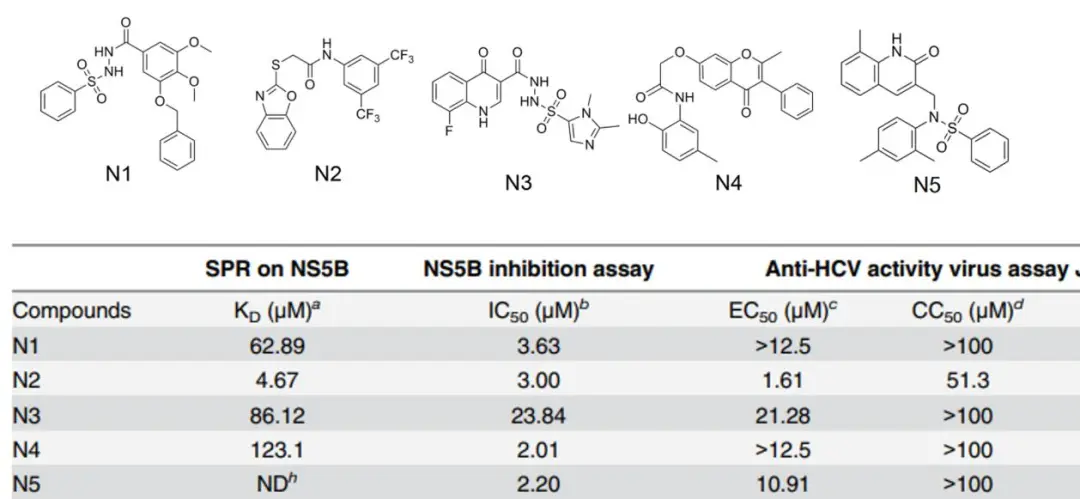
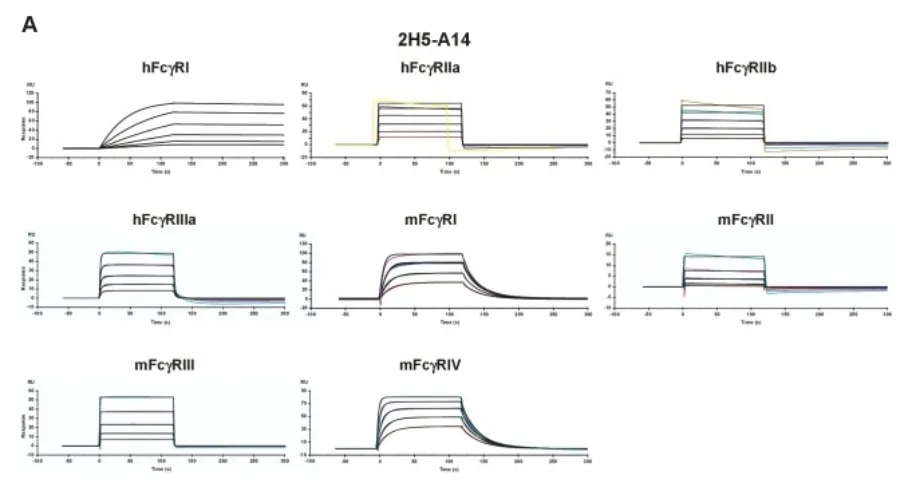
在助力核酸适配体筛选之余,Biacore也同样助力各类不同癌症早筛方法的建立。
同时,Biacore也致力于为各类癌症早筛提供直接检测方案。
作为分子互作的金标准,Biacore在三十多年的积淀中,为各类癌症疾病的筛查、诊断、治疗等领域提供技术支持,为人类健康提供了核心助力。
[1] Yin, Zhou, Wenshuai, et al. Developing slow-off dickkopf-1 aptamers for early-diagnosis of hepatocellular carcinoma[J]. Talanta, 2019.
[2] Enrichment technique to allow early detection and monitor emergence ofKRASmutation in response to treatment[J]. Scientific Reports, 2019, 9(1).
[3] Sato R , Obonai T , Tsumura R , et al. Preparation and characterization of anti-tissue factor single-chain variable fragment antibody for cancer diagnosis[J]. Cancer Science, 2015, 105(12).
[4] Yang C Y , Brooks E , Li Y , et al. Detection of picomolar levels of interleukin-8 in human saliva by SPR[J]. Lab on a Chip, 2005, 5(10):1017-1023.
[5] Shewell L K , Day C J , Kutasovic J R , et al. N-glycolylneuraminic acid serum biomarker levels are elevated in breast cancer patients at all stages of disease. 2021.


 收藏
收藏 询价
询价